
科目: 来源:海南省、文昌中学2017届高三下学期联考化学试卷 题型:填空题
已知丙烯可发生如下的一系列反应,试回答:

(1)聚合物A的名称_____________,丙烯分子中共平面的原子数最多为_________个。
(2)指出反应类型:②__________________,④__________________________。
(3)写出①的化学方程式:_________________________________________。
查看答案和解析>>
科目: 来源:海南省、文昌中学2017届高三下学期联考化学试卷 题型:填空题
废弃物的综合利用既有利于节约资源,又有利于保护环境。实验室利用废旧黄铜(Cu、Zn合金,含少量杂质Fe)制备胆矾晶体(CuSO4·5H2O)及副产物ZnO。制备流程图如下:

已知:Zn及化合物的性质与Al及化合物的性质相似,Zn(OH)2能溶于NaOH溶液。下表列出了几种离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol·L-1计算)。
Fe3+ | Fe2+ | Zn2+ | |
开始沉淀的pH | 1.1 | 5.8 | 5.9 |
沉淀完全的pH | 3.0 | 8.8 | 8.9 |
请回答下列问题:
(1)实验中的过滤操作所用到的玻璃仪器为____________________。
(2)加入ZnO调节pH=a的目的是____________________,a的范围是___________。
(3)由不溶物E生成溶液D的化学方程式为______________________________。
(4)由溶液D制胆矾晶体包含的主要操作步骤是___________,__________,过滤。
(5)若在滤液C中逐滴加入盐酸直到过量,则产生的现象是______________________________。
(6)若废旧黄铜的质量为a g,最终得到的胆矾晶体为b g,则该黄铜中铜元素的质量分数为_____________。
查看答案和解析>>
科目: 来源:海南省、文昌中学2017届高三下学期联考化学试卷 题型:填空题
18-Ⅰ 乙酸香兰酯是用于调配奶油、冰淇淋的食用香精,其合成反应的化学方程式如下:
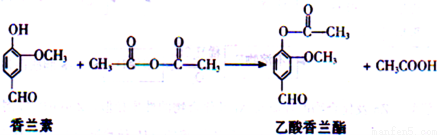

下列叙述正确的是(_____)
A.该反应属于取代反应
B.乙酸香兰酯的分子式为C10H8O4
C.FeCl3溶液可用于区别香兰素与乙酸香兰酯
D.乙酸香兰酯在足量NaOH溶液中水解得到乙酸和香兰素
18-Ⅱ用 A(CH2=CH2)和 D(HOOCCH=CHCH=CHCOOH)合成高分子P,其合成路线如下:
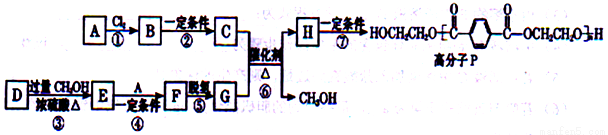
已知:①
②酯与醇可发生如下酯交换反应:

(1)B的名称为_________________,D中官能团的名称为_________________________。
(2)C的分子式是C2H6O2,反应②的试剂和反应条件是____________________________。
(3)F的结构简式是__________________________。
(4)反应⑥的化学方程式是____________________________________。
(5)G的一种同分异构体G'为甲酸酯、核磁共振氢谱有3种峰且1mol该有机物酸性条件下水解产物能与2 mol NaOH反应。G'的结构简式为___________________。
(6)以对苯二甲醇、甲醇为起始原料,选用必要的无机试剂合成G,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。___________________
查看答案和解析>>
科目: 来源:海南省、文昌中学2017届高三下学期联考化学试卷 题型:填空题
19-I下列有关晶体结构或性质的描述中正确的是(______)
A.冰中存在极性键,分子间作用力和氢键
B.因金属性K>Na,故金属钾的熔点高于金属钠
C.各1mol的金刚石与石墨晶体中所含的C-C键的数目相同
D.氧化镁的晶格能大于氯化钠,故其熔点高于氯化钠。
19-Ⅱ某类金属合金也称为金属互化物,比如:Cu9Al4,Cu5Zn8等。请问答下列问题:

(1)基态锌原子的电子排布式为_______________________________;己知金属锌可溶于浓的烧碱溶液生成可溶性的四羟基合锌酸钠Na2[Zn(OH)4]与氢气,该反应的离子方程式为: ___________________________________________________;已知四羟基合锌酸离子空间构型是正四面体型,则Zn2+的杂化方式为__________________。
(2)铜与类卤素(SCN)2反应可生成Cu(SCN)2,1mol (SCN)2分子中含有__________个σ键。类卤素(SCN)2对应的酸有两种:A—硫氰酸(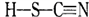 )和B-异硫氰酸(
)和B-异硫氰酸(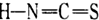 ),两者互为:_________;其中熔点较高的是___________ (填代号),原因是________________________________。
),两者互为:_________;其中熔点较高的是___________ (填代号),原因是________________________________。
(3)已知硫化锌晶胞如图1所示,则其中Zn2+的配位数是____________; S2-采取的堆积方式为____________________。(填A1或A2或A3)
(4)己知铜与金形成的金属互化物的结构如图2所示,其立方晶胞的棱长为a纳米(nm),该金属互化物的密度为_______g/cm3(用含a,NA的代数式表示)。
查看答案和解析>>
科目: 来源:2016-2017学年山西省高一3月月考化学试卷(解析版) 题型:选择题
下列各组性质的比较中正确的是( )
A. 还原性:F->Cl->Br->I- B. 稳定性:HF<HCl<HBr<HI
C. 密度:F2<Cl2<Br2<I2 D. 与H2O反应由易到难:Cl2>Br2>I2>F2
查看答案和解析>>
科目: 来源:2016-2017学年山西省高一3月月考化学试卷(解析版) 题型:选择题
230Th和232Th是钍的两种同位素,232Th可以转化成233U。下列说法中正确的是 ( )
A. Th元素的质量数是232 B. Th元素的相对原子质量是231
C. 232Th转换成233U是化学变化 D. 230Th和232Th的化学性质相同
查看答案和解析>>
科目: 来源:2016-2017学年山西省高一3月月考化学试卷(解析版) 题型:选择题
.如果n为第ⅡA族中某元素的原子序数,则原子序数为(n+1)的元素可能位于( )
A. ⅢA族或ⅢB族 B. ⅣA族 C. ⅠB族 D. ⅠA族
查看答案和解析>>
科目: 来源:2016-2017学年山西省高一3月月考化学试卷(解析版) 题型:选择题
下列关于碱金属元素和卤素的说法中错误的是( )
A. 随核电荷数的增加,碱金属元素和卤素的原子半径都逐渐增大
B. 碱金属元素中,锂原子失去最外层电子的能力最弱;卤素中,氟原子得电子能力最强
C. 溴单质与水的反应比氯单质与水的反应更剧烈
D. 钾与水的反应比钠与水的反应更剧烈
查看答案和解析>>
科目: 来源:2016-2017学年山西省高一3月月考化学试卷(解析版) 题型:选择题
短周期主族元素X、Y、Z、W的原子序数依次增大。X原子的最外层电子数是其内层电子数的2倍,Y是地壳中含量最高的元素,Z2+与Y2-具有相同的电子层结构,W与X同主族。下列说法正确的是( )
A. Y的气态简单氢化物的热稳定性比W的强
B. Y分别与Z、W形成的化合物中化学键类型相同
C. X的最高价氧化物对应的水化物的酸性比W的弱
D. 原子半径的大小顺序:r(W)>r(Z)>r(Y)>r(X)
查看答案和解析>>
科目: 来源:2016-2017学年山西省高一3月月考化学试卷(解析版) 题型:选择题
如果发现了原子序数为116的元素,下列对它的叙述中正确的是 ( )
①位于第7周期
②非金属元素
③最外电子层有6个电子
④没有放射性
⑤属于氧族元素
⑥属于锕系元素
A. ①③⑤ B. ②④⑥ C. ①③⑥ D. ③④⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com