
第二章 认识空气保护空气
2.1 生命活动离不开空气
一、教学目的要求
1.了解空气的主要成分。
2.了解氧气、氮气、稀有气体的主要用途。
3.初步了解空气污染的危害,知道空气是一种宝贵的自然资源,养成关注环境、热爱自然的情感。
4.初步学习科学实验的方法,进行观察、记录,并初步学习分析实验现象。
学生对空气已有一定的知识基础,因此内容的安排既不能与小学自然课中的知识重复,又应以此为基础。本课题包含了三部分,即“空气是由什么组成的”、“空气是一种宝贵的资源”、“保护空气”。这三部分内容相互密切联系,并逐步深入。
三、教学重点、难点
 重点:空气的主要成分及其体积分数,混合物与纯净物
重点:空气的主要成分及其体积分数,混合物与纯净物
难点:混合物与纯净物的概念及其运用
有一种东西看不见、摸不着,却无所不在,与我们密不可分,离开它,我们就无法生存。这是什么呢?―― 空气。
四、教学过程
 ?空气有哪些成份?
?空气有哪些成份?
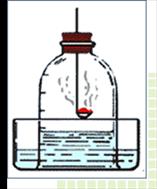
 实验探究:空气有哪些成份?
实验探究:空气有哪些成份?
实验现象:红磷燃烧时有大量白烟生成,同时钟罩内水面逐渐上升,最后反应结束时钟罩内水面上升了大约1/5体积。
结论:通过以上的实验事实,你得到什么结论?
空气并不是一种单一的物质,而是由多种气体组成的,红磷燃烧所消耗的气体是空气中的氧气,空气中剩余成分主要是氮气。
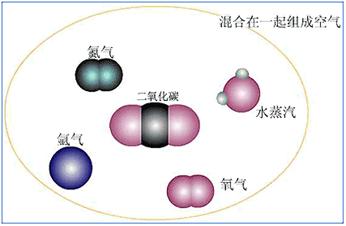
一般来说,空气的成分是比较固定的。按体积分数计算,大约是:氮气78%,氧气21%,稀有气体0.94%,二氧化碳0.03%,其它气体和杂质0.03%。
?氮气与稀有气体
氮气和稀有气体有用吗?
氮气的化学性质稳定,常温下难跟其它物质发生反应,但在高温、高能量条件下可与某些物质发生化学变化,用来制取对人类有用的新物质。
稀有气体
稀有气体是氦、氖、氩、氪、氙、氡等气体的总称,这些气体都是没有颜色,没有气味的。稀有气体一般不跟其它物质发生化学反应。
人们利用稀有气体的这一性质,常把它们用作保护气:如把氩气和氮气的混合气体充入灯泡里,使灯泡经久耐用。
稀有气体在灯管中通电时会发出不同颜色的光。充入氩气,通电时会发出紫蓝色光;充入氦气,通电时会发出粉红色光;充入氖气,通电时会发出红光,这种光能穿透浓雾,
故氖灯可用作航空、航海的指示灯。五光十色的霓虹灯就是利用稀有气体的这种在通电时会发出不同颜色的光的性质制成的。
?怎样区分混合物和纯净物
混合物是由两种或多种物质混合而成的,这些物质相互间没有发生反应,混合物里各种物质都保持原来的性质。例如空气、海水。
混合物的组成不固定,没有一定的性质(如没有固定的熔点、沸点),各成分保持其原有性质。
纯净物是由一种物质组成的。例如氧气、氮气、二氧化碳等都是纯净物。纯净物有一定的性质,如:具有固定的熔点、沸点。
研究任何一种物质的性质,都必须取用纯净物,因为一种物质里如果含有杂质,就会影响这种物质固有的某些性质。但是,有没有100%的完全纯净的物质呢?没有。
通常所谓的纯净物指的是含杂质很少的具有一定纯度的物质。如用作半导体材料的硅,经提纯,硅的质量分数可以达到99.999999999%,这种硅叫做高纯硅。
2.2 探究空气中物质构成的奥秘
一、教学目的要求
1.认识物质是由分子、原子等微小粒子构成的。
2.了解原子的构成、相对原子质量。
3.初步了解核外电子是分层排布的。
4.了解离子形成的过程,认识离子是构成物质的一种微粒。
5.初步了解空气污染的危害,知道空气是一种宝贵的自然资源,养成关注环境、热爱自然的情感。
本课题带领学生进入微观世界。认识物质的微粒性──分子、原子的存在,初步探索了物质构成的奥秘。
本课题的引入还是从简单的宏观物理变化现象着手,引起对分子、原子的原始思索与现代证明略做勾勒。引导学生用分子、原子的观点分析、比较以前学习过的一些变化(物理变化、化学变化),进一步从化学变化中认识分子、原子的特性,形成概念。
原子核外电子的排布和金属、非金属、稀有气体元素原子核外电子层结构的特征与其化学性质的关系。使学生对核外电子分层排布有一个初步认识。
重点:分子、原子和离子的概念及其特性,原子的内部结构,相对原子质量。
难点:解释某些现象,相对原子质量,分子、原子和离子之间的异同点。
四、教学过程:
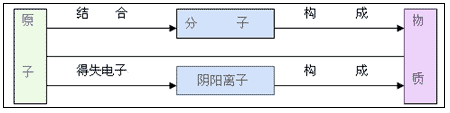
我们周围的世界是由形形色色的物质构成的。我们已经知道,空气中含有多种物质,但这些物质本身是由什么构成的呢?通过长期的实践和科学研究,人们终于搞清并证实,物质是由分子、原子等微粒构成的。
?什么是分子?
一、构成物质的微粒(1)―― 分子
概念:分子是保持物质的化学性质的一种微粒。对分子的认识有以下几点要注意:
1、物质是由微粒构成的,分子是构成物质的一种微粒,构成微粒保持该物质的化学性质。
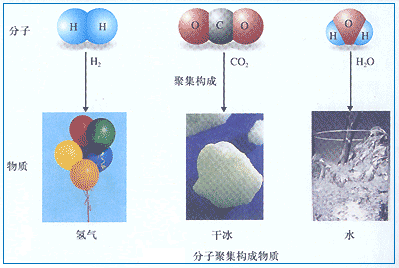
由分子构成的物质其分子保持它的化学性质,如氧气、酒精、香精分别由氧气分子、酒精分子、香精分子构成,故保持氧气、酒精、香精的化学性质的微粒就是氧气分子、酒精分子、香精分子。但物质不仅仅是由分子这一种微粒构成,有些物质如铁、食盐等是由其它一些微粒构成的,所以分子不是保持物质化学性质的唯一微粒。
2、由分子构成的物质发生物理变化时物质的分子没有变。
例如水变成水蒸气时,水分子本身没有变,水的化学性质没有变。由分子构成的物质发生化学变化时,它的分子起了变化,变成了别的分子。例如氨(NH3)和氯化氢( HCl)发生反应,生成了氯化铵。所以由分子构成的物质发生化学变化时,旧分子被破坏形成新的分子,也就形成了新的物质。在物理变化中分子不变,也就没有新物质的生成。
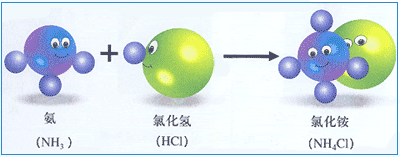
氨气和氯化氢反应生成氯化铵
3、物质的性质既有物理性质也有化学性质。
物质的物理性质如熔点、沸点、密度、硬度等都是该物质大量分子的聚集体所表现的属性,通常所讨论的物理性质都是指宏观现象,并不是每一个单个分子所能表现出来的;而同种物质的每一个分子都有相同的化学性质。所以不能说分子是保持物质性质的一种微粒。
?分子的特性

1、分子总是在不断地运
湿的衣服经过晾晒会变干;这是由于构成水的微粒(分子)在风吹日晒下扩散到空气中去了。糖块在水中溶解,同时水有了甜味,是由于糖的微粒(分子)扩散到水的微粒(分子)中去了。
2、分子间有间隔
气态物质的分子间的间隔很大,而液态和固态物质的分子间的间隔很小。故气态物质易压缩,而液体和固态物质难压缩。
二、构成物质的微粒(2)―― 原子

此图是用扫描隧道显微镜显示硅原子图像的照片,图中的白点表示硅原子
?什么是原子
原子的概念:原子是化学变化中的最小微粒。对原子的认识有以下几点要注意:
1、原子是构成物质的另一种微粒。原子构成分子,原子也可直接构成物质,如金属汞、稀有气体等。
2、在化学变化中,分子本身发生根本改变,而原子本身没有根本改变,只是重新组合成新的分子,构成新的物质。所以,原子是化学变化中的最小微粒。如氧化汞受热时氧化汞分子会分解为氧原子和汞原子,这些原子进行重新组合,每两个氧原子结合成一个氧分子,许多汞原子聚集成金属汞。在化学反应中氧原子和汞原子不能进一步再分成更小的微粒。
?原子的特性
①原子的体积很小,质量也很小,肉眼是看不见原子的。
②原子和分子一样,也是在不断地运动。
③原子间有间隔。
④同种原子性质相同,不同种原子性质不同。
⑤原子在化学变化中不能再分。
?原子的质量有多大
原子虽然很小,但也有一定的质量。不同原子的质量各不相同,下表列出了几种原子的质量。
原子的种类
一个原子的质量 / 千克
氢
1.674×10-27
碳
1.993×10-26
氧
2.657×10-26
铁
9.288×10-26
原子的质量这样小,书写、记忆和使用都不方便,就象用吨作单位来表示一粒稻谷或小麦的质量一样。因而就不直接用原子的实际质量(千克为单位),而采用以一种原子的质量作为比较的标准,得到其它原子质量跟它的比值。
国际上以一种碳原子(原子核内有6个质子和6个中子的一种碳原子)的质量的1/12(约1.66×10-27千克)作为标准,其它原子的质量跟它比较所得的值,就是这种原子的相对原子质量。
相对原子质量的计算方法:
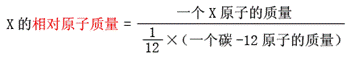
例如,氢原子的质量约等于碳-12原子质量的1/12,所以氢的相对原子质量约等于1。氧原子和铁原子的质量约等于碳-12原子质量的1/12的16倍和56倍,所以氧和铁的相对原子质量分别约等于16和56。
?原子能再分吗?

原子的体积和质量都非常小,那么它是不是构成物质世界的最小微粒呢?它能不能再分呢?
1897年,英国科学家汤姆生发现了电子,并认为一切原子中都含有电子----原子不是构成物质的最小微粒,它本身还具有复杂的结构,还可以再分。
科学证明:原子是由居于原子中心的带正电的原子核和核外电子所构成的。 而原子核又是由带正电荷的质子和不带电荷的中子构成的。
几种原子的构成:
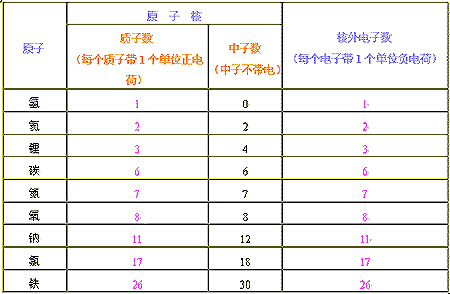
由上表可以得出:

概念:带电荷的原子。在化学变化中,一些原子容易失去电子,而另一些原子则容易得到电子,当原子得到或失去核外电子从而带上电荷以后,便转变成离子(ion)。
三、构成物质的微粒(3)―― 离子
2.3 保护空气的洁净清新
一、教学目的要求
1.初步了解空气污染的危害及其防治方法。
2.了解空气质量检测及其预报。
3.养成关注环境、热爱自然的情感。
学生对空气已有一定的知识基础,因此内容的安排既不能与小学自然课中的知识重复,又应以此为基础。本课题包含了三部分,即“空气是怎样受污染的”、“空气质量的监测”、“保护大气环境”。这三部分内容相互密切联系,并逐步深入。
重点:空气的污染源、空气的污染及其防治。
难点:树立环保概念。
?空气是怎样受污染的
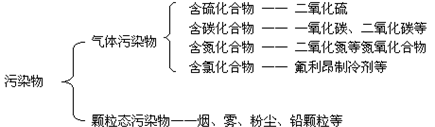
人类的活动往往会造成空气的污染(air pollution),成为空气的各种污染源,如工业污染源、交通污染源和生活污染源等。会造成空气污染物质主要有:
四、教学过程
 ?空气污染危害大(解读空气污染指数和空气质量等级)
?空气污染危害大(解读空气污染指数和空气质量等级)
被污染了的空气会严重地损害人体的健康,影响作物的生长,造成对自然资源的破坏以及对建筑物等的破坏。
【知识视窗】
几种常见空气污染物对人类健康及生态环境的危害
空气污染物
主要来源
突出的危害
二氧化硫
含硫燃料的燃烧
引发呼吸道疾病、严重者死亡;造成酸雨,破坏地面设施
氮氧化物
汽车、飞机等尾气
引发眼睛、呼吸系统炎症;造成酸雨;破坏高空臭氧层等
一氧化碳
汽车尾气、含碳燃料不完全燃烧
破坏人体血液输氧功能,使人死亡等
可吸入颗粒物(粉尘、铅、碳颗粒等)
汽车尾气、建筑、生活等城市垃圾扩散
引发咳嗽、喉病、“尘肺”;导致云雾增多,使能见度降低
?监测空气环境的质量

大气监测车

水电站
为了监测各地大气环境的质量,我国已建立了空气质量日报的制度。空气质量日报的主要内容包括:首要污染物、空气污染指数和空气质量级别三项内容。
?保护好大气环境
既然空气污染给人类和自然带来这么大的危害,所以我们在发展生产的同时,必须要充分认识保护环境的重要性,注意消除污染源,以保障人类的健康和保护自然资源。例如,工厂的废气,必须经过除尘、除污处理,达到国家规定的排放标准,才能向空气中排放;实行煤炭综合利用,减少直接以煤为燃料,改用气体燃料;大力发展水电、核电,改变能源结构;推广使用无铅汽油;植树种草,增加绿化面积。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com