
科目:gzhx 来源: 题型:
| A、氢氟酸能和玻璃的成分SiO2发生化学反应 | ||||
B、根据SiO2+Na2CO3
| ||||
| C、CO2气体通入到Na2SiO3溶液中可以制得硅酸 | ||||
| D、原硅酸不稳定,易失去水分子成为硅酸 |
科目:gzhx 来源: 题型:
| ||
| ||
科目:gzhx 来源: 题型:
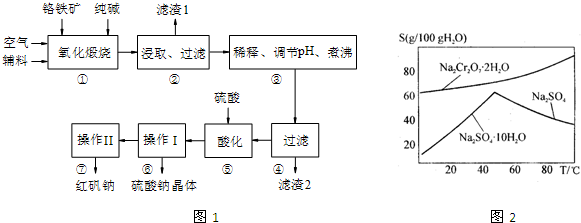
| 高温 |
| 高温 |
| 高温 |
科目:gzhx 来源: 题型:
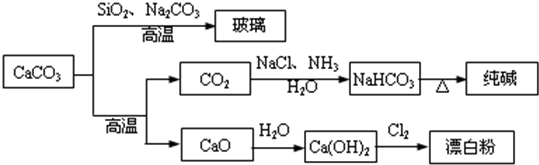
| A、Cl2和SO2均可以漂白有色物质,且漂白的原理相同 | ||||
B、由SiO2+Na2CO3
| ||||
| C、工业上,可先向饱和食盐水中通入NH3后再通入CO2制NaHCO3 | ||||
| D、制取玻璃、纯碱和漂白粉所涉及的反应都是非氧化还原反应 |
科目:gzhx 来源: 题型:
| ||
| ||
科目:gzhx 来源: 题型:阅读理解

| ||
| ||
| ||
| ||
 Cr2O72-+H2O
Cr2O72-+H2O Cr2O72-+H2O
Cr2O72-+H2O科目:gzhx 来源:西城区二模 题型:单选题
A.为减少煤燃烧产生SO2,用CaCO3脱硫:2CaCO3+O2+2SO2
| ||||
| B.为缓解胃酸过多,服含NaHCO3的抗酸药:HCO3-+H+=H2O+CO2↑ | ||||
C.将Na2CO3加热至熔融不能选用石英坩埚:SiO2+Na2CO3
| ||||
| D.将明矾放入浑浊的河水中,可使水澄清:Al3++3H2O=Al(OH)3↓+3H+ |
科目:gzhx 来源:不详 题型:单选题
A.高温煅烧石英和纯碱混合物:SiO2+Na2CO3
| ||||
| B.过量SO2通入到Ba(NO3)2溶液中:3SO2+2 NO3-+3 Ba2++2H2O=3 BaSO4↓+2NO+4H+ | ||||
| C.一定量的Cl2通入到FeBr2溶液中:FeBr2+Cl2=FeCl2+Br2 | ||||
| D.金属Na投入到CuSO4溶液中:2Na+Cu2+=2Na++Cu |
科目:gzhx 来源: 题型:阅读理解
| ||
| ||
| ||
| ||
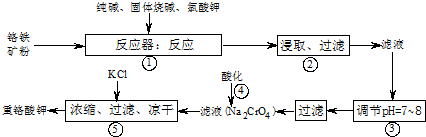
 HSiO3-+OH-、HSiO3-+H2O
HSiO3-+OH-、HSiO3-+H2O H2SiO3+OH-、AlO2-+2H2O
H2SiO3+OH-、AlO2-+2H2O Al(OH)3+OH-,降低pH有利于水解平衡向正反应方向移动,当pH调到7~8时能使它们完全水解生成沉淀
Al(OH)3+OH-,降低pH有利于水解平衡向正反应方向移动,当pH调到7~8时能使它们完全水解生成沉淀 HSiO3-+OH-、HSiO3-+H2O
HSiO3-+OH-、HSiO3-+H2O H2SiO3+OH-、AlO2-+2H2O
H2SiO3+OH-、AlO2-+2H2O Al(OH)3+OH-,降低pH有利于水解平衡向正反应方向移动,当pH调到7~8时能使它们完全水解生成沉淀
Al(OH)3+OH-,降低pH有利于水解平衡向正反应方向移动,当pH调到7~8时能使它们完全水解生成沉淀| 294×c×V×V2 |
| 6×1000×V1×m |
| 294×c×V×V2 |
| 6×1000×V1×m |
科目:gzhx 来源: 题型:
(9分)粉煤灰是燃煤电厂排出的工业废渣,其中含莫来石(Al6Si2O13)的质量分数为43.4%,还有含量
较多的SiO2(其他成分不含Al和Si)。用粉煤灰和纯碱在高温下烧结,可制取NaAlSiO4(霞石)、Na2SiO3
和NaAlO2,有关化学方程式为:
Al6Si2O13 + 3Na2CO3 = 2NaAlSiO4+ 4NaAlO2 + 3CO2↑ ①
Al6Si2O13 + 5Na2CO3 = 2Na2SiO3 + 6NaAlO2 + 5CO2↑ ②
SiO2 + Na2CO3 = Na2SiO3 + CO2↑ ③
⑴粉煤灰中铝的质量分数为 % (精确到0.1%)
⑵用1 mol Al6Si2O13 和 4 mol SiO2制得5mol NaAlO2、1mol NaAlSiO4,还应制得Na2SiO3____________mol,共消耗Na2CO3 mol(得到的固体中无SiO2)。
⑶若粉煤灰中 Al6Si2O13 与 SiO2的物质的量之比为1:2,则1kg粉煤灰与6mol Na2CO3反应(反应物全部都参与反应),可制得NaAlO2 mol。(精确到0.01)
⑷若用100 mol Al6Si2O13同时生产NaAlSiO4和NaAlO2,且n(NaAlSiO4):n(NaAlO2) = x,消耗Na2CO3 y mol,试确定y与x的关系式[即表示为y=f(x)]。
科目:gzhx 来源:必修一导学指导化学鲁科版 鲁科版 题型:021
|
下列说法正确的是 | |
A. |
二氧化硅是酸性氧化物,它可以跟强碱反应,但不能与任何酸反应 |
B. |
根据SiO2+CaCO3 |
C. |
二氧化碳气体通入硅酸钠溶液中可以制得硅酸 |
D. |
二氧化硅对应的水化物有不同的组成 |
科目:gzhx 来源:教材完全解读 苏教版课标版 高中化学 必修1 苏教版课标版 题型:021
|
下列说法正确的是( ). | |
A. |
二氧化硅是酸性氧化物,它可以跟强碱反应,但不能与任何酸反应 |
B. |
根据SiO2+CaCO3 |
C. |
二氧化碳气体通入硅酸钠溶液中可以制得硅酸 |
D. |
二氧化硅对应的水化物有不同的组成 |
科目:gzhx 来源:龙之脉新教材完全解读 高中化学 必修1 配鲁科版 鲁科版 题型:021
|
下列说法正确的是 | |
A. |
二氧化硅是酸性氧化物,它可以跟强碱反应,但不能与任何酸反应 |
B. |
根据SiO2+CaCO3 |
C. |
二氧化碳气体通入硅酸钠溶液中可以制得硅酸 |
D. |
二氧化硅可制取光导纤维 |
科目:gzhx 来源: 题型:
| ||
| ||
科目:gzhx 来源: 题型:
| ||
| ||
科目:gzhx 来源: 题型:
| ||
| ||
| ||
| ||