
题目列表(包括答案和解析)
30.为了制取碘,可通过反应:2NO+O2==2NO2 NO2+2H++2I-==NO+I2+H2O制得,NO在制碘过程中的作用是 A.还原剂 B.氧化剂 C.催化剂 D.反应物
29.工业上由粗硅制取纯硅有以下反应:
①Si+3HCl(气 ) 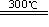 SiHCl3(气)+H2 (为放热反应)
②SiHCl3(气)+H2
SiHCl3(气)+H2 (为放热反应)
②SiHCl3(气)+H2 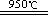 Si+3HCl(气)
Si+3HCl(气)
对上述反应的说法不正确的是: A.均为置换反应 B.反应①②实际上互为可逆反应 C.由于反应①放热,则反应②一定吸热 D.反应①②都是氧化还原反应
28.下列说法正确的是(N0表示阿伏伽德罗常数的值) A.标准状况下,以任意比例混和的甲烷和丙烷混和物22.4L,所含有的分子数为N0 B.标准状况下,1L辛烷完全燃烧后,所生成气态产物的分子数为8N0/22.4 C.常温常压下,活泼金属从盐酸中置换出22.4L H2,发生转移的电子数为2N0 D.常温常压下,1mol氦气含有的核外电子数为4N0
27.下列“反应”中不是化学变化的是 A.显色反应 B.焰色反应 C.颜色反应 D.水解反应
26.下列物质不能通过化合反应得到的是 A.Fe(OH)3 B.FeCl3 C.H2SiO3 D.NaHCO3
25.在一定温度下,向a L密闭容器中加入1 mol X气体和2mol Y气体,发生如下反应:X(g) + 2Y(g) 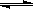 2Z(g)
,此反应达到平衡的标志是
A.容器气体的总物质的量不随时间变化
B.V正(X)=v逆(Z)
C.容器内X、Y、Z的浓度之比为l : 2 : 2
D.单位时间消耗0.1 mol X同时生成0.2 mol Z
2Z(g)
,此反应达到平衡的标志是
A.容器气体的总物质的量不随时间变化
B.V正(X)=v逆(Z)
C.容器内X、Y、Z的浓度之比为l : 2 : 2
D.单位时间消耗0.1 mol X同时生成0.2 mol Z
24.有关下列三个化学反应的叙述,正确的是 ①2H2S+SO2=3S+2H2O
②S+2H2SO4(浓)=3SO2↑+2H2O ③3S+6KOH=2K2S+K2SO3+3H2O A.反应①说明SO2能与酸反应,具有碱性氧化物的性质 B.反应②改用稀H2SO4,则能放出H2 C.反应②和③说明S具有两性元素的性质 D.反应③说明S既有氧化性又有还原性
23.现有碳酸钠、氢氧化钡和硫酸三种体积和物质的量浓度都相等的溶液,几位同学按不同顺序将它们混合(产生的沉淀立即过滤掉),对于最后所得溶液,下列说法正确的是 A.一定显碱性 B.不可能显碱性 C.不可能显中性 D.不可能显酸性
22.下列说法正确的是 A.阳离子只有氧化性,阴离子只有还原性. B.某元素的单质的氧化性很强,则它的离子的还原性很强 C.得电子越多的氧化剂,其氧化性就越强 D.元素的单质可能由氧化或者是还原含该元素的化合物来制取.
21.下列关于胶体的叙述,不正确的是 A.有色玻璃是固溶胶 B.实验室可用饱和FeCl3溶液滴入沸水中来制取氢氧化铁胶体 C.用滤纸能把胶体中的分散质与分散剂分离 D.胶粒大小直径在1nm-100nm之间
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com