
题目列表(包括答案和解析)
4.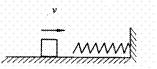 如图所示,物体p以一定的初速度沿光滑水平面向右运动,与一个右端固定的轻质弹簧相 撞,并被弹簧反向弹回。若弹簧在被压缩过程中始终遵守胡克守律,那么在p与弹簧发生相互作用的整个过程中:
如图所示,物体p以一定的初速度沿光滑水平面向右运动,与一个右端固定的轻质弹簧相 撞,并被弹簧反向弹回。若弹簧在被压缩过程中始终遵守胡克守律,那么在p与弹簧发生相互作用的整个过程中:
A. P做匀变速直线运动
B. p的加速度大小不变,但方向改变一次
C. p的加速度大小不断改变,当加速度数值最大时,速度最小
D.有一段过程,p的加速度逐渐增大,速度也逐渐增大
3.用20N的水平外力F,拉一个放在光滑水平面上静止的质量为20kg的物体,力F作用2s 后消失,则第5s末物体的速度和加速度分别为:
A, 2m/s, 1.5m/s2 B, 2m/s, 1.Om/s2
C、2m/s, 0 D, 5 m/s, 0
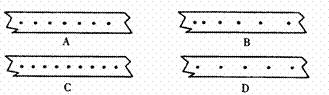
2、如图所示的为同一打点计时器打出的4条纸带,加速度最大的纸
带是:
1、 a、b两物体从同一位置沿同一直线运动,它们的速度图象
a、b两物体从同一位置沿同一直线运动,它们的速度图象
如图所示,下列法正确的是:
A.a、b加速时,物体a的加速度大于物体b的加速度
B. 20秒时,a, b两物体相距最远
C. 60秒时,物体a在物体b的前方
D. 40秒时,a, b两物体速度相等,相距200m
31.(14分)1928年,英国生物学家格里菲思(F·Griffith)想研制出抗肺炎双球菌的疫苗。当时,他选择了两种肺炎双球菌,带有荚膜.有毒的S型细菌(注射到小鼠体内,小鼠死亡)和无荚膜.无毒的R型细菌(注射到小鼠体内,小鼠不死亡)。格里菲思通过实验:①将加热杀死后的S型细菌注射到小鼠体内,小鼠不死亡,②将加热杀死的S型细菌和R型活细菌混合注射到小鼠体内,会使小鼠致死。检查死鼠血样,发现其体内竟然存在有S型活细菌。请依据上述材料回答:
(1)格里菲思根据实验得出的结论是_______________________________________。
(2)小鼠体内产生的抗肺炎双球菌抗体的化学本质是_____________。
(3)肺炎双球菌与酵母菌在结构上最主要的区别是_______________。
(4)有人设想R型细菌可以作为S型细菌的疫苗增强小鼠的免疫力。
请你根据提供的实验材料和用具,写出第二步及以后的实验步骤,并回答问题:
实验目的:探究R型细菌是否可以作为S型细菌的疫苗
实验原理:(略)
实验材料和用具:小鼠若干只.S型活细菌.R型活细菌.生理盐水.注射器等。(提示:可用生理盐水配制一定浓度的活菌数,但浓度和剂量不作要求)
实验过程:
第一步:取小鼠若干只,均等地分为两组,编号为甲组和乙组。
第二步:在甲组体内注射________________________________________________________,在乙组体内注射________________________________________________________。
第三步:______________________________________________________________________
30.(28分)Ⅰ.(17分)人体在正常情况下,血糖含量在80-120 mg/dL的范围内保持相对稳定,对于保证人体各种组织和器官的能量供应,进而保持人体的健康,有着非常重要的意义。请回答下面有关糖代谢的问题:
(1)_________________是人体血糖调节中枢部位。
(2)人体的血糖的去路是________________________________________________________
________________________________________________________________________。
(3)糖尿病患者机体逐渐消瘦的原因_________________________________________。
(4)近年来,对胰岛素作用机制的研究进一步深入,对其作用的信号通路已比较清楚。A.B所示细胞通讯方式为人体内常见的两种不同类型的信号分子及其信号传导方式,C.D表示不同的信号分子对靶细胞作用的方式。据下图分析,符合胰岛素作用信号通路是图中的_____________________

(5)如果某人的胰岛素含量并不低,但却出现了典型的糖尿病患者症状,根据上图,你认为可能的原因是_____________________________________________________。
(6)有学者曾设想提取哺乳动物的胰岛素,但将绵羊的胰脏制成研磨液,却难以直接分离出胰岛素的最可能的原因是________________________________________________。
(7)根据你所学知识结合现代科技成果,请你提出治疗糖尿病的两个方案。(写出思路即可)
①_____________________________________________________________________________
②_____________________________________________________________________________
Ⅱ.(11分)甘蔗是我国南方的一种重要的经济作物。据此回答:
(1)如果用显微镜观察甘蔗叶片的横切面,可以发现围绕其维管束的是呈___________的两圈细胞,其合成淀粉的场所是________________________________________。
(2)用含32P的完全营养液培养甘蔗幼苗,几天后在叶片中检测到32P,其中参与光反应的反应物中含有32P的有机物有________________等。
(3)在利用叶肉细胞获得原生质体后,需要对其活力进行检查,下列哪种实验最适合?________。
A.观察原生质体的结构是否完整 B.观察细胞质流动
C.观察细胞的有丝分裂 D.观察叶绿体的形态和数目
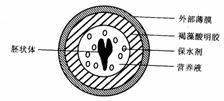 (4)目前通过生物技术可以生产如图所示的人工种子,制造人工种子的原理是在植物组织培养得到的“胚状体”的最外面用一层有机膜包裹,并在薄膜以内放入一些营养物质,这层膜和这些营养物质分别具有种皮和胚乳的功能,在制造过程中还可以加入某些农药.菌肥等。由离体的植物体细胞形成胚状体的过程中要经过的两个重要的生理过程是______________________和______________________,在这一过程中被培养的细胞始终受______
的调节。
(4)目前通过生物技术可以生产如图所示的人工种子,制造人工种子的原理是在植物组织培养得到的“胚状体”的最外面用一层有机膜包裹,并在薄膜以内放入一些营养物质,这层膜和这些营养物质分别具有种皮和胚乳的功能,在制造过程中还可以加入某些农药.菌肥等。由离体的植物体细胞形成胚状体的过程中要经过的两个重要的生理过程是______________________和______________________,在这一过程中被培养的细胞始终受______
的调节。
(5)从保证甘蔗人造种子正常生命力及与生态系统的物质循环上来看,其外部薄膜(人工种皮)应具有 和 的特点。
(6)在甘蔗人工种子中被包入的菌肥通常是 。
29. (13分)Cu(NO3)2受热分解后的产物为不含氮元素的固体.NO2和O2,CuO在一定温度下可发生下列反应:
(13分)Cu(NO3)2受热分解后的产物为不含氮元素的固体.NO2和O2,CuO在一定温度下可发生下列反应: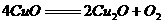 ,试回答下列问题:
,试回答下列问题:
(1)若Cu(NO3)2受热分解后生成的NO2和O2的物质的量之比为4:1,则铜元素的化合价在分解前后是否发生了变化___________(填“改变”或“不变”),其理由是________________________________________________________________________________
(2)若称到
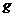 Cu(NO3)2强热使其分解得到NO2和O2,还有
Cu(NO3)2强热使其分解得到NO2和O2,还有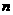
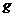 固体。将气体用水充分吸收后还有残余气体同时得到100
固体。将气体用水充分吸收后还有残余气体同时得到100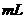 溶液,则该溶液物质的量浓度为_________mol.L-1(用含
溶液,则该溶液物质的量浓度为_________mol.L-1(用含 的式子表示)。
的式子表示)。
(3)若(2)中 =3.76
=3.76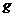 ,
,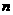 =1.52
=1.52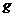 ,试通过计算求残留固体的成分及其质量。
,试通过计算求残留固体的成分及其质量。
28. (15分)长期存放的亚硫酸钠可能会被空气中的氧气氧化。某化学兴趣小组通过实验来测定亚硫酸钠试剂的被氧化的程度,设计了右图实验:请回答下面的问题:
(15分)长期存放的亚硫酸钠可能会被空气中的氧气氧化。某化学兴趣小组通过实验来测定亚硫酸钠试剂的被氧化的程度,设计了右图实验:请回答下面的问题:
(1)若将虚线框内的分液漏斗换成长颈漏斗,
则应该怎样检查虚线框内装置的气密性? 。
(2)D装置中反应的化学方程式为
。B装置中反应的离子方程为 。
(3)称量ag Na2SO3样品放入锥形瓶中,向B装置反应后的溶液中加入足量的BaCl2溶液充分反应,过滤.洗涤.干燥,得白色沉淀bg,原样品中Na2SO3的质量分为数为 。
(4)为保证实验测定的准确性,则C装置中反应的离子方程式为 。
(5)现有以下试剂:①蒸馏水.②稀盐酸.③稀硝酸.④BaCl2溶液.⑤Ba(NO3)2溶液,请从中选择合适试剂,设计一种不同的实验方法测定试样中无水亚硫酸钠被氧化的程度
。
27.(共15分)已知由短周期元素组成的A.B.C.D四种化合物所含原子数目依次为2.3.4.5,其中A.B.C含有18个电子,D含有10个电子。请回答
(1)A.B.D的化学式分别是A ;B ;D
(2)已知8gD与O2完全反应,生成稳定化合物时放出445kJ的热量,写出反应的热化学方程式
(3)若C为第一和第三周期元素组成的化合物,C在空气中能够自燃生成两种常见的氧化物,写出化学方程式
若C为第一和第二周期元素组成的化合物。
①C的溶液中加入少量的二氧化锰,有无色气体生成,写出化学方程式
②C的溶液中加入足量二氧化锰和稀硫酸,二氧化锰逐渐溶解生成Mn2+,反应中二氧化锰做 剂
③当C分别发生①和②两个反应时,若都有1molC完全反应,①和②两个反应中转移电子数之比是:
26.(17分 )亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖.油脂的漂白与杀菌。以下是过氧化氢法生产亚氯酸钠的工艺流程图:
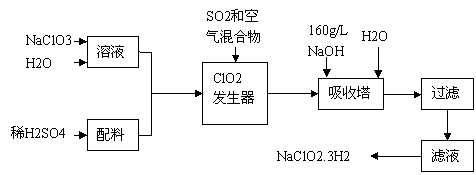
已知:①NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2.3H2O。
②纯ClO2易分解爆炸,一般用稀有气体或空气稀释到10%以下安全。
③160 g/L NaOH溶液是指160 g NaOH固体溶于水所得溶液的体积为1 L。
(1)160 g/L NaOH溶液的物质的量浓度为 。若要计算该溶液的质量分数,还需要的一个条件是 (用文字说明)。
(2)发生器中鼓入空气的作用可能是 (选填序号)。
a.将SO2氧化成SO3,增强酸性;
b.稀释ClO2以防止爆炸;
c.将NaClO3氧化成ClO2
(3)吸收塔内的反应的化学方程式为 。吸收塔的温度不能超过20℃,其目的是 。
(4)在碱性溶液中NaClO2比较稳定,所以吸收塔中应维持NaOH稍过量,判断NaOH是否过量的简单实验方法是 。
(5)吸收塔中为防止NaClO2被还原成NaCl,所用还原剂的还原性应适中。除H2O2外,还可以选择的还原剂是 (选填序号)。
a.Na2O2 b.Na2S c.FeCl2
(6)从滤液中得到NaClO2.3H2O粗晶体的实验操作依次是 (选填序号)。
a.蒸馏 b.蒸发 c.灼烧 d.过滤 e.冷却结晶
要得到更纯的NaClO23H2O晶体必须进行的操作是 (填操作名称)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com