
题目列表(包括答案和解析)
1、 化学在古代的应用与发展。 如_________、_________、_________、_______等
2、物质的变化
(1)物理变化______________________________________________________________.
(2)化学变化________________________________________________________________.
特征___________________________________________________________________.
现象___________________________________________________________________.
物理变化和化学变化的关系_______________________________________________.
3物质的性质
(1)物理性质:物质_______________________就能表现出来的性质,包括_______、______、_________、_________以及两点________、________三度________、_________、________
(2)化学性质:物质在___________中表现出来的性质。如:碱式碳酸铜受热分解是化学性质,其分解的化学方程式为_________________________________
1、化学科学就是在______________水平上研究物质的______ _______ _____ ______ ____________________自然科学,
22、⑴CH3CH2CH2CH3 正丁烷 CH3—CH—CH3 异丁烷
⑵B为甲烷,C为丙烯 或B为乙烷,C为乙烯
⑶C只能是丙烯
[解析]设烷烃B的分子式为CnH2n+2,其相对分子质量为MB;烯烃C的分子式为CmH2m,其相对分子质量为MC.根据质量守恒定律,链烃A的分子式为Cn+mH2(n+m)+2,可见A为烷烃。据题意:MA=MB+MC=2×14.5×2=58,即14(n+m)+2=58,n+m=4。所以A为C4H10。
⑵讨论 n+m=4
当n=1时,m=3即B为甲烷,C为丙烯;
当n=2时,m=3,即B为乙烷,C为乙烯;
当n 3时,m
3时,m 1,无意义
1,无意义
⑶从B的燃烧反应来看:CH4+2O2
→CO2+2H2O,C2H6+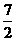 O2
O2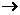 2CO2+3H2O,要求1molB完全燃烧的耗氧量(mol)为整数,可见B为甲烷,则C只能为丙烯。
2CO2+3H2O,要求1molB完全燃烧的耗氧量(mol)为整数,可见B为甲烷,则C只能为丙烯。
21、⑴CH3CH3+Cl2 CH3CH2Cl
取代反应
CH3CH2Cl
取代反应
⑵CH2=CH2+Br2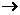 CH2BrCH2Br
加成反应
CH2BrCH2Br
加成反应


 ⑶
⑶ ⑷ +HNO3
⑷ +HNO3 NO2+H2O
取代反应
NO2+H2O
取代反应
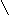

 CH3
O2N
CH3 NO2
CH3
O2N
CH3 NO2
 ⑷
+3HNO3
⑷
+3HNO3 +3H2O
取代反应
+3H2O
取代反应
NO2

 ⑸ +3H2
⑸ +3H2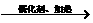 加成反应
加成反应
 ⑹CH2=CH2+3O2
⑹CH2=CH2+3O2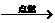 2CO2+2H2O 氧化反应
CH3
2CO2+2H2O 氧化反应
CH3
20、
|
组合编号 |
A的分子式 |
B的分子式 |
A和B的体积比(VA:VB) |
|
① |
CH4 |
C3H6 |
1:3 |
|
② |
CH4 |
C4H8 |
1:1 |
|
③ |
C2H6 |
C3H6 |
1:1 |
|
④ |
C2H6 |
C4H8 |
3:1 |
[解析]:设混合气体的平均分子式为CxHy,因为同温同压下气体的体积比等于物质的量之比,所以1mol混合烃充分燃烧可生成2.5molCO2,即x=2.5,故混合烃平均分子式为C2.5Hy。可推断,混合气体只能由碳原子数小于2.5的烷烃(CH4和C2H6)和碳原子数大于2.5的烯烃(C3H6和C4H8)组成。它们有四种可能的组合,根据每一种组合中烷烃和烯烃的碳原子数及平均分子式中碳原子数,可以确定A和B的体积比。
以第①组为例,用十字交叉法确定VA:VB。

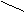 (CH4) 1
0.5
(CH4) 1
0.5

 2.5
2.5
(C3H6)3
1.5
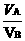 =
=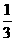
其他组同理可以用十字交叉法确定出VA:VB
19、C5H10


 CH2=C—CH2—CH3 CH3—C=CH—CH3 CH3—CH—CH=CH2
CH2=C—CH2—CH3 CH3—C=CH—CH3 CH3—CH—CH=CH2
CH3 CH3 CH3
[解析]据烯烃的通式CnH2n,可知烯烃的相对分子质量为14n,由题意可知n=70÷14=5;
则该烯烃为戊烯,与氢加成后为戊烷,据题意可写出有三个甲基的戊烷为
① ② ③
 CH3—CH—CH2—CH3 其双键可在①②③三个位置,从而写出三种可能的结构简式即可。
CH3—CH—CH2—CH3 其双键可在①②③三个位置,从而写出三种可能的结构简式即可。
CH3
18、由CxHy+(x+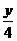 )O2→xCO2+
)O2→xCO2+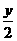 H2O,△V=x+
H2O,△V=x+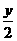 -1-x-
-1-x-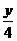 =
=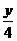 -1由题意可知,△V=1即y=8(混合烃的平均氢原子数),这表明混合烃中要么两种烃的氢原子数都是8,要么一种烃的氢原子数少于8,而另一种的氢原子数多于8,仅有B项不符合此条件。
-1由题意可知,△V=1即y=8(混合烃的平均氢原子数),这表明混合烃中要么两种烃的氢原子数都是8,要么一种烃的氢原子数少于8,而另一种的氢原子数多于8,仅有B项不符合此条件。
8、只能生成三种沸点不同的产物,即只存在三种同分异构体,亦即在分子中只存在三种氢。A中有5种,B中有2种,C中有2种。
[解析]:
5、由CH4+2O2 →CO2+2H2O可知,甲烷要在氧气中完全燃烧,甲烷与氧气的比要 1:2,由此可排除A项;由题意可知,所得白色沉淀为碳酸钙,据碳元素守恒,n(CH4)=n(C)=n(CaCO3)=0.001mol,所以n(O2)=0.007mol。故选D。
1:2,由此可排除A项;由题意可知,所得白色沉淀为碳酸钙,据碳元素守恒,n(CH4)=n(C)=n(CaCO3)=0.001mol,所以n(O2)=0.007mol。故选D。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com