
题目列表(包括答案和解析)
6.把Al放入过量盐酸中,不影响产生H2速率的因素是( )
A 盐酸的浓度 B 铝的表面积
C 溶液的温度 D 加少量的硫酸钠
5.下列能源中不属于化石能源的是( )
A 天然气 B 氢气 C 煤 D 石油
4.下列各组粒子属于同位素的是( )
A 35Cl和37Cl B 40K和40Ca C O2和O3 D H2O和D2O
3.下列物质中所含化学键类型不相同的是( )
A Cl2 B H2O C NaOH D CaCl2
2.下列化合物中所有化学键都是共价键的是( )
A Na2O2 B NaOH C BaCl2 D H2SO4
1.属于短周期的金属元素共有( )
A 3种 B 4种 C 5种 D 6种
25、(14分)学习了元素周期律后,同学们对第四周期过渡元素氧化物产生了浓厚的兴趣。是否只有二氧化锰能催化氯酸钾受热分解?氧化铁、氧化铜、氧化铬等对氯酸钾的受热分解有没有催化作用?对此他们进行了实验探究。请你根据要求完成下列部分实验报告。
I 课题名称:____________________________________________________________
II实验仪器及试剂:
实验仪器:带铁夹的铁架台、带橡皮塞的导管、量气装置、过滤装置、电子天平、药匙、大试管、酒精灯、计时器等。
实验试剂:二氧化锰、氧化铁、氧化铜、氧化铬和氯酸钾
III 实验步骤:略
IV 实验数据:
|
实验 编号 |
KClO3(g) |
氧化物 |
产生气体(mL) |
耗时(s) |
||
|
化学式 |
质量(g) |
回收 |
(已折算到标况) |
|||
|
1 |
0.60 |
- |
- |
- |
10 |
480 |
|
2 |
0.60 |
MnO2 |
0.20 |
90% |
67.2 |
36.5 |
|
3 |
0.60 |
CuO |
0.20 |
90% |
67.2 |
79.5 |
|
4 |
0.60 |
Fe2O3 |
0.20 |
90% |
67.2 |
34.7 |
|
5 |
0.60 |
Cr2O3 |
0.20 |
异常 |
67.2 |
188.3 |
V 实验讨论:
(1)实验编号1的实验作用是 。
(2)实验编号3的实验中KClO3的分解率为_________%(保留一位小数)
(3)在用Cr2O3 做研究实验时,发现有刺激性气味的气体产生,同时绿色的混合物变成了橘黄色。该刺激性气体可能是________(填分子式),可用______________试纸检验。上述异常现象产生的原因是___________________________________。
VI 实验结论:_____________________________________________________________
24、(12分)工业上用铝土矿(含氧化铝、氧化铁)制取铝的过程如下:
请回答下列问题:
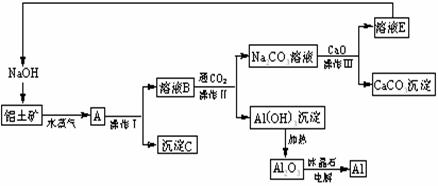
(1)操作I、操作II、操作III都是________________(填操作名称),实验室要洗涤Al(OH)3沉淀应该在________________装置中进行。
(2)生产过程中,除NaOH、H2O可以循环使用外,还可以循环使用的物质有________(填化学式)。用此法制取铝得到的副产品是________(填化学式)。
(3)写出Na2CO3溶液与CaO反应离子方程式:__________________________________。
(4)若铝土矿中还含有二氧化硅,此生产过程中得到的氧化铝将混有杂质:___(填化学式)。
23、(14)下表是元素周期表的一部分。表中所列的字母分别代表某一化学元素。
|
b |
|
|
|||||||||||||||
|
|
|
|
|
h |
|
j |
|
|
|||||||||
|
a |
c |
f |
|
|
i |
l |
m |
||||||||||
|
|
|
|
e |
|
|
|
|
|
|
|
|
|
g |
|
|
|
|
|
|
d |
|
|
|
|
|
|
|
|
|
|
|
|
|
k |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(1)下列 (填写编号)组元素的单质可能都是电的良导体。
①a、c、h ②b、g、k ③c、h、1 ④d、e、f
(2)原子半径最小的元素 单质化学性质最稳定的元素是 (均填元素符号)。
(3)最高价氧化物对应水化物酸性最强的是 (填化学式)
(4)j、i对应的离子还原性由强到弱顺序为 (填离子符号)
(5)设计实验比较a、c的金属性强弱
22、(10分)A.B.C.D.E都是元素周期表中前20号元素,原子序数依次增大,B、C、D, 同周期,A、D同主族,E与其它元素既不在同周期也不在同主族,B、C、D的最高价氧化物的水化物两两混合均能发生反应,D的单质为淡黄色固体。根据以上信息,回答下列问题:
(1)A和D的氢化物中,稳定性较弱的是 (选填A或D);A和B的离子中,半径较小的是 (填离子符号 )。
(2)元素C在元素周期表中的位置是 。(3)E元素的名称是 。
(4)写出C、D的最高价氧化物的水化物之间反应的离子方程式
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com