
题目列表(包括答案和解析)
3.下列关于元素周期表中8号元素和16号元素的说法错误的是 ( )
A.具有相同的最外层电子数 B.可以形成两种氧化物
C.位于同一周期 D.位于同一主族
2.与化学反应速率无关的是
A.浓度 B.密度 C.温度 D.催化剂
1.世界上第一张元素周期表是由下列哪位科学家绘制完成的: ( )
A.道尔顿 B.勒夏特列 C.拉瓦锡 D.门捷列夫
22.(8分)烟气脱硫是控制二氧化硫污染的主要技术手段。利用海水脱硫是一种有效的方法,其工艺流程如下图所示:

某研究小组为探究提高含硫烟气中SO2的吸收效率的措施,进行了天然海水吸收含硫烟气的模拟实验,实验结果如下图所示。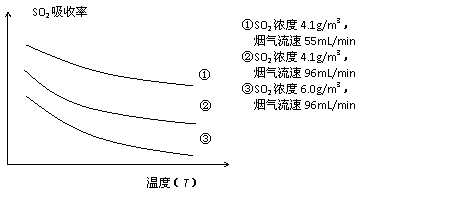

(1)根据图示实验结果,为了提高一定浓度含硫烟气中SO2的吸收效率,下列措施正确的是 。
①降低通入含硫烟气的温度 ②减小通入含硫烟气的流速
③减少天然海水的进入量 ④在天然海水中加入生石灰
(2)天然海水吸收了含硫烟气后会溶有H2SO3,使用空气中的氧气将其氧化,写出该反应的化学方程式 。
(3)某电厂用煤300吨(煤中含硫质量分数为2.5%),若燃烧时煤中的硫全部转化成二氧化硫,用石膏湿法烟气脱硫中有96%的硫转化为石膏(CaSO4·2H2O),则可生产石膏 吨。(写出计算过程)
21.(10分)镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取的。从海水中提出镁的主要步聚如下:
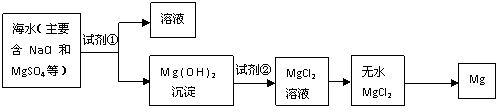

⑴ 为了使MgSO4转化为Mg(OH)2,试剂①可以选用(填化学式)______________。
⑵ 试剂②可以选用(填名称)_________。相关反应的离子方程式________________________________。
⑶ 写出由无水MgCl2制备Mg的化学方程式________________________________。
⑷ 镁粉和铝粉的混合物,溶于足量盐酸后,加过量的 NaOH溶液,过滤,将沉淀完全收集后,充分加热,直至质量不再变化,则得到的物质是_________。
20.(14分)已知:①A是石油裂解气的主要成份,A的产量通常用来衡量一个国家的石油化工水平;②2CH3CHO+O2 2CH3COOH。现以A为主要原料合成乙酸乙酯,其合成路线如图所示。
2CH3COOH。现以A为主要原料合成乙酸乙酯,其合成路线如图所示。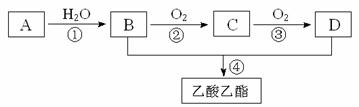
回答下列问题:
(1)有10个氢原子的烷烃的分子式为 ;
(2)C4-C10的烃类混合物含有 (填“等于”、“少于”或“多于”)7种不同的物质
(3)A的结构简式 ; D分子中的官能团名称是 ;
(4)C的分子式 ;①的反应类型是 。
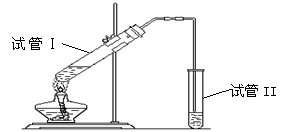 (5)实验室用右图所示装置制备少量乙酸乙酯。
(5)实验室用右图所示装置制备少量乙酸乙酯。
①写出制备乙酸乙酯的化学方程式
②试管I中盛有由_________________________ _组成的反应混合液。
③试管II中的盛有______________。
④甲、乙两种有机化合物,当混合质量一定时,无论甲、乙以何种比洌混合,完全燃烧时产生的CO2的量为一定值,则符合上述条件的是_______
a同分异构体 b同系物 c各元素的原子个数比相同 d含碳的质量分数相等
A.ac B.bd C.acd D.abcd
19.(10分) 某化学课外活动小组将氯化钠固体中混有的硫酸钠、碳酸氢铵杂质除去并得到氯化钠溶液,设计了如下方案:
|
|
|

|
|
|
⑴ 操作①的目的是 ,操作④的名称是 。
⑵ 操作②为什么不能改为加硝酸钡溶液 。
⑶ 进行操作②后,判断SO42-已除尽的方法是 。
⑷ 用化学方程式表示操作③的目的 。
18.(14分)下表是元素周期表的一部分,回答下列有关问题:
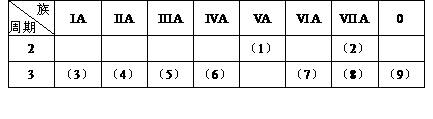
(1)写出下列元素符号:(1)________,(6)________,(7)________。
(2)在这些元素中,最活泼的金属元素是________,最活泼的非金属元素是_____,最不活泼的元素是________。(填元素符号)
(3)在这些元素的最高价氧化物对应水化物中,酸性最强的是________(填化学式,下同),碱性最强的是________,呈两性的氢氧化物是_______,氢化物稳定性最强的是________。
(4)在这些元素中,原子半径最大的是________,原子半径最小的是________。
(5)元素(8)所形成的单质的电子式________ ,
元素(4)和(8)所组成化合物中含______键。
17.某溶液中可能含有下列6种离子中的某几种: 、
、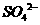 、
、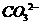 、
、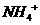 、
、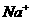 、
、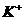 。为确认溶液组成进行如下实验:(1)200mL上述溶液,加入足量
。为确认溶液组成进行如下实验:(1)200mL上述溶液,加入足量 溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀4.30g,向沉淀中加入过量的盐酸,有2.33g沉淀不溶。(2)向(1)的滤液中加入足量的
溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀4.30g,向沉淀中加入过量的盐酸,有2.33g沉淀不溶。(2)向(1)的滤液中加入足量的 溶液,加热,产生能促使湿润红色石蕊试纸变蓝的气体1.12L(已换算成标准状况,假定产生的气体全部逸出)。由此可以得出关于原溶液组成的正确结论是
溶液,加热,产生能促使湿润红色石蕊试纸变蓝的气体1.12L(已换算成标准状况,假定产生的气体全部逸出)。由此可以得出关于原溶液组成的正确结论是
A.一定存在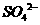 、
、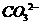 、
、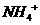 、
、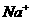
B.一定存在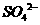 、
、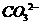 、
、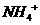 、
、
C.c(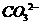 )=0.01mol·L-1,
)=0.01mol·L-1,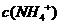 >
>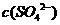
D.如果上述6种离子都存在,则c( )>
)>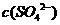
非选择题部分(共56分)
16.“绿色化学”是当今社会提出的一个新概念.在“绿色化学”工艺中,理想状态是反应中原子全部转化为欲制的产物,即原子利用率为100%。以下反应最符合绿色化学,“原子经济”要求的是
A.乙烯聚合为聚乙烯高分子材料 B.甲烷与氯气制备一氯甲烷
C.以铜和浓硝酸为原料生产硝酸铜 D.用氯气和消石灰制漂白粉
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com