
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
19ЃЎ(10Зж)гУ18mol/L ХЈСђЫсХфжЦ100 ml 3.0mol/L ЯЁСђЫсЕФЪЕбщВНжшШчЯТЃК
Ђй МЦЫуЫљгУХЈСђЫсЕФЬхЛ§ЁЁ Ђк СПШЁвЛЖЈЬхЛ§ЕФХЈСђЫсЁЁ Ђл ЯЁЪЭЁЁ
ЁЁ Ђм зЊвЦЁЂЯДЕгЁЁ Ђн ЖЈШнЁЂвЁдШ
ЛиД№ЯТСаЮЪЬт
(1)ЫљашХЈСђЫсЕФЬхЛ§ЪЧЁЁЁЁЁЁЁЁЁЁЁЁ ЃЌСПШЁХЈСђЫсЫљгУЕФСПЭВЕФЙцИёЪЧЁЁЁЁЁЁЁЁ
(ДгЯТСажабЁгУЁЁ A. 10mlЁЁ B. 25mlЁЁ C. 50mlЁЁ D. 100ml)
(2)ЯТСаЧщПіЖдЫљХфжЦЕФЯЁСђЫсХЈЖШгаКЮгАЯьЃП(гУЦЋДѓЁЂЦЋаЁЁЂЮогАЯьЬюаД)
A. ЫљгУЕФХЈСђЫсГЄЪБМфЗХжУдкУмЗтВЛКУЕФШнЦїжаЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
B. ШнСПЦПгУеєСѓЯДЕгКѓВаСєгаЩйСПЕФЫЎЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
C. ЫљгУЙ§ЕФЩеБЁЂВЃСЇАєЮДЯДЕгЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
18ЃЎ(12Зж)ЖдгкЛьКЯЮяЕФЗжРыЛђЬсДПЃЌГЃВЩгУЕФЗНЗЈгаЃКЂйЙ§ТЫЁЂЂкеєЗЂЁЂЂлеєСѓЁЂЂмнЭШЁЁЂЂнМгШШЗжНтЁЂЂоЗжвКЕШЁЃЯТСаИїзщЛьКЭЮяЕФЗжРыЛђЬсДПгІВЩгУЪВУДЗНЗЈЃП(ЧыЬюађКХ)
(1)ЪЕбщЪвжаЕФЪЏЛвЫЎОУжУЃЌвКУцЩЯГЃаќИЁгаCaCO3ЮЂСЃЁЃПЩгУЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЕФЗНЗЈГ§ШЅCa(OH)2ШмвКжааќИЁЕФCaCO3ЮЂСЃЁЃ
(2)ЬсШЁЕтЫЎжаЕФЕтЃЌгУЁЁЁЁЁЁЁЁЁЁЁЁ ЗНЗЈЁЃ
(3)Г§ШЅЪГбЮШмвКжаЕФЫЎЃЌПЩВЩгУЁЁЁЁЁЁЁЁЁЁ ЕФЗНЗЈЁЃ
(4)ЗжРыУКгЭКЭЫЎЃЌПЩВЩгУЁЁЁЁЁЁЁЁЁЁЁЁ ЕФЗНЗЈЁЃ
(5)Г§ШЅбѕЛЏИЦжаЕФЬМЫсИЦПЩгУЁЁЁЁЁЁЁЁЁЁ ЕФЗНЗЈ
(6)гЩКЃЫЎжЦШЁеєСѓЫЎПЩгУЁЁЁЁЁЁЁЁЁЁ ЕФЗНЗЈ
17ЁЂ(4Зж)Дг1 L 1 mol/L NaOHШмвКжаШЁГі10mlЃЌдђет10 mlШмвКЕФЮяжЪЕФСПХЈЖШЮЊ______________ ЃЛ 30 mL 1 mol/L NaClШмвККЭ40 mL 0.5 mol/L CaCl2ШмвКЛьКЯжЎКѓ(ЬхЛ§ЕФБфЛЏКіТдВЛМЦ)ЃЌЛьКЯвКжаCl-ЕФЮяжЪЕФСПХЈЖШЮЊ____________ЁЃЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁ
16ЃЎ(8Зж)2molCO2ЕФжЪСПЪЧ_________ЃЛдкБъзМзДПіЯТЫљеМЕФЬхЛ§дМЮЊ__________ЃЛЫљКЌЕФЗжзгЪ§ФПдМЮЊ______________ЃЛЫљКЌбѕдзгЕФЪ§ФПдМЮЊ______________ЁЃ
15ЃЎЭЌЮТЭЌбЙЯТЃЌФГШнЦїГфТњO2жи116 gЃЌШєГфТњCO2жи122 gЃЌЯжГфТњФГЦјЬхжи114 gЃЌдђФГЦјЬхЕФЗжзгСПЮЊ(ЁЁЁЁ )A
AЃЎ28ЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎ60 ЁЁЁЁЁЁЁЁCЃЎ32ЁЁЁЁЁЁ ЁЁDЃЎ4
14ЃЎФГИідзгЕФжЪСПЮЊa gЃЌЩшNAЮЊАЂЗќМгЕТТоГЃЪ§ЕФЪ§жЕЃЌдђИУдзгЕФЯрЖддзгжЪСПЪЧЁЁ (ЁЁЁЁ )
AЃЎaNAЁЁЁЁ ЁЁЁЁBЃЎ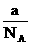 ЁЁЁЁЁЁ
CЃЎ
ЁЁЁЁЁЁ
CЃЎ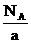 ЁЁЁЁЁЁ DЃЎ
ЁЁЁЁЁЁ DЃЎ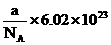
13ЃЎЯТСаШмвКжаЃЌгы100 mlЁЁ 0.5 mol/L NaClШмвКЫљКЌЕФCl-ЕФЮяжЪЕФСПХЈЖШЯрЭЌЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
AЃЎ100 ml 0.5 mol/L MgCl2 ШмвКЁЁЁЁ ЁЁЁЁ BЃЎ200 ml 0.25 mol/L HClШмвК
CЃЎ50 ml 1 mol/L NaClШмвКЁЁЁЁЁЁЁЁ DЃЎ200 ml 0.25 mol/L CaCl2ШмвК
12ЃЎФГШмвКжаПЩФмКЌгаSO42-ЁЂCO32-ЁЂCl-ЁЃЮЊСЫМьбщЦфжаЪЧЗёКЌгаSO42-ЃЌГ§BaCl2ШмвКЭтЃЌЛЙашвЊЕФШмвКЪЧ(ЁЁЁЁ )
AЃЎH2SO4ЁЁ ЁЁBЃЎHClЁЁ ЁЁЁЁЁЁCЃЎNaOHЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎNaNO3ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ Ип&ПМ%зЪ(дД#Эј
11ЃЎНЋ40ПЫNaOHШмгкЫЎжаЃЌХфжЦГЩ1LШмвКЃЌдђИУШмвКЕФЮяжЪЕФСПХЈЖШЮЊ(ЁЁЁЁ )
AЃЎ0.1mol/LЁЁЁЁ ЁЁЁЁBЃЎ0.5mol/LЁЁЁЁЁЁ CЃЎ 4mol/LЁЁЁЁЁЁ DЃЎ 1mol/L
10ЃЎШнСПЦПЩЯУЛгаБъМЧЕФЪЧ (ЁЁЁЁ )
AЃЎБъЯпЁЁЁЁЁЁ BЃЎЮТЖШЁЁЁЁ CЃЎЮяжЪЕФСПХЈЖШЁЁЁЁЁЁ DЃЎШнСП
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com