
题目列表(包括答案和解析)
3.下列关于常见有机物的说法不正确的是
A.石油和天然气的主要成分都是碳氢化合物
B.糖类和蛋白质都是人体重要的营养物质
C.乙酸和油脂都能与氢氧化钠溶液反应
D.乙烯和苯都能与溴水反应
2.下列各项中表达正确的是--
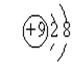 A.氟原子的结构示意图
B.丙烯的结构式 CH3-CH=CH2
A.氟原子的结构示意图
B.丙烯的结构式 CH3-CH=CH2
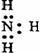
C.乙烷的结构简式 CH3CH3 D.NH3的电子式
1.19世纪中叶,门捷列夫的突出贡献是
A.提出了原子学说 B.发现了元素周期律
C.提出了分子学说 D.发现质量守恒定律
21.(6分)
铝粉和氧化铁粉末的混合物制成的铝热剂可用于焊接钢轨。现取不同质量的该铝热剂分别和100ml同物质的量浓度的NaOH溶液反应,所取铝热剂的质量与产生气体的体积关系如下表(气体体积均在标准状况下测定):
|
|
① |
② |
③ |
④ |
|
铝热剂质量/g |
5g |
10g |
15g |
20g |
|
气体体积/L |
2.24L |
4.48L |
6.72L |
6.72L |
试完成下列计算:
(1)NaOH溶液的物质的量浓度 。
(2)该铝热剂中铝的质量分数 。
(3)20g该铝热剂发生铝热反应理论上产生铁的质量是多少?(写出步骤)
2009-2010学年(下)福建省古田五中高一期末试卷
20.(14分)
有如下转化关系:
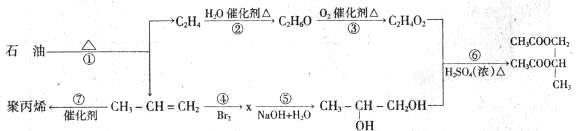
回答下列问题:
(1)实现第①步转化的方法: 。
(2)(用序号填空)属加聚反应的为 ;属取代反应的为 。
(3)写出x的结构简式: ;x的同分异构体共有 种。
(4)写出②、⑥反应的化学方程式:
②:
⑥:
19.(6分)
“酒是陈的香”就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室和工业上常采用如下反应: 来制取乙酸乙酯。
来制取乙酸乙酯。
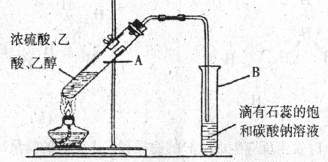
(1)实验时,试管B观察到的现象是界面处产生浅红色,下层为蓝色,振荡后产生气泡,界面处浅红色消失,原因是(用化学方程式表示) 。 欲从上述混合物中分离出乙酸乙酯,采用的分离方法是 (填操作名称)。
(2)事实证明,此反应以浓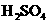 为催化剂,也存在缺陷,其原因可能是
。
为催化剂,也存在缺陷,其原因可能是
。
a.浓H2SO4易挥发,以至不能重复使用 b.会使部分原料炭化
c.浓H2SO4有吸水性 d.会造成环境污染
18.(10分)下表中五个小实验,每个小实验有一项未填写,试按要求填空:
|
序号 |
要完成的实验 |
选用的试剂 |
原理(用化学方程式表示)或方法 |
|
(1) |
由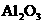 冶炼 冶炼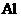 |
加冰晶石 |
|
|
(2) |
由煤制取粗苯 |
 |
|
|
(3) |
从溴水中提取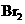 |
|
萃取分液 |
|
(4) |
从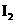 和 和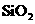 混合物中提取 混合物中提取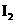 (固) (固) |
 |
|
|
(5) |
从海水中提取食盐 |
 |
|
17.(16分)
下表是元素周期表中短周期部分,表中所列字母分别代表一种元素,试回答有关问题。
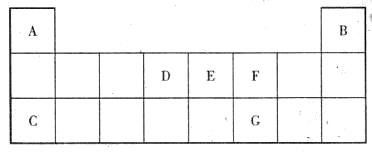
(1)只由A、D、F三种元素组成的可为人体提供能量的营养物质是 (填其中一种物质的名称)
(2)A和D可形成一种最简单化合物,它的分子构型为: 。这种化合物含
键。(填“极性”或“非极性”)
(3)由上表元素中的两个原子形成的阴离子的电子式为 。
(4)NH3·H2O的电离方程式为: ,据此电离方程式推断NH3溶于水后的合理结构是: (填序号)

(5)下图是A2与F2发生反应生成A2F的途径和三个状态的能量(E)
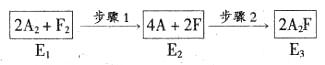
则:①步骤l是 (填“吸热”或“放热”,下同)过程,步骤2是 过程。
②比较E1、E2、E3的大小 。(由大到小顺序排列)
16.在KIO3、KHSO3的酸性混合溶液中,加入少量KI和淀粉,不停地搅拌,有下列反应发生:①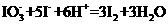 ②
② 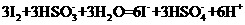 ,总反应为:
,总反应为: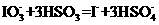 ;当反应进行到15min时,溶液突然变为蓝色,随之又很快消失,这一反应称为时钟反应,有人用它来解释生物钟现象。下列有关说法错误的是:
;当反应进行到15min时,溶液突然变为蓝色,随之又很快消失,这一反应称为时钟反应,有人用它来解释生物钟现象。下列有关说法错误的是:
A.在整个时钟反应过程中,起催化作用的物质是KI
B.上述两个反应中,反应速率较快的是②
C.时钟反应的快慢由反应②决定
D.“溶液突然变为蓝色,随之又很快消失”,这一现象与①②的反应速率有关
第II卷(非选择题,共52分)
15.室温下,一种气态烷烃和一种气态烯烃的混合物9克,其密度是相同条件下H2密度的11.25倍。当混合物通过足量的溴水时,溴水增重4.2克,则这两种气态烃是:
A.C2H6和C2H4 B.CH4和C3H6 C.CH4和C2H4 D.CH4和C4H8
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com