
ΧβΡΩΝ–±μ(Αϋά®¥πΑΗΚΆΫβΈω)
7Θ°X‘ΣΥΊΒΡ“θάκΉ”Θ§Y‘ΣΥΊΒΡ“θάκΉ”ΚΆZ‘ΣΥΊΒΡ―τάκΉ”ΨΏ”–œύΆ§ΒΡΒγΉ”≤ψΫαΙΙΘ§“―÷ΣXΒΡ‘≠Ή”–ρ ΐ±»YΒΡ¥σΘ§‘ρXΓΔYΓΔZΒΡ»ΐ÷÷άκΉ”ΑκΨΕΒΡ¥σ–ΓΥ≥–ρ «(Ζ÷±π”Οr1ΓΔr2ΓΔr3±μ Ψ)(ΓΓ )
AΘ°r1 > r2 > r3ΓΓΓΓΓΓΓΓΓΓΓΓ BΘ°r2> r1> r3ΓΓ ΓΓΓΓΓΓΓΓCΘ°r3 > r1 > r2ΓΓΓΓΓΓΓΓΓΓΓΓΓΓ DΘ°r3 > r2 > r1
6Θ°Ε‘”Ύ»ΈΚΈ“ΜΗωΤΫΚβΧεœΒΘ§≤…”Ο“‘œ¬¥κ ©Θ§“ΜΕ®Μα ΙΤΫΚβ“ΤΕ·ΒΡ «(ΓΓΓΓ )ΓΓΓΓΓΓΓΓ
ΓΓΓΓΓΓ AΘ°Φ”»κ“Μ÷÷Ζ¥”ΠΈοΓΓ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ BΘ°…ΐΗΏΈ¬Ε»
ΓΓΓΓΓΓ CΘ°Ε‘ΤΫΚβΧεœΒ‘ωΦ”―Ι«ΩΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ DΘ° Ι”Ο¥ΏΜ·ΦΝ
5Θ°œ¬Ν–ΥΒΖ®÷–¥μΈσΒΡ «(ΓΓ )
AΘ°Ζ≤ «Ζ≈»»Ζ¥”ΠΚΆλΊ‘ωΦ”ΒΡΖ¥”ΠΘ§ΨΆΗϋ“ΉΉ‘ΖΔΫχ––
BΘ°Ε‘”ΎΆ§“ΜΈο÷ ‘Ύ≤ΜΆ§Ή¥Χ§ ±ΒΡλΊ÷Β «ΘΚΤχΧ§>“ΚΧ§>ΙΧΧ§
CΘ°ΤΫΚβ≥Θ ΐK÷Β‘Ϋ¥σΘ§‘ρΩ…ΡφΖ¥”ΠΫχ––‘ΫΆξ»ΪΘ§Ζ¥”ΠΈοΒΡΉΣΜ·¬ “≤‘Ϋ¥σ
DΘ°Ζ≤ «ΡήΝΩ¥οΒΫΜνΜ·ΡήΒΡΖ÷Ή”ΖΔ…ζΒΡ≈ωΉ≤ΨυΈΣ”––ß≈ωΉ≤
4Θ°ΫΪpH ‘÷Ϋ”Ο’τΝσΥ° Σ»σΚσΘ§»Ξ≤βΕ®Ρ≥»ή“ΚΒΡpH÷ΒΘ§≤βΒΟΗΟ»ή“ΚΒΡpH÷ΒΫαΙϊΫΪΜαΘΚ
AΘ°ΤΪΗΏΓΓΓΓ ΓΓBΘ°ΤΪΒΆΓΓΓΓ ΓΓCΘ°≤Μ±δΓΓ ΓΓ DΘ°…œ ω»ΐ÷÷«ιΩωΨυ”–Ω…Ρή
3Θ°‘Ύ‘≠Βγ≥ΊΚΆΒγΫβ≥ΊΒΡΒγΦΪ…œΥυΖΔ…ζΒΡΖ¥”ΠΘ§ τ”Ύ―θΜ·Ζ¥”ΠΒΡ «(ΓΓΓΓ )
AΘ°‘≠Βγ≥ΊΒΡ’ΐΦΪΚΆΒγΫβ≥ΊΒΡ―τΦΪΥυΖΔ…ζΒΡΖ¥”Π
BΘ°‘≠Βγ≥ΊΒΡ’ΐΦΪΚΆΒγΫβ≥ΊΒΡ“θΦΪΥυΖΔ…ζΒΡΖ¥”Π
CΘ°‘≠Βγ≥ΊΒΡΗΚΦΪΚΆΒγΫβ≥ΊΒΡ―τΦΪΥυΖΔ…ζΒΡΖ¥”Π
DΘ°‘≠Βγ≥ΊΒΡΗΚΦΪΚΆΒγΫβ≥ΊΒΡ“θΦΪΥυΖΔ…ζΒΡΖ¥”Π
2Θ° ‘Ύ“ΜΕ®ΒΡΈ¬Ε»œ¬, ΫΪ 2mol SO2ΚΆ1mol
O2≥δ»κ“ΜΕ®»ίΜΐΟή±’»ίΤς÷–, ‘Ύ¥ΏΜ·ΦΝ¥φ‘Ύœ¬Ϋχ––œ¬Ν–Ζ¥”Π: 2SO2(g) + O2(g)ΓΓΓΓ 2SO3(g) ΓςH=-197
kJ/mol, Β±¥οΒΫΤΫΚβΉ¥Χ§ ±, œ¬Ν–ΥΒΖ®÷–’ΐ»ΖΒΡ «(ΓΓΓΓ )
‘Ύ“ΜΕ®ΒΡΈ¬Ε»œ¬, ΫΪ 2mol SO2ΚΆ1mol
O2≥δ»κ“ΜΕ®»ίΜΐΟή±’»ίΤς÷–, ‘Ύ¥ΏΜ·ΦΝ¥φ‘Ύœ¬Ϋχ––œ¬Ν–Ζ¥”Π: 2SO2(g) + O2(g)ΓΓΓΓ 2SO3(g) ΓςH=-197
kJ/mol, Β±¥οΒΫΤΫΚβΉ¥Χ§ ±, œ¬Ν–ΥΒΖ®÷–’ΐ»ΖΒΡ «(ΓΓΓΓ )
AΘ°…ζ≥… SO3 2 molΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ BΘ°Ζ≈≥ω 197 kJ ΒΡ»»ΝΩ
CΘ°Έϋ ’197 kJ ΒΡ»»ΝΩΓΓΓΓΓΓΓΓΓΓΓΓ DΘ° SO2 ΚΆ SO3 Ι≤”– 2 mol
1Θ°œ÷ΫΉΕΈΈ“ΙζΒΡΡή‘¥ΫαΙΙ»‘“‘Μ· ·Ρή‘¥ΈΣ÷ςΘ§ΈΣΦθ…ΌΜ· ·Ρή‘¥œϊΚΡΓΔ Βœ÷Ω…≥÷–χΖΔ’ΙΘ§Έ“ΙζΧα≥ωΝΥΓΑΙΙΫ®ΫΎ‘Φ–Ά…γΜαΓ±ΒΡΩΎΚ≈ΓΘœ¬Ν–ΫΎ‘ΦΜ· ·Ρή‘¥ΒΡ¥κ ©≤Μ«– ΒΦ ΒΡ «(ΓΓΓΓ )
AΘ°¥σΝΠΩΣΖΔ«βΡή‘¥ΓΓ ΓΓΓΓBΘ°≥δΖ÷άϊ”ΟΧΪ―τΡήΓΓ
CΘ°≤Μ Ι”ΟΚ§ΧΦΒΡΡή‘¥ΓΓΓΓ DΘ°ΧαΗΏΡή‘¥άϊ”Ο¬
20Θ°Ρ≥ΤχΧ§ΆιΧΰΚΆ““œ©Β»ΧεΜΐΜλΚœ ±Θ§1ΧεΜΐΜλΚœΤχΧεΆξ»Ϊ»Φ…’œϊΚΡΆ§Έ¬Ά§―Ι
œ¬4.75ΧεΜΐ―θΤχΓΘ ‘ΜΊ¥πΘΚ
(1)ΗΟΆιΧΰΒΡΖ÷Ή” ΫΈΣΓΓΓΓΓΓΓΓΓΓΓΓ ΘΜ
ΓΓ (2)ΗΟΆιΧΰΥυ”–Ά§Ζ÷“λΙΙΧεΒΡΫαΙΙΦρ ΫΈΣΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ

19Θ°Ρ≥ΩΈΆβ–ΓΉι…ηΦΤΒΡ Β―ι “÷Τ»Γ““Υα““θΞΒΡΉΑ÷Ο(»γΆΦΥυ Ψ)Θ§A÷–Ζ≈”–≈®ΝρΥαΘ§B÷–Ζ≈”–““¥ΦΓΔΈόΥ°¥ΉΥαΘ§D÷–Ζ≈”–±ΞΚΆΧΦΥαΡΤ»ή“ΚΓΘΑ¥ΆΦΝ§Ϋ”ΉΑ÷ΟΘ§”ΟΨΤΨΪΒΤΕ‘…’ΤΩBΦ”»»Θ§Β±Ιέ≤λΒΫD÷–”–Οςœ‘œ÷œσ ±ΆΘ÷Ι Β―ιΓΘ ‘Άξ≥…œ¬Ν–Έ ΧβΘΚ
(1)‘Ύ…’ΤΩ÷–≥ΐΝΥΦ”»κ““¥ΦΓΔ≈®ΝρΥαΚΆ““ΥαΆβΘ§ΜΙ”ΠΖ≈»κΦΗΩιΥι¥…Τ§Θ§ΤδΡΩΒΡ «ΘΚ_________ΓΘ
ΓΓ(2)«ρ–ΈΗ…‘οΙή≥ΐΤπάδΡΐΉς”ΟΆβΘ§Νμ“Μ÷Ί“ΣΉς”Ο «_________________ΓΘ
(3)ΉΑ÷ΟD÷–±ΞΚΆΧΦΥαΡΤ»ή“ΚΒΡΉς”Ο «___________________________
(4)‘ΎΗΟ Β―ι÷–Θ§»τ”Ο1mol““¥ΦΚΆ1mol ““Υα‘Ύ≈®ΝρΥαΉς”Οœ¬Φ”»»Θ§≥δΓΓΓΓΓΓΓΓΓΓΓΓ Ζ÷Ζ¥”ΠΘ§ΡήΖώ…ζ≥…1mol““Υα““θΞΘΩΓΓΓΓ Θ§‘≠“ρ «ΘΚΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
18Θ°“―÷Σ““œ©ΡήΖΔ…ζ“‘œ¬ΉΣΜ·ΘΚ
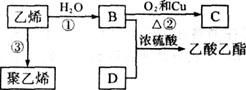
(1)““œ©ΒΡΫαΙΙ ΫΈΣΘΚ_________________________ΓΘ
(2)–¥≥ωœ¬Ν–Μ·ΚœΈοΙΌΡήΆ≈ΒΡΟϊ≥ΤΘΚ
B÷–Κ§ΙΌΡήΆ≈Οϊ≥Τ___________ΘΜD÷–Κ§ΙΌΡήΆ≈Οϊ≥Τ____________ΓΘ
(3)–¥≥ωΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΦΑΖ¥”Πάύ–ΆΘΚ
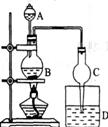 ΓΓΔΌ______________________________________________ΘΜΖ¥”Πάύ–ΆΘΚ________ΓΘ
ΓΓΔΌ______________________________________________ΘΜΖ¥”Πάύ–ΆΘΚ________ΓΘ
ΓΓΔΎ______________________________________________ΓΘ
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com