
题目列表(包括答案和解析)
7.已知:H2(g)+F2(g) = 2HF(g);ΔH═-270kJ·mol-1 ,下列说法正确的是( )
A.2L氟化氢气体分解成1L的氢气和1L的氟气吸收270kJ热量
B.1mol氢气与1mol氟气反应生成2mol液态氟化氢放出的热量小于270kJ
C.在相同条件下,1mol氢气与1mol氟气的能量总和大于2mol氟化氢气体的能量
D.1个氢气分子与1个氟气分子反应生成2个氟化氢分子放出270kJ热量
6.反应:CaCl2+CO2+H2O =CaCO3↓+2HCl在任何情况下都不能发生反应,原因是该反应( )
A.△H > 0 △S > 0 B.△H < 0 △S < 0
C.△H < 0 △S > 0 D.△H > 0 △S < 0
5.X、Y、Z三种气体,取X和Y按1∶1的物质的量之比混合,放入密闭容器中发生如下反应:X+2Y 2Z ,达到平衡后,测得混合气体中反应物的总物质的量与生成物的总物质的量之比为3∶2 ,则Y的转化率最接近于( )
2Z ,达到平衡后,测得混合气体中反应物的总物质的量与生成物的总物质的量之比为3∶2 ,则Y的转化率最接近于( )
A.33% B.40% C.50% D.65%
4.已知:①1molH2分子中化学键断裂时需要吸收436kJ的能量
②1molCl2分子中化学键断裂时需要吸收243kJ的能量
③由H原子和Cl原子形成1molHCl分子时释放431kJ的能量
下列叙述正确的是( )
A.氢气和氯气反应生成氯化氢气体的热化学方程式是H2(g)+Cl(g)=2HCl(g)
B.氢气与氯气反应生成2mol氯化氢气体,反应的△H=183kJ/mol
C.氢气与氯气反应生成2mol氯化氢气体,反应的△H=-183kJ/mol
D.氢气与氯气反应生成1mol氯化氢气体,反应的△H=-183kJ/mol
3.铅蓄电池总反应为PbO2 + Pb + 2H2SO4 ═ 2PbSO4 + 2H2O ,下列关于铅蓄电池的说法正确的是( )
A.在放电时,正极发生的反应是 Pb(s) +SO42―(aq)→ PbSO4(s) +2e―
B.在放电时,该电池的负极材料是铅板
C.在充电时,电池中硫酸的浓度不断变小
D.在充电时,阳极发生的反应是 PbSO4(s)+2e―→ Pb(s)+ SO42―(aq)
2.对于反应2SO2(g)+O2(g) 2SO3(g),能增大正反应速率的措施是( )
2SO3(g),能增大正反应速率的措施是( )
A.降低体系温度 B.增大容器容积
C.移去部分SO3 D.增大O2 的浓度
1.下列有关金属腐蚀与防护的说法正确的是( )
A.纯银器表面在空气中因电化学腐蚀渐渐变暗
B.当镀锡铁制品的镀层破损时,镀层仍能对铁制品起保护作用
C.在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法
D.可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀
31、一种无色液态有机物具有下列性质:①能与钠反应生成氢气;②与碳酸钠不发生反应;③其蒸气对氢气的相对密度为37。
(1) 推断该物质属于哪一类有机化合物;
(2) 计算该有机物的相对分子质量、分子式;
(3) 写出该有机物可能有的同分异构体的结构式。
30、完全燃烧0.1mol某烃,生成5.4gH2O和13.44LCO2(标准状况),通过计算写出该烃的分子式。
29、(除(1)题每空1分外,其余每空2分,共12分)
实验室制取乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量二氧化硫,有人设计下列实验以确认上述混合气体中含有乙烯和二氧化硫。
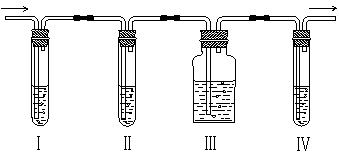
(1)Ⅰ、Ⅱ、Ⅲ、Ⅳ装置中盛放的试剂是:Ⅰ ;Ⅱ ;Ⅲ ;
Ⅳ 。(将试剂的序号填入空格内,试剂可重复使用)
A、品红溶液 B、NaOH溶液 C、浓H2SO4 D、酸性KMnO4溶液
(2)能说明二氧化硫气体存在的现象是 ;
(3)使用装置Ⅱ的目的是 ;
(4)使用装置Ⅲ的目的是
;
(5)确证含有乙烯的现象是
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com