
题目列表(包括答案和解析)
17.在密闭容器中,反应:CH4(g)+H2O(g)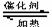 CO(g)+3H2(g) △H>0 达到平衡。下列叙述不正确的是( )
CO(g)+3H2(g) △H>0 达到平衡。下列叙述不正确的是( )
A.增加甲烷的量,上式中△H增大 B.增大水蒸气的量,可提高甲烷的转化率
C.升高温度,逆反应速率增大 D.增大体系压强,该反应的化学平衡常数不变
16.某同学按右图所示的装置进行电解实验。下列说法正确的是( )
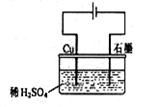 A.电解过程中,铜电极上有H2产生
A.电解过程中,铜电极上有H2产生
B.电解初期,主要反应方程式为:Cu+H2SO4 CuSO4+H2↑
CuSO4+H2↑
C.电解开始时,石墨电极上有铜析出
D.整个电解过程中,H+的浓度不断增大
15.
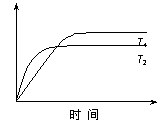 在密闭的容器中进行如下的反应:H2(g)+I2(g)
在密闭的容器中进行如下的反应:H2(g)+I2(g) 2HI(g),在温度T1和T2时,产物的量与时间的关系如下图所示,符合图象的正确的判断是( )
2HI(g),在温度T1和T2时,产物的量与时间的关系如下图所示,符合图象的正确的判断是( )
A.T1>T2,△H>0 B.T1>T2,△H<0
C.T1<T2,△H>0 D.T1<T2,△H<0
14.工业上制备纯硅反应的热化学方程式如下:
SiCl4(g)+2H2(g)
 Si(s)+4HCl(g);△H=+QkJ·mol-1(Q>0)
Si(s)+4HCl(g);△H=+QkJ·mol-1(Q>0)
某温度、压强下,将一定量的反应物通入密闭容器进行以上的反应,下列叙述正确的是( )
A.反应过程中,若增大压强能提高SiCl4的转化率
B.若反应开始时SiCl4为1mol,则达到平衡时,吸收热量为QkJ
C.反应至4min时,若HCl的浓度为0.12mol·L-1,则H2的反应速率为0.03mol/(L·min)
D.当反应吸收热量为0.025QkJ时,生成的HCl通入100mL1mol·L-1的NaOH恰好反应
13.下列有关工业生产的叙述正确的是( )
A.合成氨生产过程中将NH3液化分离,可加快正反应速率,提高N2、H2的转化率
B.合成氨工业中,使用铁催化剂可加快正反应速率,提高N2、H2的转化率
C.电解饱和食盐水制烧碱采用离子交换膜法,可防止阴极室产生的C12进入阳极室
D.电解精炼铜时,同一时间内阳极溶解铜的质量比阴极析出铜的质量小
12.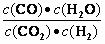 高温下,某反应达平衡,平衡常数K =
。恒容时,温度升高,H2浓度减小。下列说法正确的是( )
高温下,某反应达平衡,平衡常数K =
。恒容时,温度升高,H2浓度减小。下列说法正确的是( )
A.该反应的焓变为正值 B.恒温恒容下,增大压强,H2浓度一定减小
C.升高温度,逆反应速率减小 D.该反应化学方程式为CO+H2O  CO2+H2
CO2+H2
11. LiFePO4电池具有稳定性高、安全、对环境友好等优点,可用于电动汽车。电池反应为:
LiFePO4电池具有稳定性高、安全、对环境友好等优点,可用于电动汽车。电池反应为:
FePO4+Li LiFePO4,用含有Li+的导电固体为电解质。下列有关LiFePO4电池说法正确的是( )
A.可加入硫酸以提高电解质的导电性
B.放电时电池内部Li+ 向负极移动.
C.充电过程中,电池阳极反应Li+ + e―→ Li
D.放电时电池正极反应为:FePO4+Li++e-→LiFePO4
10.一种燃料电池中发生的化学反应为:在酸性溶液中甲醇与氧气作用生成水和二氧化碳。该电池负极发生的反应是( )
A.CH3OH + O2 → H2O + CO2 + 2H+ + 2e- B.O2 + 4H+ + 4e-→ 2H2O
C.CH3OH + H2O → CO2 + 6H+ + 6e- D.O2 + 2H2O + 4e-→ 4OH-
9.用铜片、银片、Cu (NO3)2溶液、AgNO3溶液、导线和盐桥(装有琼脂-KNO3的U型管)构成一个原电池。以下有关该原电池的叙述正确的是( )
①在外电路中,电流由铜电极流向银电极
②正极反应为:Ag++e-=Ag
③实验过程中取出盐桥,原电池仍继续工作
④将铜片浸入AgNO3溶液中发生的化学反应与该原电池反应相同
A.①② B.②③ C.②④ D.③④
8.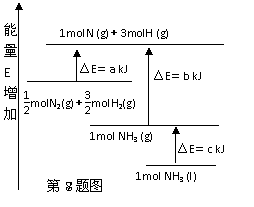 化学反应N2+3H2=2NH3的能量变化如图所示,E是正值,该反应的热化学方程式是( )
化学反应N2+3H2=2NH3的能量变化如图所示,E是正值,该反应的热化学方程式是( )
A.N2(g)+3H2(g)=2NH3(1); △H=2(a-b-c)kJ·mol-1
B. N2(g)+3H2(g)=2NH3(g); △H=2(b-a)kJ·mol-1
C.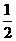 N2(g)+
N2(g)+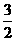 H2(g)=NH3(1); △H=(b+c-a)kJ·mol-1
H2(g)=NH3(1); △H=(b+c-a)kJ·mol-1
D.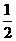 N2(g)+
N2(g)+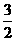 H2(g)=NH3(g); △H=(a+b)kJ·mol-1
H2(g)=NH3(g); △H=(a+b)kJ·mol-1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com