
题目列表(包括答案和解析)
25.(15分)(1)(2分)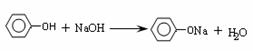
(2)(2分)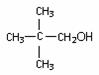
(3)(2分)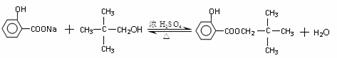
(4)(4分)缩聚反应;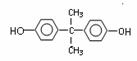
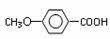
(5)(5分)C8H8O3
。
6.A 7.C 8.C 9.D 10.A 11.B 12.B
28. 为了减少煤燃烧对大气造成的污染,煤的气化和液化是高效、清洁利用煤炭的重要途径,而减少CO2气体的排放也是人类面临的重大课题。煤综合利用的一种途径如下所示:
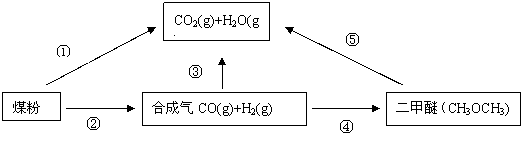
(1)用下图所示装置定量检测过程①产生的CO2(已知:煤粉燃烧过程中会产生SO2)
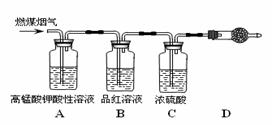
B中预期的实验现象是 ,D中的试剂是 。
(2)已知C(s)+H2O(g)=CO(g)+H2(g) ΔH1 = +131.3 kJ·mol-1
C(s)+2H2O(g)=CO2(g)+2H2(g) ΔH2 = +90 kJ·mol-1
则一氧化碳与水蒸气反应生成二氧化碳和氢气的热化学方程式是 ,该反应的化学平衡常数K随温度的升高将 (填“增大”、“减小”或“不变”)。
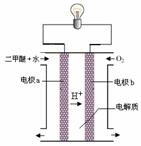
(3)用图装置可以完成⑤的转化,同时提高能量的利用率。其实现的能量转化形式主要是 ,a的电极反应式是 。
(4)燃煤烟气中的CO2可用稀氨水捕获和吸收,不仅可以减少CO2的排放,也可以生产化肥碳酸氢铵。假设该方法每小时处理含CO2的体积分数为11.2%的燃煤烟气1000 m3(标准状况),其中CO2的脱除效率为80%,则理论上每小时生产碳酸氢铵 kg。
2010-2011学年度东城区二模答案
27.(1) 已知Na2S2O3 + H2SO4 = Na2SO4 + S↓+ SO2 + H2O 。甲同学通过测定该反应发生时溶液变浑浊的时间,研究外界条件对化学反应速率的影响。设计实验如下(所取溶液体积均为10mL):
|
实验编号 |
实验温度/℃ |
c(Na2S2O3)/mol·L-1 |
c(H2SO4)/mol·L-1 |
|
① |
25 |
0.1 |
0.1 |
|
② |
25 |
0.1 |
0.2 |
|
③ |
50 |
0.2 |
0.1 |
|
④ |
50 |
0.1 |
0.1 |
其他条件不变时:探究浓度对化学反应速率的影响,应选择 (填实验编号);
探究温度对化学反应速率的影响,应选择 (填实验编号)。
(2)已知Na2S2O3溶液与Cl2反应时, 1mol Na2S2O3转移8 mol电子。该反应的离子方程式是 。
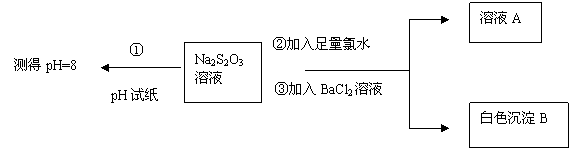 甲同学设计如下实验流程探究Na2S2O3的化学性质。
甲同学设计如下实验流程探究Na2S2O3的化学性质。

(Ⅰ)甲同学设计实验流程的目的是证明Na2S2O3溶液具有碱性和 性。
(Ⅱ)生成白色沉淀B的离子方程式是 。
(Ⅲ)乙同学认为应将上述流程中②③所加试剂顺序颠倒,你认为甲、乙两同学的设计更合理的是 (填“甲”或“乙”),理由是 。
26.X、Y、Z、M、R、Q是短周期主族元素,部分信息如下表所示:
|
|
X |
Y |
Z |
M |
R |
Q |
|
原子半径/nm |
|
|
0.186 |
0.074 |
0.099 |
0.143 |
|
主要化合价 |
|
-4,+4 |
|
-2 |
-1,+7 |
+3 |
|
其它 |
阳离子核外无电子 |
无机非金属材料的主角 |
焰色反应呈黄色 |
|
|
|
(1)R在元素周期表中的位置是 ;R在自然界中有质量数为35和37的两种核素,它们之间的关系互为 。
(2)Z的单质与水反应的化学方程式是 。
(3)Y与R相比,非金属性较强的是 (用元素符号表示),下列事实能证明这一结论的是 (选填字母序号)。
a. 常温下Y的单质呈固态,R的单质呈气态
b. 稳定性XR >YX4
c. Y与R形成的化合物中Y呈正价
(4)根据表中数据推测,Y的原子半径的最小范围是 。
(5)甲、乙是上述部分元素的最高价氧化物的水化物,且甲 + 乙→丙 + 水 。若丙的水溶液呈碱性,则丙的化学式是 。
25. 苯酚是一种重要的化工原料。以苯酚为主要起始原料,经下列反应可制得香料M和高分子化合物N。(部分产物及反应条件已略去)
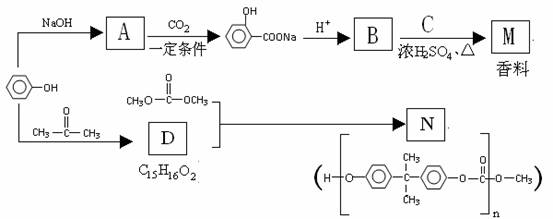
(1)由苯酚生成A的化学方程式是 。
(2)已知C的分子式为C5H12O,C能与金属Na反应,C的一氯代物有2种。C的结构简式是 。
(3)B与C反应的化学方程式是 。
(4)生成N的反应类型是 ,D的结构简式是 。
(5)以苯酚为基础原料也可以合成防腐剂F。经质谱分析F的相对分子质量为152,其中氧元素的质量分数为31%,F完全燃烧只生成CO2和H2O。则F的分子式是 。
已知:
①芳香族化合物F能与NaHCO3溶液反应,且不能发生水解反应;
②F的核磁共振氢谱显示其分子中含有4种氢原子;
③分子结构中不存在“-O-O- ”的连接方式。
F的结构简式是 。
12.下列溶液中各微粒的浓度关系正确的是
A.0.1 mol·L-1 Na2S溶液中:2c(Na+)=c(S2-)+c(HS-)+c(H2S)
B.0.1 mol·L-1 pH=9的NaNO2溶液中: c(Na+)>c(NO2-)>c(OH-) >c(H+)
C.等pH的氨水、NaOH溶液、Ba(OH)2溶液中: c(NH4+)=c(Na+)=c(Ba2+)
D.向NH4HCO3溶液中滴加NaOH溶液至pH=7:c(NH4+)+c(Na+)= c(HCO3-)+c(CO32-)
11.有X、Y、Z三种物质。常温下分别用Y或Z与X混合时,反应速率几乎相同的是
|
选项 |
X |
Y |
Z |
|
A |
2mL 5%H2O2
溶液 |
1mL 1 mol·L-1CuSO4溶液 |
1mL 1
mol·L-1FeCl3溶液 |
|
B |
1mL 1
mol·L-1 NaHCO3溶液 |
1 mL 1 mol·L-1 HCl溶液 |
1mL 0.5 mol·L-1 H2SO4溶液 |
|
C |
钠块 |
10 mL 乙醇 |
10 mL 水 |
|
D |
经过酸洗除锈的铁钉 |
5mL 海水 |
5 mL 蒸馏水 |
10.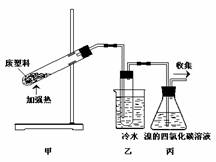 加热聚丙烯废塑料可以得到碳、氢气、甲烷、乙烯、丙烯、苯和甲苯。用图所示装置探究废旧塑料的再利用。下列叙述不正确的是
加热聚丙烯废塑料可以得到碳、氢气、甲烷、乙烯、丙烯、苯和甲苯。用图所示装置探究废旧塑料的再利用。下列叙述不正确的是
A.聚丙烯的链节是-CH2-CH2-CH2-
B.装置乙的试管中可收集到芳香烃
C.装置丙中的试剂可吸收烯烃以制取卤代烃
D.最后收集的气体可做燃料
9.下列各组物质不能按“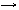 ”所示关系实现转化的是(“
”所示关系实现转化的是(“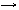 ”表示反应一步完成)
”表示反应一步完成)
A. 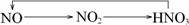 B.
B. 
C.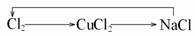 D.
D.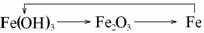
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com