
题目列表(包括答案和解析)
7、对可逆反应4NH3(g)+ 5O2(g) 4NO(g)+ 6H2O(g),下列叙述正确的是
4NO(g)+ 6H2O(g),下列叙述正确的是
A、达到化学平衡时,4υ正(O2)= 5υ逆(NO )
B、若单位时间内生成x mol NO的同时,消耗x mol NH3 ,则反应达到平衡状态
C、达到化学平稳时,若增加容器体积,则正反应速率减少,逆反应速率增大
D、化学反应速率关系是:2υ正(NH3)= 3υ正(H2O)
6、在一定温度下,向a L密闭容器中加入1mol X气体和2 mol Y气体,发生如下反应:X(g)+2Y(g)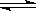 2Z(g) 此反应达到平衡的标志是
2Z(g) 此反应达到平衡的标志是
A.容器内压强不随时间而变化 B. 容器内X、Y、Z的浓度之比为1︰2︰2
C. 容器内各物质的浓度相等 D. 单位时间消耗0.1mol X同时生成0.2mol Z
5.下列说法中正确的是(NA表示阿伏加德罗常数的值)( )。
A、SiO2晶体中,1mol硅原子与氧原子形成的共价键数是2NA
B、标准状况下,1L己烷所含碳原子个数约为6NA/22.4
C、3.2g铜在硫蒸气中完全燃烧,转移的电子数为0.1NA
D、常温常压下,0.1mol氖气含有的电子数为1NA
4.在已处于化学平衡状态的体系中,如果下列量发生变化,其中一定能表明平衡移动的是
A. 反应混和物的浓度 B. 反应物的转化率
C. 正、逆反应速率 D. 反应混和物的压强
3、短周期元素M和N的离子M2+和N2-具有相同电子层结构,则下列说法正确的是
A、M2+的离子半径比N2-小 B、M的原子序数比N小
C、M和N原子的电子层数相等 D、M和N原子最外层电子数相等
2.一定量的盐酸跟过量的铁粉反应时,为了减缓反应的速率,且不影响生成H2的总量,可向反应中加入适量的
A、NaOH(s) B、CH3COONa(s) C、NH4Cl(s) D、Na2CO3(s)
1.一定条件下反应N2(g)+3H2(g) 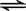 2NH3(g )在10L的密闭容器中进行,测得2min内,N2的物质的量由20mol减小到8mol,则2min内N2的反应速率为
2NH3(g )在10L的密闭容器中进行,测得2min内,N2的物质的量由20mol减小到8mol,则2min内N2的反应速率为
A.1.2mol/(L·min) B.1mol/(L·min)
C.0.6mol/(L·min) D.0.4mol/(L·min)
32.(12分)为测定已变质的过氧化钠的纯度,设计如下图所示的实验:Q为一具有良好的弹性气球,称取一定量的样品放于其中,按图安装的实验装置打开分液漏斗的活塞,将稀H2SO4滴入气球中。请填空:
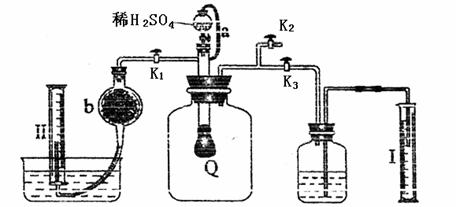
(1)Q内发生反应生成 种气体,其中的反应有 个氧化还原反应。
(2)为测定反应生成气体的总体积,滴稀H2SO4前必须关闭(填K1、K2或K3,下同)
,打开 。
(3)当上述反应停止,将K1、K2、K3处于关闭状态,然后先打开K2,再缓缓打开K1,这时可观察到的现象是 。
(4)导管a的作用是 。
(5)b中装的固体试剂是 ,为何要缓缓打开K1 。
(6)实验结束时量筒I中有x mL水,量筒II中收集到y mL气体,则过氧化钠的纯度是
(体积折算到标准状况)。(4分)
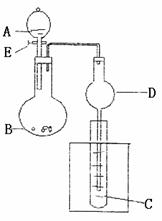
31.(16分)用右图所示装置进行实验, 将A逐滴加入B中:
(1)若A为浓硫酸, B为第3周期金属元素的片状单质,
B在常温下难与水反应; C为品红溶液,实验中观察
到溶液褪色。则B是 (填化学式),B
与浓硫酸反应的化学方程式为:
。
反应后往烧杯中加入沸水,又可观察到试管C中的现象
为: 。
(2)若B为Na2CO3,C为C6H5ONa溶液,实验中观察到小试管内溶液变浑浊,则酸A应具有的性质是 。然后往烧杯中加入沸水,可观察到试管C中的现象是 。
(3)若B是生石灰,实验中观察到C溶液先形成沉淀,然后沉淀溶解,当溶液恰好澄清时,关闭E,然后往烧杯中加入热水,静置片刻,观察到试管壁出现光亮的银镜,则A是 (填名称),C是 与葡萄糖的混合液,仪器D在此实验中的作用是 。
|
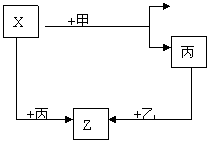
(1)若甲是具有氧化性的黄绿色气体单质,丙通常是暗红色的液体,Y和Z具有相同的阳离子,X与Z含有相同的阴离子。
①写出乙物质的化学式 ;
②写出X与过量的甲在水溶液中的离子反应过程式: 。
(2)若甲是具有还原性的金属单质,X、Y、Z中有一种是离子晶体,试推断:
①写出Y的电子式 ;
②写出X与甲反应的化学方程式,并标出电子转移的方向和数目:
30.(8分)A、B、C、D均为短周期元素。A、B可形成两种液态化合物,其最简式分别为BA和B2A。A与D可形成气态化合物DA、DA2。A、B、D可组成离子化合物,该晶体化学式为B4A3D2,其水溶液呈弱酸性。B与D可形成一种气体X,且X分子与B2A分子中的电子数相等。B与C可形成气体Y,且Y分子与最简式为BA的分子中的电子数相等。
请回答:
(1)写出元素的名称:A ,C 。
(2)完成下列反应的化学方程式。
①C2+(BA)n→A2
②C2+X(过量)→D
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com