
题目列表(包括答案和解析)
20.下列曲线图(纵坐标为沉淀的量,横坐标为加入物质的量)正确的是 ( )
A.向1L浓度均为0.1mol/L的Ba(OH)2、NaAIO2混合液加入0.1mol/L稀H2SO4
B.向含有0.1mol/L AlCl3和0.3mol/L NH4Cl的混合液1L中加入0.1mol/L NaOH溶液
C.向氢氧化钡溶液中滴加明矾溶液
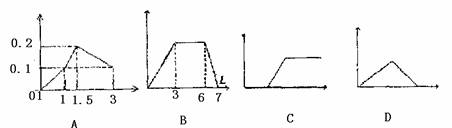 D.向AlCl3溶液滴加过量氨水
D.向AlCl3溶液滴加过量氨水
19.某干燥粉末可能由Na2O、Na2O2、Na2CO3、NaHCO、NaCI中的一种或几种组成,将该粉末与足量的盐酸反应有气体X逸出,X通过足量的NaOH溶液后体积缩小(同温同压下测定)若将原混合粉末在空气中用酒精灯加热,也有气体放出,且剩余固体质量大于原混合粉末的质量,下列判断正确的是 ( )
A.粉末中一定有Na2O、Na2O2、NaHCO3
B.粉末中一定不含有Na2CO3和NaCI
C.粉末中一定不含有Na2O和NaCI
D.无法肯定粉末里是否含有Na2O2和NaCI
18.下列离子方程式中,正确的是 ( )
 A.向氯化亚铁溶液中通入氯气Fe2++CI2 Fe3++2CI-
A.向氯化亚铁溶液中通入氯气Fe2++CI2 Fe3++2CI-
 B.二氯化铁溶液跟过量氨水反应Fe3++3NH3·H2O Fe(OH)3↓3NH+4
B.二氯化铁溶液跟过量氨水反应Fe3++3NH3·H2O Fe(OH)3↓3NH+4
 C.钠与水的反应Na+2H2O Na++2OH-+H2↑
C.钠与水的反应Na+2H2O Na++2OH-+H2↑
D.氯气通入冷水中CI2+H2O=2H++CI-+CIO-
17.在25℃时将两个不溶性电极插入一定量的硫酸钠饱和溶液中进行电解,电解一段时间后,阴阳极两极共逸出3a摩气体,同时有W克十水硫酸钠晶体析出,若温度不变,则原溶液中溶质的质量分数为 ( )
A.W/(W+54a)×100% B.71W/161(W+36a)×100%
C.W/(W+36a)×100% D.71W/161(W+54a)×100%
16.用两个质量都等于10.2克铜棒作电池插入硝酸银溶液中,接通直流电源,当阴极通入0.1摩电子时,溶液中还有大量的银离子,这时,阴阳两极的质量比为 ( )
A.21:10.2 B.10.2:21 C.3:1 D.1:3
15.向一定量的Fe、FeO和Fe2O3的混合物中加入120mL 4mol/L的稀硝酸,恰好使混合物完全溶解,放出1.344L NO(标准状况),往所得溶液中加入KSCN溶液,无血红色出现。若用足量的氢气在加热下还原相同质量的混合物,能得到铁的物质的量为
( )
A.0.24mol B.0.21mol C.0.16mol D.0.14mol
14.将x、y、z、w四块金属分别用导线两两相连浸入稀硫酸中组成原电池。x、y相连时,x为负极;z、w相连时,电流由w→z;z、x相连时,z极上产生大量气泡;w、y相连时,w极发生氧化反应。据此判断四种金属的活动顺序是 ( )
A.x>z>w>y B.z>x>y>w C.x>y>z>w D.y>w>z>x
13.下列各组物质,可用一种试剂加以区别的是 ( )
①四种黑色固体:FeO、Fe、CuCO、C
②四种白色粉末:(NH4)2SO4、NH4CI、Na2SO4、NaCI
③四种无色溶液:乙醛、乙酸、甲酸、乙醇
④四种有机物:苯、四氯化碳、乙烯、无水乙醇
A.只有①② B.只有③④ C.只有①②④ D.全部
12.下列各组离子能在溶液中大量共存的是 ( )
A.Fe3-、Cu2+、NO3-、S2- B.Fe2+、H+、CI-、NO3-
C.Fe3-、K+、CI-、I- D.Fe2+、Fe3+、Cu2+、CI-
11.下列叙述中不正确的是 ( )
A.原电池负极上下发生的反应是氧化反应
B.失电子能力弱的物质获得电子的能力一定强
C.阳离子在氧化还原反应中,可能表现氧化性,也可能表现还原性
D.氯气分子在反应中,作氧化剂的同时也可能是还原剂
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com