
题目列表(包括答案和解析)
4.含氧酸
① 同周期非金属元素最高价含氧酸从左到右酸性增强
② 氧化性:同种元素低价强于高价含氧酸
如: HClO>HClO3>HClO4(稀)
H2SO3>H2SO4(稀)
HNO2>HNO3(稀)
3.卤化物:易水解
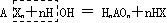
如 PCl3+3H2O=H3PO3+3HCl
SiCl4+3H2O=H2SiO3+4HCl
BCl3+3H2O=H3BO3+3HCl
BrF5+3H2O=HBrO3+5HF
利用此法可制得氢卤酸和含氧酸
2.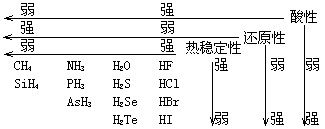 氢物
氢物
4.化学活性及反应
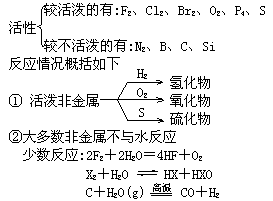
③非金属一般为成酸元素,难以与稀酸反应.
固体非金属能被氧化性酸氧化.
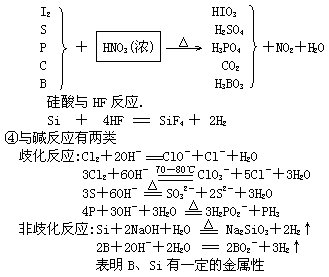
3.导电性
非金属一般属于非导体,金属是良导体,而锗、硅、砷、硒等属于半导体.但半导体与导体不同之一是导电率随温度升高而增大.
2.熔沸点与聚集态
它们可以分为三类:
①小分子物质.如:H2、O2、N2、Cl2等,通常为气体,固体为分子晶体.
②多原子分子物质.如P4、S8、As等,通常为液态或固态.均为分子晶体,但熔、沸点因范德华力较大而比①高,Br2、I2也属此类,一般易挥发或升华.
③原子晶体类单质,如金刚石、晶体硅和硼等,是非金属单质中高熔点“三角区”,通常为难挥发的固体.
1.单质:
(1)结构:除稀有气体外,非金属原子间以共价键结合.非金属单质的成键有明显的规律性.若它处在第N族,每个原子可提供8-N个价电子去和8-N个同种原子形成8-N个共价单键,可简称8-N规则;(H遵循2-N规则).如ⅦA族单质:x-x;H的共价数为1,H-H,第ⅥA族的S,Se、Te共价单键数为8-6=2,第ⅤA族的P、As共价单键数8-5=3.但第二周期的非金属单质中N2、O2形成多键.
(1) 除H外,非金属元素均在“阶梯线”的右上方
(2) 非金属元素(包括稀有元素)均在主族(零族)
(3) 最外层电子数一般≥4(H.B除外)
(4) 原子半径比同周期金属半径小.(稀有元素除外)
5.元素化合物知识网络化
元素化合物的知识在中学化学教材中占有较重的比例,内容繁多锁碎,要尽可能以最佳的方法或方式来总结成网络图,主线明确、脉络清晰.
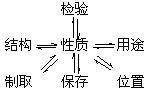
4.理清下列关系.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com