
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
11.(11Зж)ЁЁ
(1)ВЮМћНЬВФ
(2)B.ЪЧАВШЋзАжУЃЌПЩЕїНкЬхЯЕбЙЧПЃЛЁЁ D.ЪЧРфШДзАжУ?
(3)C.ЮќЪеввЯЉжаЛьгаЕФSO2ЁЂCO2ЃЛЁЁ D.ЮќЪевнГіЕФфхеєЦјЃЌЗРжЙЮлШОПеЦј
(4)ввДМЭбЫЎжЦввЯЉЃЌввЯЉгыфхМгГЩ(ЗНГЬЪНТд)
1ЁЂCЁЁ 2ЁЂAЁЁ 3ЁЂCЁЁ 4ЁЂBЁЁ 5ЁЂCЁЁ 6ЁЂADЁЁ 7ЁЂCЁЁ 8ЁЂDЁЁ 9ЁЂADЁЁ 10ЁЂBDЁЁЁЁ
15.CuЁЂCu2OКЭCuOзщГЩЕФЛьКЯЮяЃЌМгШы100mL0.6mol∙L-1HNO3ШмвКЧЁКУЪЙЛьКЯЮяШмНтЃЌЭЌЪБЪеМЏЕН224mLNOЦјЬх(БъзМзДПі)ЁЃЧѓЃК
ЂХаДГіCu2OИњЯЁЯѕЫсЗДгІЕФЛЏбЇЗДгІЗНГЬЪН___________________________ЁЃ
ЂЦВњЮяжаЯѕЫсЭЕФЮяжЪЕФСП___________molЁЃ
ЂЧШчЛьКЯЮяжаКЌ0.01moLCuЃЌдђЦфжаCu2OЁЂCuOЕФЮяжЪЕФСПЗжБ№ЪЧ________molЁЂ
__________molЁЃ
ЂШШчЛьКЯЮяжаCuЕФЮяжЪЕФСПЮЊXЃЌЧѓЦфжаCu2OЁЂCuOЕФЮяжЪЕФСПМАXЕФШЁжЕЗЖЮЇ________________ЁЂ________________ЁЂ______________ЁЃ
ИпПМЛЏбЇГхДЬбЕСЗ(1)
14ЃЎ(1)дкФГЬьШЛВњЮяжаЕУЕНвЛжжгаЛњЮяЗжзгXЃЌЗжзгЪНЮЊC10H14ЃЌОЫсадИпУЬЫсМибѕЛЏКѓЕУЕНгаЛњЮяAКЭBЃЌAОИпЕтЫсбѕЛЏКѓЕУЕНЗжзгЪНЮЊC2H4O2ЕФЫсКЭCO2ЁЃЖјBЪЧЖўдЊєШЫсЃЌПЩгЩЛЗЮьЖўЯЉКЭввЯЉОЫЋЯЉМгГЩЕФВњЮягУЫсадИпУЬЫсМибѕЛЏЕУЕНЁЃЧыИјГіЛЏКЯЮяAЁЂBКЭXЕФНсЙЙМђЪН(ПЩгУМќЯпЪНБэЪО)ЁЃ
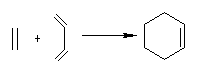 ЬсЪОЃКЂйЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
Ђк
ЬсЪОЃКЂйЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
Ђк
 ЁЁ
ЁЁ
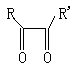
ЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁ+HIO4+H2OЁњRCOOH+RЁЏCOOH+HIO3
AЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁBЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁXЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
(2)AЁЂBЁЂCЁЂDЫФжжЬўЃЌФІЖћжЪСПжЎБШЪЧ1:2:3:4ЃЌЧвЫќУЧЕФЪЕбщЪНЖМЪЧC7H5ЃЌЖМжЛга3 жжвЛЯѕЛљШЁДњЮяЁЃ
аДГіAЁЂBЁЂCЁЂDЕФНсЙЙМђЪН(ИїаДвЛР§)ЃЛ
ЁЁЁЁЁЁЁЁЁЁЁЁ ЁЂЁЁЁЁЁЁЁЁЁЁЁЁ ЁЂЁЁЁЁЁЁЁЁЁЁЁЁ ЁЂЁЁЁЁЁЁЁЁЁЁЁЁ
13ЃЎюбБЛгўЮЊЁАЬЋПеН№ЪєЁБЁЂЁАЮДРДИжЬњЁБЃЌдвђЪЧЫќЕФЧПЖШДѓЃЌУмЖШаЁЃЌПЙИЏадФмКУЁЃ
(1)ЪвЮТЯТЃЌЫќВЛгыЫЎЁЂЯЁбЮЫсЁЂЯЁH2SO4ЁЂЯЁHNO3зїгУЃЌЕЋвзШмгкЧтЗњЫсЃЌЭЦВтЦфдвђЪЧЁЁЁЁЁЁЁЁЁЁ ЃК
ЁЁЁЁ A.ЧтЗњЫсЕФЫсадБШЦфЫќЫсЧПЁЁЁЁ B. юбРызгвзгыЗњРызгаЮГЩПЩШмадФбЕчРыЮяжЪ
ЁЁЁЁ C.ЧтЗњЫсЕФЛЙдадБШЦфЫќЫсЧПЁЁ D. ЧтЗњЫсЕФбѕЛЏадБШЦфЫќЫсЧП
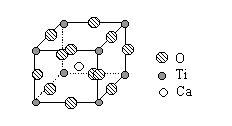
(2)юбЕФвЛжжГЌЕМЛЏКЯЮя--ИЦюбПѓОЇЬхжазюаЁжиИДЕЅдЊ(ОЇАћ)ЕФНсЙЙШчгвЭМЁЃЧыЛиД№ЃК
ЂйИУЛЏКЯЮяЕФЛЏбЇЪНЮЊЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁ ЃЛ
ЂкдкИУЛЏКЯЮяОЇЬхжаЃЌгыУПИіюбдзгОрРызюНќЧвЯрЕШЕФЦфЫќюбдзгЙВгаЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁИіЁЃ
(3)гЩюбЬњПѓ(ЦфжївЊГЩЗжжаИїдзгИіЪ§БШгы(2)жаЕФЛЏКЯЮявЛбљ)ЬсШЁюбЕФЙЄвеСїГЬБэЪОШчЯТ(ВПЗжЗДгІЬѕМўТдШЅ)ЃК
 ЁЁ
ЁЁ
ЁЁ Ђй ЗНПђжаЫљШБЮяжЪЕФЛЏбЇЪНЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛ
Ђк ЩЯЪі5ИіЗДгІжаЪєгкбѕЛЏЛЙдЗДгІЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЬюађКХ)ЃЛаДГіЦфжавЛИіЕФЛЏбЇЗДгІЗНГЬЪНЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛ
Ђл ЁЁTiCl4ГЃЮТЯТЮЊЮоЩЋвКЬх(ШлЕу- 23.2ЁцЃЌЗаЕу136.4Ёц)ЃЌдкГБЪЊЕФПеЦјжаКмШнвзаЮГЩбЬЮэЃЌаДГіЯргІЕФ
ЛЏбЇЗДгІЗНГЬЪНЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃЛ
TiCl4ЪЧ_______ЛЏКЯЮя(ЬюаДЃКЁАРызгЁБЛђЁАЙВМлЁБ)ЁЃ
12ЃЎШчЯТЭМЃЌвбжЊXЮЊжабЇЛЏбЇжаЕФвЛжжГЃМћЕФбЮЃЌFЮЊЕЛЦЩЋЙЬЬхЃЛMЁЂNЮЊГЃМћЕФН№ЪєЃЌNЕФзюИпМлбѕЛЏЮяЪЧФЭЛ№ВФСЯЃЌЫќЕФОЇЬхгВЖШКмДѓЃЌГЃзіЪжБэЕФжсГаЃЛHЮЊЕЅжЪЁЃЯТЭМжаВПЗжЗДгІВњЮявбТдШЅЁЃ
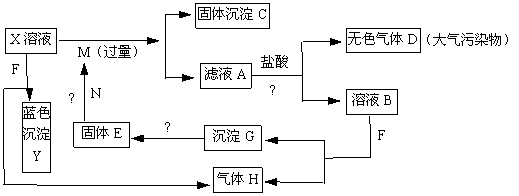
(1)XЕФЛЏбЇЪНЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛFЕФЕчзгЪНЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(2)ЗДгІЂйЕФРызгЗНГЬЪНЮЊ_______________________________________________ЁЃ
ЁЁЁЁ ЗДгІЂкЕФЛЏбЇЗНГЬЪНЮЊ_______________________________________________ЁЃ
(3)ШєЯђ100 mL ЁЁбЮXЕФШмвКжаМгШы10 gН№ЪєЕЅжЪMЕФЗлФЉЃЌГфЗжНСАшКѓЃЌЙ§ТЫЃЌКцИЩЕУ10.16gЙЬЬхCЁЃдђТЫвКAжаШмжЪЕФЮяжЪЕФСПХЈЖШЮЊ________________________ЁЃ
11.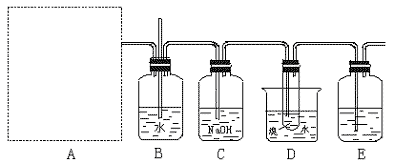 ЪЕбщЃКЯТЭМЮЊЪЕбщЪвгУввЯЉгывКфхзїгУжЦШЁ1ЃЌ2-ЖўфхввЭщЕФВПЗжзАжУЭМЃЌ
ЪЕбщЃКЯТЭМЮЊЪЕбщЪвгУввЯЉгывКфхзїгУжЦШЁ1ЃЌ2-ЖўфхввЭщЕФВПЗжзАжУЭМЃЌ
1ЃЌ2-ЖўфхввЭщЕФжївЊЮяРэаджЪЪЧ
|
ШлЕу |
ЗаЕу |
УмЖШ |
ШмНтад |
|
9.79Ёц |
131.4Ёц |
2.18gЁЄcm-3 |
ФбШмгкЫЎвзШмгкДМУбЕШ |
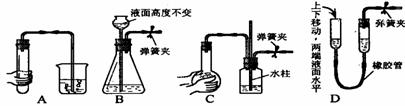
(1)ЪддкЗНПђФкЛГіввЯЉЕФЗЂЩњзАжУЭМЁЃ
(2)BЁЂDжаЖМЪЂгаЫЎЃЌетСНИізАжУЕФзїгУЗжБ№ЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЂ
ЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
(3)CКЭEзАжУЖМЪЂгаNaOHШмвКЃЌЫќУЧЕФзїгУЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
(4)аДГівдввДМЁЂХЈСђЫсЁЂвКфхЮЊжївЊдСЯЩњГЩ1ЃЌ2-ЖўфхввЭщЕФжївЊЛЏбЇЗДгІЗНГЬЪНЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁ
10ЁЂвбжЊФГаЉЕчНтжЪЗжзгЕФжааФдзгзюЭтВуЕчзгЮДДяБЅКЭНсЙЙЃЌЦфЕчРыВЩШЁНсКЯШмвКжаЦфЫќРызгЪЙжааФдзгзюЭтВуДяЕНБЅКЭНсЙЙЕФаЮЪНЃЌШчХ№ЫсдкЫЎжаПЩгУЗНГЬЪНБэЪОЮЊЃКЂйH3BO3 + H2O 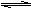 ЁЁ[B(OH)4]- + H+ЃЛЂкюыЕФЛЏКЯЮяМфПЩЗЂЩњвдЯТЗДгІЃКBeCl2+Na2BeO2+2H2OЃН2NaCl+2Be(OH)2Ё§ЁЃдђвдЯТЭЦЖЯжае§ШЗЕФЪЧ
ЁЁ[B(OH)4]- + H+ЃЛЂкюыЕФЛЏКЯЮяМфПЩЗЂЩњвдЯТЗДгІЃКBeCl2+Na2BeO2+2H2OЃН2NaCl+2Be(OH)2Ё§ЁЃдђвдЯТЭЦЖЯжае§ШЗЕФЪЧ
A ЁЂBeCl2ШмвКpHЃМ7ЃЌНЋЦфеєИЩЁЂзЦЩеКѓПЩЕУВаСєЮяBeCl2 ЁЁB ЁЂNa2BeO2ШмвКpHЃО7ЃЌНЋЦфеєИЩЁЂзЦЩеКѓПЩЕУВаСєЮяNa2BeO2 ЁЁC ЁЂBe(OH)2КЭB(OH)3ОљЪЧСНадЧтбѕЛЏЮяЃЌЧвХ№ЫсПЩЪгЮЊШ§дЊЫс ЁЁD ЁЂХ№ЫсМгШыЫЎжаКѓПЩДйНјЫЎЕФЕчРы
9ЁЂ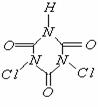
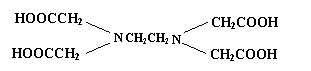 ОнЪРНчЮРЩњзщжЏЕїВщЃЌШБЬњадЦЖбЊЪЧЪРНчЩЯзюСїааЕФгЊбјадЮЪЬтЃЌвЛИіМђЕЅЕФАьЗЈМДЪЧдкЦеЭЈНДгЭжаМгШыЮоЬњаШЮЖЁЂМЋвзБЛШЫЬхЮќЪеЕФЬэМгМС--EDTAFeNaЃЌЦфжаEDTAНсЙЙ(ШчЯТзѓЭМ)ЃЌНДгЭЩњВњвдКѓЕФЗЯЫЎПЩгУЮяжЪТЬЩЋЯћЖОМС(ЯћЖОКѓЮоЙЋКІ)X(ШчЯТгвЭМ)РДЩБОњЁЃ
ОнЪРНчЮРЩњзщжЏЕїВщЃЌШБЬњадЦЖбЊЪЧЪРНчЩЯзюСїааЕФгЊбјадЮЪЬтЃЌвЛИіМђЕЅЕФАьЗЈМДЪЧдкЦеЭЈНДгЭжаМгШыЮоЬњаШЮЖЁЂМЋвзБЛШЫЬхЮќЪеЕФЬэМгМС--EDTAFeNaЃЌЦфжаEDTAНсЙЙ(ШчЯТзѓЭМ)ЃЌНДгЭЩњВњвдКѓЕФЗЯЫЎПЩгУЮяжЪТЬЩЋЯћЖОМС(ЯћЖОКѓЮоЙЋКІ)X(ШчЯТгвЭМ)РДЩБОњЁЃ
ЯТСаЫЕЗЈе§ШЗЕФЪЧ
AЁЂ1mol EDTAФмгы4mol NaOHЗЂЩњЗДгІ
BЁЂПЩгУЗжвКТЉЖЗДгЬњЧПЛЏНДгЭжаЗжРыГіEDTAFeNaЁЁЁЁЁЁЁЁ
CЁЂEDTAКЭXдквЛЖЈЬѕМўЯТОљФмЗЂЩњЫЎНтЗДгІ
DЁЂXЦ№бѕЛЏЩБОњзїгУЕФПЩФмЪЧЦфЫЎНтВњЮяДЮТШЫс
8ЁЂЯТСаИїЭМЫљЪОзАжУЕФЦјУмадМьВщжаЃЌТЉЦјЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com