
题目列表(包括答案和解析)
1.(1)C,(2)4.36:1,(3)PdH0.8。
7.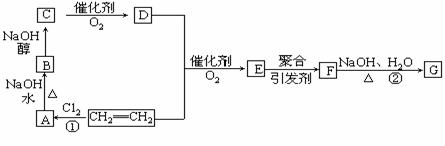 以石油产品乙烯为起始原料进行合成高分子化合物F和G,合成路线如图所示:
以石油产品乙烯为起始原料进行合成高分子化合物F和G,合成路线如图所示:
已知:E的分子式为C4H6O2,F的分子式为(C4H6O2)n(俗名“乳胶”的主要成分),G的分子式为(C2H4O)n(可用于制化学浆糊),2CH2=CH2+2CH3COOH+O2
 2C4H6O2(醋酸乙烯酯)+2H2O,卤代烃(R-X)能发生消去反应和水解反应,例如:
2C4H6O2(醋酸乙烯酯)+2H2O,卤代烃(R-X)能发生消去反应和水解反应,例如:
CH3CH2Cl  CH2=CH2+HCl
CH2=CH2+HCl
CH3CH2Cl+H2O  CH3CH2OH+HCl
CH3CH2OH+HCl
又知:与 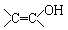 结构相似的有机物不稳定,发生分子重排生成
结构相似的有机物不稳定,发生分子重排生成 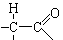 请回答下列问题:
请回答下列问题:
(1)写出结构简式:E_______________,F___________________。
(2)反应①、②的反应类型。
(3)写出A  B、B
B、B  C的化学方程式。
C的化学方程式。
答案和部分试题提示
6.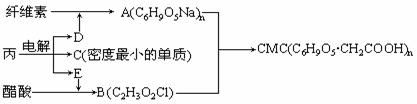 CMC在食品工业中可制造人造奶油。CMC可按下列流程生产:
CMC在食品工业中可制造人造奶油。CMC可按下列流程生产:
(1)写出丙、D、C、E各物质的名称。
(2)由纤维素和醋酸作为原始反应物生成CMC的反应,可以看成属于的反应类型是______,A、B反应产物中又有丙生成。丙可以看成是催化剂吗?答:____,原因是____。
5.去年9月底,国家质检总局查处了在食品中使用“雕白块”七大案例。“雕白块”的化学名称为甲醛次硫酸氢钠,违法者往食品中添加“雕白块”是为了漂白增色、防腐、增加米面制品的韧性及口感。但人食用“雕白块”后会刺激肠道,引起过敏和食物中毒,容易致癌。已知“雕白块”是甲醛和次硫酸氢钠(可表示成Na+[OSOH]-)反应制得:
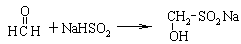
回答下列问题:
(1)“雕白块”_______________(填“易”或“微”或“难”)溶于水。“雕白块”具有________(填“强还原性”或“强氧化性”),写出“雕白块”溶液中滴加足量碘水所发生反应的化学方程式_____________________________________。
(2)写出次硫酸氢根的电子式___________________________。
(3)写出水溶液中次硫酸氢钠和氢氧化钾反应的离子方程式____________________。
(4)甲醛能使__________变性凝固,所以可用其浓溶液保存动物标本。
(5)甲醛是非常重要的合成原料。纯净的甲醛在[F3B←O(CH2CH3)2]配位化合物的催化下,生成聚甲醛(是一种优良的工程塑料),聚甲醛的结构简式为_____________;俄国化学家布特列洛夫在1861年首次发现在弱碱作用下,6个甲醛分子加合得到己糖,此己糖的分子式为___________。
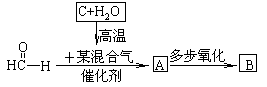 (6)已知
(6)已知
其中A可还原新制的氢氧化铜悬浊液,亦可与乙酸发生酯化反应;B的相对分子质量是甲醛的整数倍,自然界中常以盐的形式存在于多种植物的细胞膜中,B可洗除衣物上的铁锈渍。完成下列填空:
A的同分异构体有(写出结构简式)____________________________。
A催化加氢的化学方程式_____________________________________。
B可被酸性高锰酸钾溶液氧化,写出B跟稀硫酸、高锰酸钾混合溶液反应的反应式_____。
3.2001年11月20日,《解放日报》报道:南太平洋岛国“图瓦卢被迫全国移民”到新西兰。该国前总理佩鲁曾声称图瓦卢是“温室效应的第一个受害者”。目前该国正面临生存环境严重恶化的局面。该国岛屿近20年来已经被海水侵蚀得千疮百孔,岛上的淡水日益减少;海水的大量侵入使土壤盐碱化,粮食和蔬菜无法正常生长。图瓦卢陆地最高处仅海拔4.5m,由于海平面日渐升高,据估计这些岛屿将于50年内被海水淹没。请根据以上材料分析:
(1)图瓦卢是由多个珊瑚礁形成的岛国。由于大气中CO2含量的剧增,大量珊瑚礁(主要成分是碳酸钙)被海水侵蚀,其原因是(用化学方程式表示): 。
(2)温室效应导致海平面上升,引起温室效应的人为原因主要是: 。
(3)为了控制温室效应。各国科学家提出了不少方法和设想。有人根据液态CO2密度大于海水密度的事实,设想将CO2液化后,送入深海海底。以减小大气中CO2的浓度。为使CO2液化,可采用的措施是( )。
(A)减压、升温 (B)增压、升温 (C)减压、降温 (D)增压、降温
(4)科学家致力于二氧化碳的“组合转化”技术研究,把过多的二氧化碳转化为有益于人类的物质。如将CO2和H2以1︰4的比例混合,通入反应器。在适当的条件下及反应,可获得一种重要的能源。请完成以下化学方程式:
CO2+4H2→( )+2H2O
若将CO2与H2混合,在一定条件下以1︰3的比例发生反应,生成某种重要的化工原料和水。该化工原料可能是( )。
(A)烷烃 (B)烯烃 (C)炔烃 (D)芳香烃
(5)有效地减缓大气中CO2大量增加的生态学措施是( )。
(A)使用天然气等燃料 (B)控制全球人口增长
(C)植树造林,保护森林 (D)立即减少煤和石油的燃烧
2.随着材料科学的发展,金属钒及其化合物得到了越来越广泛的应用,并被誉为“合金维生素”。已知钒的原子序数为23,回答下列问题:
(1)钒被认为是一种稀土元素,广泛分散于各种矿物中。钾钒铀矿中的钒原子最外层已达8电子稳定结构,其化学式为K2H6U2V2O15,若用氧化物的形式表示,该化合物的化学式为____________。
(2)测定钒含量的方法是先把钒转化成V2O5,V2O5在酸性溶液里转变成VO2+,再用盐酸、硫酸亚铁、草酸等测定钒。总反应式可表示为:
VO2++H2C2O4→VO++CO2+H2O(未配平)
其中还原剂是________ 。若消耗0.9g草酸,所对应钒元素质量是_____g。
1.近年来,对未来动力燃料氢能源的研究获得了迅速发展。
(1)为了有效地发展民用氢能源,首先必须制得廉价的氢气,下列可供开发又较经济且资源可持续利用的制氢方法是
A.电解水 B.锌和稀硫酸反应 C.光解海水 D.以石油、天然气为原料
(2)氢气燃料时耗氧量小,发热量大。已知热化学方程式为:
C(g)+O2(g)=CO2(g)+393.5kJ 2H2(g)+O2(g)=2H2O(l)+571.6kJ
试通过计算说明等质量的氢气和碳燃烧时发热量的大小关系。
(3)氢能源有可能实现能量的储存,也有可能实现经济、高效的输送。研究表明,过渡金属元素与氢可生成储氢材料金属氢化物(又称间充氢化物)。在这类氢化物中,氢原子填充在金属的晶格间隙,其组成不固定,通常是非化学计量的,如:LaH2.76、TiH1.73、CeH2.69、ZrH1.98、PrH2.85、TaH0.78。书籍标准状况下,1体积钯粉大约可吸附896体积氢气(钯粉密度为10.64 g·cm-3),相对原子质量为106.4),试写出钯(Pd)的氢化物“化学式”:_________。
33.青苹果剖面遇碘溶液显蓝色,成熟的苹果剖面能还原银氨溶液,这说明
(A)青苹果中含淀粉不含糖类 (B)熟苹果中只含糖类不含淀粉
(C)苹果成熟进程中,淀粉转化为单糖(D)苹果转熟时,单糖聚合成淀粉
32.人们把食品分为绿色食品、蓝色食品、白色食品等。绿色植物通过光合作用转化的食品叫做绿色食品,海洋提供的食品叫蓝色食品,通过微生物发酵制得的食品叫白色食品。下面属于白色食品的是
(A)食醋 (B)面粉 (C)菜油 (D)海带
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com