
ÌâÄ¿Áбí(°üÀ¨´ð°¸ºÍ½âÎö)
6£®ÏÂÁÐ˵·¨ÕýÈ·µÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ (¡¡¡¡ )
¡¡¡¡¡¡ A£®Àë×Ó»¯ºÏÎïÖÐÒ»¶¨º¬ÓнðÊôÔªËØ
¡¡¡¡¡¡ B£®¹¹³É·Ö×Ó¾§ÌåµÄ΢Á£ÖÐÒ»¶¨º¬Óй²¼Û¼ü
¡¡¡¡¡¡ C£®Ô×Ó¾§ÌåÈÛ»¯ÒªÆÆ»µ¹²¼Û¼ü
¡¡¡¡¡¡ D£®Ö»ÓÐÀë×Ó»¯ºÏÎïÖвŴæÔÚÀë×Ó
5£®ÒÑÖª·´Ó¦£º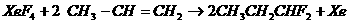 £¬ÏÂÁÐÓйØ˵·¨ÕýÈ·µÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ (¡¡¡¡ )
£¬ÏÂÁÐÓйØ˵·¨ÕýÈ·µÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ (¡¡¡¡ )
¡¡¡¡¡¡ A£®¸Ã·´Ó¦²»ÊôÓÚÑõ»¯»¹Ô·´Ó¦
¡¡¡¡¡¡ B£®XeF4¼ÈÊÇÑõ»¯¼Á£¬ÓÖÊÇ»¹Ô¼Á
¡¡¡¡¡¡ C£®·´Ó¦Öеç×ÓÓÉXeתÒƵ½C
¡¡¡¡¡¡ D£®Ñõ»¯¼ÁÓ뻹ԼÁµÄÎïÖʵÄÁ¿Ö®±ÈΪ1£º2
4£®ÒÑÖªÔÚ25¡æ¡¢101kPaÏ£¬1gC8H18(ÐÁÍé)ȼÉÕÉú³É¶þÑõ»¯Ì¼ºÍҺ̬ˮʱ·Å³ö48.40kJÈÈÁ¿¡£±íʾÉÏÊö·´Ó¦µÄÈÈ»¯Ñ§·½³ÌʽÕýÈ·µÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ (¡¡¡¡ )
¡¡¡¡¡¡ A£®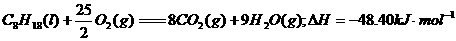
¡¡¡¡¡¡ B£®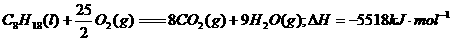
¡¡¡¡¡¡ C£®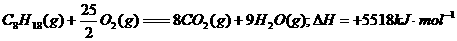
¡¡¡¡¡¡ D£®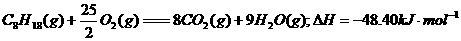
2£®13C-NMR(ºË´Å¹²Õñ)15N-NMR¿ÉÓÃÓڲⶨµ°°×ÖʺËËáµÈÉúÎï´ó·Ö×ӵĿռä½á¹¹£¬Kurt WuthrichµÈÈËΪ´Ë»ñµÃ2002Äêŵ±´¶û»¯Ñ§½±¡£ÏÂÁÐÓйØ13C¡¢15NÐðÊöÕýÈ·µÄÊÇ(¡¡¡¡ )
¡¡¡¡¡¡ A£®13CÓë15NÓÐÏàͬµÄÖÐ×ÓÊý¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ B£®13CÓëC60ÓÐÏàͬµÄÖÐ×ÓÊý
¡¡¡¡¡¡ C£®15NÓë14N»¥ÎªÍ¬Î»ËØ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ D£®15NµÄºËÍâµç×ÓÊýÓëÖÐ×ÓÊýÏàͬ
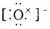 ¡¡
3£®ÏÂÁеç×ÓʽÖдíÎóµÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ (¡¡¡¡ )
¡¡
3£®ÏÂÁеç×ÓʽÖдíÎóµÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ (¡¡¡¡ )
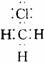 ¡¡
¡¡
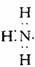 ¡¡
¡¡¡¡¡¡ A£®Na+¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ B£®
¡¡
¡¡¡¡¡¡ A£®Na+¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ B£®
¡¡¡¡¡¡ C£®¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ D£®
1£®ÉèNA´ú±í°¢·ü¼ÓµÂÂÞ³£ÊýµÄÖµ£¬ÏÂÁÐ˵·¨ÕýÈ·µÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ (¡¡¡¡ )
¡¡¡¡¡¡ A£®1.8gï§Àë×ÓËùº¬µÄµç×ÓÊýΪ1.1NA
¡¡¡¡¡¡ B£®1mol°×Á×·Ö×ÓÖÐËùº¬¹²¼Û¼üÊýΪ4NA
¡¡¡¡¡¡ C£®±ê¿öÏÂ22.4LÒÒ´¼Ëùº¬µÄ·Ö×ÓÊý±Ø¶¨ÎªNA
¡¡¡¡¡¡ D£®ÔÚµç½âʳÑÎË®µÄʵÑéÖУ¬²âµÃµç½âºóÈÜÒºµÄpHΪ14£¬ÓÖÖªµç½âºóÈÜÒº×ÜÌå»ýΪ1L£¬ÔòÒõ¼«Îö³öµÄÆøÌåµÄ·Ö×ÓÊýΪ0.5NA
24¡¢(9`)ÔÚ±ê×¼×´¿öÏ£¬½«224 L HClÆøÌåÈÜÓÚ635 mLË®ÖÐ(¦Ñ£½1 g£¯cm3)£¬ËùµÃÑÎËáµÄÃܶÈΪ1.18 g£¯cm3¡£ÊÔ¼ÆË㣺
(1)¡¡¡¡ È¡³öÕâÖÖÑÎËá100.0 mL£¬Ï¡ÊÍÖÁ1.18 L£¬ËùµÃÏ¡ÑÎËáµÄÎïÖʵÄÁ¿Å¨¶È¡£
(2)ÔÚ40.0 mL 0.0650 mol¡¤L£1Na2CO3ÈÜÒºÖУ¬ÖðµÎ¼ÓÈë(1)ËùÅäÖƵÄÏ¡ÑÎËᣬ±ßµÎ±ßÕñµ´¡£Èôʹ·´Ó¦²»²úÉúCO2ÆøÌ壬¼ÓÈëÏ¡ÑÎËáµÄÌå»ý×î¶à²»Äܳ¬¹ý¶àÉÙºÁÉý?
´ð°¸ 1¡¢C 2¡¢C 3¡¢A 4¡¢D 5¡¢C 6¡¢D 7¡¢B 8¡¢A 9¡¢BC 10¡¢AC¡¢ 11¡¢BC¡¢12¡¢BD 13¡¢B 14¡¢C 15¡¢D 16¡¢A 17¡¢B 18¡¢BD 19¡¢(1) 1¡¢2¡¢4¡¢3¡¢5 (3)Æ«¸ß¡¢ (4)Æ«µÍ¡¢Æ«µÍ¡¢ (5)ÖØ×ö¡¢ÖØ×ö 20¡¢(1)Zn£¬½«Cu2+¡¢Fe3+»¹Ô (2)20%µÄH2O2£¬ ½«Fe2+Ñõ»¯ÎªFe3+£¬Í¬Ê±²»ÒýÈëÔÓÖÊÀë×Ó (3)ZnO»òZnCO3»òZn(OH)2£¬µ÷½ÚÈÜÒºµÄPHÖµ½«Fe3+³Áµí 21¡¢(1)O¡¢H¡¢N¡¢Cl 22¡¢(1)0.93-1.57 (2)2.25-3.44 (2)XÔ½´ó£¬Ô×Ӱ뾶ԽС£¬ ÖÜÆÚÐÔ (3)µª (4)¹²¼Û¼ü (5)Áù-IA 23¡¢3£º2 24¡¢1mol/L 2.6mL
23¡¢(8`)ÒÑÖªÏÂÁÐÁ½¸öÈÈ»¯Ñ§·½³Ìʽ£»
¡¡¡¡ H2(g)+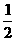 O2(g)==== H2O(l )£»¡÷H= £285.8kJ/ mol
O2(g)==== H2O(l )£»¡÷H= £285.8kJ/ mol
C3H8(g)+5O2(g) ==== 3CO2(g) +4H2O(l)£»¡÷H= £2220.0 kJ/ mol
¡¡ (1)ʵÑé²âµÃH2ºÍC3H8µÄ»ìºÏÆøÌå¹²5mol£¬ÍêȫȼÉÕÉú³ÉҺ̬ˮʱ·ÅÈÈ5297.4kJ£¬Ôò»ìºÏÆøÌåÖÐH2ºÍC3H8µÄÌå»ý±ÈÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡¡¡£
¡¡ (2)ÒÑÖª£ºH2O(l)=H2O(g)£»¡÷H=+44.0 kJ/ mol ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
¡¡¡¡¡¡¡¡ ÊÔд³ö±ûÍéȼÉÕÉú³ÉCO2ºÍË®ÕôÆøÈÈ»¯Ñ§·½³Ìʽ¡£
20¡¢(15`)ijСÐÍ»¯¹¤³§Éú²úð©·¯(ZnSO4¡¤7H2O)µÄ¹¤ÒÕÁ÷³ÌÈçÏÂͼËùʾ£º
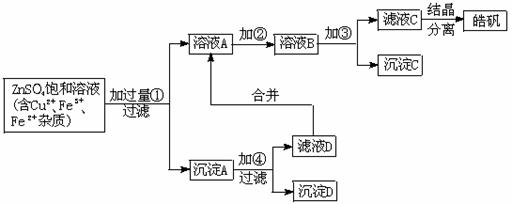
ÒÑÖª£º¿ªÊ¼Éú³ÉÇâÑõ»¯Îï³Áµíµ½³ÁµíÍêÈ«µÄpH·¶Î§·Ö±ðΪ£º
Fe(OH)3£º2.7-3.7¡¡ Fe(OH)2£º7.6-9.6¡¡ Zn(OH)2£º5.7-8.0
ÊԻشðÏÂÁÐÓйØÎÊÌ⣺
(1)¼ÓÈëµÄÊÔ¼Á¢ÙÓ¦ÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ £¬
ÆäÄ¿µÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
(2)¼ÓÈëµÄÊÔ¼Á¢Ú£¬¹©Ñ¡ÔñʹÓõÄÓУº°±Ë®¡¢NaClOÈÜÒº¡¢20%µÄH2O2¡¢Å¨ÁòËᡢŨÏõËáµÈ£¬Ó¦Ñ¡Óá¡¡¡¡¡¡¡¡¡¡¡¡¡ £¬ÆäÀíÓÉÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
(3)¼ÓÈëµÄÊÔ¼Á¢ÛÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
µÄÄ¿µÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡£
21(14`)¡¢A¡¢B¡¢C¡¢D¾ùΪ¶ÌÖÜÆÚÔªËØ£¬A¡¢B¿ÉÐγÉÁ½ÖÖҺ̬»¯ºÏÎÆä×î¼òʽ·Ö±ðΪBAºÍB2A¡£AÓëD¿ÉÐγÉÆø̬»¯ºÏÎïDA¡¢DA2£ºA¡¢B¡¢D¿É×é³ÉÀë×Ó¾§Ì壬¸Ã¾§ÌåµÄ»¯Ñ§Ê½ÎªB4A3D2£¬ÆäË®ÈÜÒº³ÊÈõËáÐÔ£ºBÓëD¿ÉÐγÉÒ»ÖÖ¼«Ò×ÈÜÓÚË®µÄ¼îÐÔÆøÌåX£¬BÓëC¿ÉÄÜÐγɼ«Ò×ÈÜÓÚË®µÄËáÐÔÆøÌåY£¬ÒÑÖªX·Ö×ÓÓëB2A·Ö×ÓÖеĵç×ÓÊýÏàµÈ£¬Y·Ö×ÓÖеĵç×ÓÊýÓë×î¼òʽΪBAµÄµç×ÓÏàµÈ£¬Çë»Ø´ð£º
(1)д³öËÄÖÖÔªËصķûºÅ£ºA________ B________ C________ D________
(2)д³öÏÂÁз´Ó¦µÄ»¯Ñ§·½³Ìʽ£º
¢Ù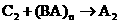 £º________________________________
£º________________________________
¢Ú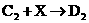 £º________________________________
£º________________________________
(3)B4A3D2µÄ»¯Ñ§Ê½Îª___________£¬ÆäË®ÈÜÒºÏÔËáÐÔµÄÀë×Ó·½³ÌʽΪ_________________________________¡£
(4)ÒÑ֪Һ̬XÓëB2AÏàËÆ£¬Ò²¿É·¢Éú΢ÈõµÄµçÀ룬µçÀë³öº¬ÓÐÏàͬµç×ÓÊýµÄ΢Á££¬ÔòXµÄµçÀë·½³ÌʽΪ__________________________¡£
22(14`)¡¢²»Í¬ÔªËصÄÔ×ÓÔÚ·Ö×ÓÄÚÎüÒýµç×ÓµÄÄÜÁ¦´óС¿ÉÓÃÒ»¶¨ÊýÖµxÀ´±íʾ£¬ÈôxÔ½´ó£¬ÆäÔ×ÓÎüÒýµç×ÓÄÜÁ¦Ô½Ç¿£¬ÔÚËùÐγɵķÖ×ÓÖгɷÖΪ´ø¸ºµçºÉµÄÒ»·½¡£
ÏÂÃæÊÇijЩ¶ÌÖÜÆÚÔªËصÄxÖµ£º
|
ÔªËØ·ûºÅ |
Li |
Be |
B |
C |
O |
F |
Na |
Al |
Si |
P |
S |
Cl |
|
xÖµ |
0.98 |
1.57 |
2.04 |
2.25 |
3.44 |
3.98 |
0.93 |
1.61 |
1.90 |
2.19 |
2.58 |
3.16 |
(1)¡¡¡¡¡¡ ͨ¹ý·ÖÎöxÖµ±ä»¯¹æÂÉ£¬È·¶¨Mg¡¢NµÄxÖµ·¶Î§£º
¡¡¡¡¡¡¡¡¡¡ £¼x(Mg)£¼¡¡¡¡¡¡¡¡¡¡ £¬¡¡¡¡¡¡¡¡¡¡ £¼x(N)£¼¡¡¡¡¡¡¡¡¡¡ ¡£
(2)ÍƲâxÖµÓëÔ×Ӱ뾶µÄ¹ØϵÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡£¾Ý¾Ý¶ÌÖÜÆÚÔªËصÄxÖµ±ä»¯Ìص㣬ÌåÏÖÁËÔªËØÐÔÖʵġ¡¡¡¡¡¡¡¡¡ ±ä»¯¹æÂÉ¡£
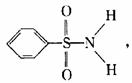
(3)ijÓлú»¯ºÏÎï½á¹¹Ê½Îª£º¡¡¡¡¡¡¡¡ ÆäÖÐS-N¼üÖÐÄãÈÏ
Ϊ¹²Óõç×Ó¶ÔÆ«ÏòË£¿¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ (дÔ×ÓÃû³Æ)¡£
(4)¾Ñé¹æÂɸæËßÎÒÃÇ£ºµ±³É¼üµÄÁ½Ô×ÓÏàÓ¦ÔªËصÄx²îÖµ(¦¤x)¼´¦¤x£¾1.7ʱ£¬Ò»°ãΪÀë×Ó¼ü£¬¦¤x£¼1.7£¬Ò»°ãΪ¹²¼Û¼ü£¬ÊÔÍƶϣºAlBr3Öл¯Ñ§¼üÀàÐÍÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
(5)Ô¤²âÔªËØÖÜÆÚ±íÖУ¬xÖµ×îСµÄÔªËصÄλÖ㺡¡¡¡¡¡¡¡¡¡¡¡¡¡ (·ÅÉäÐÔÔªËسýÍâ)¡£
19¡¢(16`)ʵÑéÊÒÅäÖÆ500 mL 0.5 mol¡¤L£1µÄNaC1ÈÜÒº£¬ÓÐÈçϲÙ×÷²½Ö裺
¢Ù°Ñ³ÆÁ¿ºÃµÄNaC1¾§Ìå·ÅÈëСÉÕ»³ÖУ¬¼ÓÊÊÁ¿ÕôÁóË®Èܽ⣻¢Ú°Ñ¢ÙËùµÃÈÜҺСÐÄתÈë500 mLÈÝÁ¿Æ¿ÖУ»¢Û¼ÌÐøÏòÈÝÁ¿Æ¿ÖмÓÕôÁóË®ÖÁÒºÃæ¾à¿Ì¶È1 cm - 2 cm´¦£¬¸ÄÓýºÍ·µÎ¹ÜСÐĵμÓÕôÁóË®ÖÁÈÜÒº°¼Ãæµ×²¿Óë¿Ì¶ÈÏßÏàÇУ»¢ÜÓÃÉÙÁ¿ÕôÁóˮϴµÓÉÕ±ºÍ²£Á§°ô2-3´Î£¬Ã¿´ÎÏ´µÓµÄÒºÌ嶼СÐÄתÈëÈÝÁ¿Æ¿£¬²¢ÇáÇáÒ¡ÔÈ£»¢Ý½«ÈÝÁ¿Æ¿ÈûÈû½ô£¬³ä·ÖÒ¡ÔÈ¡£ÌîдÏÂÁпհףº
(1)²Ù×÷²½ÖèµÄÕýȷ˳ÐòΪ_______¡¡¡¡ ¡¡¡¡_¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡¡(ÌîÐòºÅ)¡£
(2)±¾ÊµÑéÓõ½µÄ»ù±¾ÊµÑéÒÇÆ÷ÓС¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡¡¡£
(3)ijͬѧ¸©ÊÓÈÝÁ¿Æ¿¿Ì¶ÈÏߵμÓÕôÁóË®¶ø¶¨ÈÝ£¬¶ÔËùÅäÈÜҺŨ¶ÈÓкÎÓ°Ïì?________(¡°Æ«¸ß¡±¡°Æ«µÍ¡±»ò¡°ÎÞÓ°Ï족)¡£
(4)Èô³öÏÖÈçÏÂÇé¿ö£¬¶ÔËùÅäÈÜҺŨ¶È½«ÓкÎÓ°Ï죺
ûÓнøÐвÙ×÷²½Öè¢Ü________£»¼ÓÕôÁóˮʱ²»É÷³¬¹ýÁ˿̶È________¡£
(5)ÈôʵÑé¹ý³ÌÖгöÏÖÈçÏÂÇé¿öÓ¦ÈçºÎ´¦Àí?
¼ÓÕôÁóˮʱ²»É÷³¬¹ýÁ˿̶ȡ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
ÏòÈÝÁ¿Æ¿ÖÐתÒÆÈÜҺʱ(ʵÑé²½Öè¢Ú)²»É÷ÓÐÒºµÎµôÔÚÈÝÁ¿Æ¿ÍâÃæ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡¡
18¡¢ÏÂÁлÓкáÏßµÄÎïÖÊÔÚ·´Ó¦Öв»ÄÜÍêÈ«ÏûºÄµÄÊÇ
A.½«º¬ÉÙÁ¿H2O(g)µÄH2ͨÈëÊ¢ÓÐ×ãÁ¿Na2O2µÄÈÝÆ÷Öв¢²»¶ÏÓõç»ð»¨µãȼ
B.½«l mol CuÖÃÓÚº¬2 mo1H2SO4µÄŨÁòËáÖмÓÈÈ
C.ÔÚÇ¿¹â³ÖÐøÕÕÉäÏ£¬Ïò¹ýÁ¿µÄCa(C1O)2ÈÜÒºÖÐͨÈëÉÙÁ¿µÄCO2
D.ÔÚÒ»¶¨Ìõ¼þÏ£¬3Ìå»ýH2ºÍ1Ìå»ýN2ÔÚ´ß»¯¼Á´æÔÚÏ·´Ó¦
¹ú¼ÊѧУÓÅÑ¡ - Á·Ï°²áÁбí - ÊÔÌâÁбí
ºþ±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ÐÅÏ¢¾Ù±¨Æ½Ì¨ | ÍøÉÏÓк¦ÐÅÏ¢¾Ù±¨×¨Çø | µçÐÅթƾٱ¨×¨Çø | ÉæÀúÊ·ÐéÎÞÖ÷ÒåÓк¦ÐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ÐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com