
题目列表(包括答案和解析)
20.在一定温度时,将1mol A和2mol B放入容积为5L的某密闭容器中发生如下反应:
 A(s)+2B(g) C(g)+2D(g),经5min后,测得容器内B的浓度减少了0.2mol/L。
A(s)+2B(g) C(g)+2D(g),经5min后,测得容器内B的浓度减少了0.2mol/L。
下列叙述不正确的是( )
A.在5min内该反应用C的浓度变化表示的反应速率为0.02mol/(L·min)
B.5min时,容器内D的浓度为0.2mol/L
C.当容器内压强保持恒定时,该可逆反应达到平衡状态
D.5min时容器内气体总的物质的量为3mol
19.一定条件下,往容积恒定的密闭容器中投入2molA和1molB,发生可逆反应:
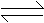 2A(g)+B(g)
C(g)+D(s),达到平衡时,测得压强为原压强的
2A(g)+B(g)
C(g)+D(s),达到平衡时,测得压强为原压强的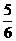 ,
,
则A的转化率为[ ]
A.25% B.40% C.50% D.75%
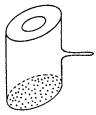
18.实验室里常见到如图所示的仪器,该仪器为两头密封的玻璃管,中间带有一根玻璃短柄。当玻璃管内装有碘片时,用此仪器进行碘的升华实验,具有装置简单、操作方便、现象明显、可反复使用等优点。用此仪器不能反复进行的实验是[ ] A.NH4Cl受热分解的实验 B.KMnO4受热分解的实验 C.白磷和红磷在一定温度下相互转变的实验 D.无水CuSO4与胆矾的互变实验
17. 用一定量的铁与足量的稀硫酸及足量的CuO制取单质铜,有人设计了以下两种方案:
用一定量的铁与足量的稀硫酸及足量的CuO制取单质铜,有人设计了以下两种方案:
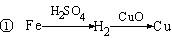
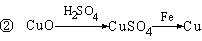 若要制取得相同质量的铜单质,并按实验原则进行操作,则两者消耗的单质铁的量为[ ]
A.①多 B.②多 C.一样多 D.无法判断
若要制取得相同质量的铜单质,并按实验原则进行操作,则两者消耗的单质铁的量为[ ]
A.①多 B.②多 C.一样多 D.无法判断
16.下列各组溶液中,用括号内的试剂及物质间相互反应不能鉴别的一组是[ ] A.Ba(OH)2 KSCN NaCl Mg(NO3)2 (FeCl3溶液) B.NaNO3 NaHCO3 (NH4)2SO3 Na2SiO3 (H2SO4溶液) C.NH4Br K2CO3 NaI CaCl2 (AgNO3溶液) D.(NH4)3PO4 NaBr CuSO4 AlCl3 (KOH溶液)
15.下图两个装置中,溶液体积均为200 mL,开始时,电解质溶液的浓度均为0.1 mol/L,工作一段时间后,测得导线上都通过了0.02
mole-,若不考虑溶液体积的变化,则下列叙述正确的是[ ]
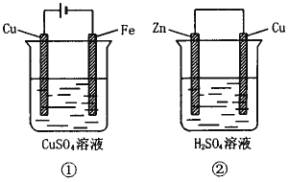 A.在①中Cu棒为阳极,在②中Cu棒为负极
B.电极上析出物质的质量:①<②
C.电极反应式:①中阳极:4OH--4e-=2H2O+O2↑;②中负极:2H++2e-=H2↑
D.溶液的pH:①不变,②增大
A.在①中Cu棒为阳极,在②中Cu棒为负极
B.电极上析出物质的质量:①<②
C.电极反应式:①中阳极:4OH--4e-=2H2O+O2↑;②中负极:2H++2e-=H2↑
D.溶液的pH:①不变,②增大
14.我国首创的海洋电池以铝板为负极,铂网为正极,海水为电解质溶液,空气中的氧气与铝反应产生电流。电池总反应为:4A1+3O2+6H2O=4A1(OH)3,下列说法不正确的是[ ] A.正极反应式为:O2+2H2O+4e-=4OH- B.电池工作时,电流由铝电极沿导线流向铂电极 C.以网状的铂为正极,可增大与氧气的接触面积 D.该电池通常只需更换铝板就可继续使用
13.把等物质的量的Na2SO4、NaCl、AgNO3混合物放入足量水中,经充分搅拌后,将所得溶液用石墨做电极进行电解,阳极生成的物质是[ ]
A.H2 B.Ag C.Cl2 D. O2
12.能正确表示下列化学反应的离子方程式是[ ]
A.氯气通入水中:Cl2+H2O==2H++ClO-+Cl-
B.硫化钠溶于水中:S2-+
2H2O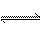 H2S
+ 2OH-
H2S
+ 2OH-
C.铜与稀硝酸反应:Cu + 4H+ +NO3- = Cu2++NO↑+2H2O
D.水玻璃与盐酸反应:SiO32-+2H+= H2SiO3↓
11.室温下,在强酸性和强碱性溶液中都不能大量共存的离子组是[ ] A .Ba2+、Fe2+、NO3-、Br- B.K+、Na+、SO32-、S2- C.K+、Na+、AlO2-、SO42- D.NH4+、Cu2+、Cl-、NO3-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com