
题目列表(包括答案和解析)
14.将0.1L含有0.02molCuSO4和0.01molNaCl的水溶液用惰性电极电解。电解一段时间后,某电极的质量增重了0.64g。下列说法正确的是
A.质量增重的电极为阳极 B.电解过程中电子转移数为0.02NA
C.电解过程中某电极上只有Cl2产生 D.电解过程中pH增大
13.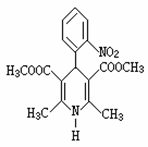 硝苯地平缓释片(简称NSRT)是一种用于治疗各种类型的高血压及心绞痛的新药,其结构式如右图所示。下列关于硝苯地平缓释片的说法正确的是
硝苯地平缓释片(简称NSRT)是一种用于治疗各种类型的高血压及心绞痛的新药,其结构式如右图所示。下列关于硝苯地平缓释片的说法正确的是
A.NSRT的分子式为C18H17N2O6
B.1molNSRT在水溶液中最多能消耗2molNaOH
C.NSRT不能使酸性高锰酸钾溶液褪色
D.1mol NSRT在一定条件下能和7molH2发生加成反应
12.类推是在化学学习和研究中常用的思维方法,但类推出的结论最终要经过实践的检验才能决定其正确与否,下列几种类推结论中错误的是
A.由Fe跟S直接化合可得FeS,类推出Cu跟S直接化合可得Cu2S
B.金属镁失火不能用CO2灭火,金属钠失火也不能用CO2灭火
C.NH4C1、NH4I结构相似,将两种固体分别加热,都分解生成卤化氢和氨气
D.原电池中通常是活泼金属做负极,不活泼金属做正极,用铜和铝与浓硝酸构成原电池时,铝是负极
11.下列离子方程式正确的是
A.等体积等物质的量浓度的氢氧化钡溶液与碳酸氢铵溶液混合:
2 OH- + NH4+ + HCO3-== CO32-+ NH3·H2O + H2O
B.乙酸和氢氧化钠溶液混合:OH-+ CH3COOH 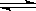 CH3COO- + H2O
CH3COO- + H2O
C.次氯酸钠溶液和氯化亚铁溶液混合:
6 Fe2+ + 3 ClO- + 3 H2O == 2 Fe(OH)3↓ + 4 Fe3+ + 3 Cl-
D.Fe(OH)3溶于氢碘酸:Fe(OH)3 + 3 H+ = Fe3+ + 3 H2O
10.某溶液可能含有K+、Ag+、A13+、AlO2-、S2-、CO32-、SO32-、NO3-等离子中的数种。向此溶液中加入稀盐酸,有浅黄色沉淀和气体出现,此溶液的焰色反应为紫色(透过蓝色钴玻璃)。根据以上实验现象,下列结论中错误的是
A.此溶液中一定有S2-、SO32-、K+ B.此溶液中可能有AlO2-、CO32-
C.此溶液中一定没有Ag+、A13+ D.此溶液中可能有S2-、NO3-
9.现有等体积的Ba(OH)2、KOH和NH3·H2O三种溶液,将它们分别与V1 L、V2 L、
V3 L等浓度的盐酸混合,下列说法中正确的是
A.若混合前三种溶液pH相等,将它们同等倍数稀释后,则KOH溶液pH最大
B.若混合前三种溶液物质的量浓度相等,混合后溶液呈中性,则V1>V2>V3
C.若混合前三种溶液物质的量浓度相等,酸碱恰好完全反应,则V1>V2>V3
D.若混合前三种溶液pH相等,酸碱恰好完全反应,则V1>V2>V3
8.已知:在100℃时,水的离子积为1×10-12,此时将pH=12的NaOH溶液V1 L与
pH=l的H2SO4溶液V2 L混合,若所得混合溶液的pH=10,则V1∶V2为
A.1 : 9 B.10: 1 C.9 : 1 D.1: 10
7.下列叙述不正确的是
A.乙醛或硝酸银溶液均能使蛋白质变性
B.将乙烯和二氧化硫分别通入酸性KMnO4溶液中,均能使KMnO4溶液褪色
C.反应AgBr + KI AgI
+ KBr能在水溶液中进行,是因为AgI比AgBr更难溶于水
AgI
+ KBr能在水溶液中进行,是因为AgI比AgBr更难溶于水
D.常温下浓硝酸可贮存在铁制或铝制容器中,说明常温下铁和铝与浓硝酸不反应
6.用NA表示阿伏加德罗常数,下列说法正确的是
A.71g氯气与过量的FeCl2溶液完全反应转移的电子数为2NA
B.1 mol甲基(-14CH3)所含中子数为9 NA
C.在标准状况下,2.24L二氯甲烷所含的分子数为0.1NA
D.2L 0.1mol/L 的醋酸钠溶液中,所含离子总数是0.2NA
5. 在101 kPa时燃烧1 t 含FeS2质量分数为70%的黄铁矿生成固态Fe2O3和气态SO2,放出4.98×106 kJ的热量,表示上述反应的燃烧热的热化学方程式正确的是
A.4FeS2(s)+11O2(g) = 2 Fe2O3(s)+8SO2(g); △H= -3414.8 kJ·mol-1
B.FeS2(s)+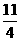 O2(g) =
O2(g) = 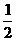 Fe2O3(s)+2SO2(g); △H=-853.7
kJ·mol-1
Fe2O3(s)+2SO2(g); △H=-853.7
kJ·mol-1
C.4FeS2(s)+11O2(g) = 2 Fe2O3(s)+8SO2(g); △H= +3414.8 kJ·mol-1
D.FeS2(s)+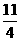 O2(g) =
O2(g) = 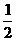 Fe2O3(s)+2SO2(g); △H=+853.7
kJ·mol-1
Fe2O3(s)+2SO2(g); △H=+853.7
kJ·mol-1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com