
题目列表(包括答案和解析)
4.下列说法正确的是
A.冰、水和水蒸气中都存在氢键
B.除稀有气体外的非金属元素都能生成不同价态的含氧酸
C.若ⅡA某元素的原子序数为m,则同周期IIIA元素的原子序数有可能为m+11
D.干冰升华时分子内共价键会发生断裂
3.下列对物质用途的描述中,错误的是
A.与Mg、Al比较,镁铝合金的强度和硬度均较大,常用作航天器的材料
B.Cl2、SO2、NaClO均可用于漂白某些物质
C.浓硫酸具有吸水性,可用于干燥HCl、H2S、O2
D.碳酸钠可用于制皂和制玻璃
2.下列有关HF、HCl、HBr、HI的说法错误的是
A.均为直线型极性分子 B.熔、沸点依次升高
C.稳定性依次减弱 D.还原性依次增强
1.化学与生活、环境、社会等密切相关。下列说法正确的是
A.凡含有食品添加剂的食物对人体健康都有害,不可食用
B.棉、麻、丝、毛及合成纤维完全燃烧都只生成H2O和CO2,对环境不会有影响
C.三聚氰胺(C3N6H6)是引起婴幼儿因食用“三鹿牌”奶粉而患泌尿系统结石病症的元凶,它不属于有机物
D.我国规定自2008年6月1日起,商家不得无偿提供塑料袋,目的是减少“白色污染”和节约资源
29. ( 15 分)
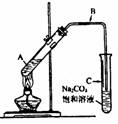 某兴趣小组利用右图装置,取不同浓度的硫酸与 3mL 无水乙醇和 2mL 冰醋酸分别进行制取乙酸乙酯的研究。
某兴趣小组利用右图装置,取不同浓度的硫酸与 3mL 无水乙醇和 2mL 冰醋酸分别进行制取乙酸乙酯的研究。
( l ) A 试管内生成乙酸乙酷的化学反应方程式为:
_______________________________________________________
( 2 )导气管 B 的管口没有插入饱和碳酸钠液面以下,原因是
__________________________________________________________
( 3 )兴趣小组记录的实验现象和结果如下表:

I.第 ① 组实验中,试管内溶液颜色随反应进行逐渐加深,最后变成黑色的原因是:
_______________________________________________________________________;
若同时有刺激性气味的气体产生,则可能发生的化学反应方程式是:
___________________________________________________________。
II.试管 C 的酯层中没有乙酸的实验组是(填组序号)____________________;从实验结果分析,选用催化剂的最佳浓度是_______________________________。
Ⅲ.由实验结果可知,盐酸_______(填“能”或“不能”)作酯化反应的催化剂,其原因是_______________________________________________________________________。
09届高中毕业班第一次诊断性检测
28. ( 16 分)
以 HCHO 和 C2H2为有机原料,经过下列反应可得化合物 N ( C4H8O2 )。
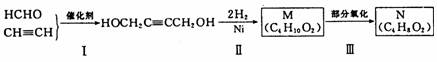
( l )反应 1 的反应类型为_______________。
( 2 ) HOCH2C≡CCH2OH 分子中,在同一个平面的原子最多有________个。
( 3 )化合物 M 不可能发生的反应是_______________(填序号)。
A.氧化反应 B.取代反应 C.消去反应 D.加成反应 E.还原反应
( 4 ) N 的同分异构体中,属于酯类的有________________种。
( 5 ) A 与 M 互为同分异构体,有如下转化关系。
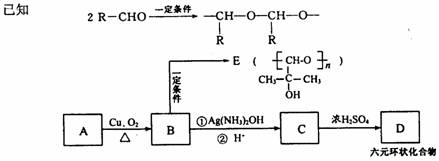
填写下列空白:
① A 的结构简式为_________________, B 中的官能团名称是___________________
② D 的化学式为_______________________
③ 写出 B 与银氨溶液反应的化学方程式:
____________________________________________________________
④ 在 120 ℃ 时,由 A 、 B 、 E 组成的混合物 wg 与氧气充分反应,生成产物全部为气体时,消耗氧气[m (O2)]的质量范围为____________________________________。
27. ( 13 分)
苯酚遇 FeC13 溶液发生显色反应,其原理如下:
Fe3 + + 6C6H5OH  [Fe (C6H5O)6]3一+6H+
[Fe (C6H5O)6]3一+6H+
黄色 紫色
( 1 )在 FeC13 与 C6H5OH 混合溶液中加入适量铁粉,溶液变为浅绿色。则该反应的离子方程式为_____________________________________________________:该反应中每消耗 0 . 2 mol 氧化剂,转移电子为_________________moL。
若在 FeC13 与 C6H5OH 的混合溶液中滴入足量 NaOH 溶液,可观察到有红褐色沉淀产生。则上述平衡__________移动(填“向左”、“向右”或“不”)。
( 2 )在苯酚钠中逐滴加入酸化的 FeCl3溶液,可依次出现红褐色沉淀一沉淀溶解一溶液显紫色一紫色变浅(或溶液由紫色变为黄色)等几种变化。请回答:
① 开始时出现红褐色沉淀的原因是(用分步写出的离子方程式表示)_______________
_____________________________________________________________________________
② 最后紫色变浅或变为黄色的原因是(用文字表述)__________________________
_______________________________________________________________________。
26. ( 16 分)
A 、 B 、 C 、 D 、 E 为原子序数依次增大的五种短周期元素。 A 、 E 同主族, A 能与 B 、 C 、 D 分别形成电子数相等的三种分子, C 、 D 最外层电子数之和与 E 的核外电子总数相等。试回答:
( 1 ) E 在周期表中的位置为_______周期_______族。
( 2 ) A 、 C 、 E 三种元素的原子半径由大到小的顺序是________(用元素符号填写)。
( 3 )化合物 BA4的空间构型为___________________,化合物 ABC中化学键类型为__________________, 它属于___________分子(填“极性”或“非极性”)。
化合物 C2A2是一种高能量分子,且 C 原子满足 8 电子稳定结构。写出 C2A2的电子式_______________________________________
( 4 ) A 、 D 、 E 三种元素可形成一种离子化合物 R ,用惰性电极电解 R 的稀溶液的反应方程式为_________________________________;电解一段时间后,溶液 pH_____(填“增大”、“减小”或“不变”)。
( 5 )在 0 . l mol·L-1E2BD3 的溶液中,各离子浓度由大到小的顺序是___________;分子式为 A2B2D4 的化合物,与等物质的量的 KOH 溶液反应后溶液呈酸性,其原因是(用文字表述)_________________________________________________________________
_________________________________________________________________________.
13.某同学按右图所示的装置进行试验。 A 、 B 为两种常见金属,它们的硫酸盐可溶于水。当 K 闭合时,在交换膜处 SO42一从右向左移动。下列分析正确的是
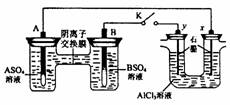 A.溶液中。(A2+)浓度减小
A.溶液中。(A2+)浓度减小
B.B 的电极反应: B-2e一==B2+
C.y 电极上有 H2 产生,发生还原反应
D.反应初期, x 电极周围出现白色胶状沉 淀,不久沉淀溶解
第 II 卷(非选择题,共60 分)
12.在盛有足量 A 的体积可变的密闭容器中,加入
B ,发生反应: A ( s )
+ 2B ( g ) 4 C( g ) + D ( g );△H < 0 。在一定温度、压强下达到平衡。平衡时 C 的物质的量与加
4 C( g ) + D ( g );△H < 0 。在一定温度、压强下达到平衡。平衡时 C 的物质的量与加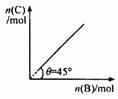 入的 B 的物质的量的变化关系如右图。下列说法正确的是
入的 B 的物质的量的变化关系如右图。下列说法正确的是
A.平衡时 B 的转化率为 50 %
B.若再加入 B ,则再次达到平衡时正、逆反应速率均增大
C.若保持压强一定,再加人 B ,则反应体系气体密度减小
D.若保持压强一定,当温度升高 10 ℃ 后,则图中 θ > 45°
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com