
题目列表(包括答案和解析)
2.分类方法在化学学科的发展中起到了非常重要的作用。下列分类标准合理的是
①根据酸分子中含有的氢原子数将酸分为一元酸、二元酸等,②根据反应中是否有电子转移将化学反应分为氧化还原反应和非氧化还原反应,③根据分散系是否具有丁达尔现象将分散系分为溶液、胶体和浊液,④根据反应中的热效应将化学反应分为放热反应和吸热反应。
A.①③ B.②④ C.①②④ D.②③④
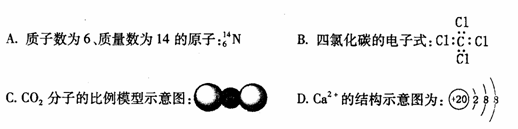
1.下列叙述正确的是
30、 (14分)、下图表示A-H之间的转化关系。已知E无支链,E、G均可使溴的四氯化碳溶液褪色, 1molA、B、E、H均可与2molNaHCO3反应。
(14分)、下图表示A-H之间的转化关系。已知E无支链,E、G均可使溴的四氯化碳溶液褪色, 1molA、B、E、H均可与2molNaHCO3反应。
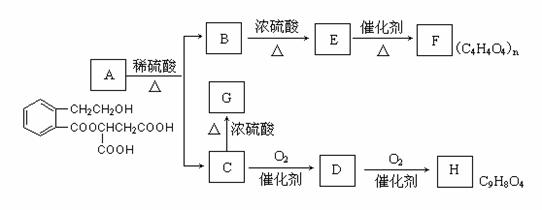
回答下列问题:
(1)A、B、C中所含相同官能团的名称为 ,C→G的反应类型为 。
(2)F、H的结构简式分别为
(3)写出下列反应的化学方程式:
B→E: ,
C→D: 。
(4)写出与C互为同分异构体且满足下列条件的物质的结构简式:
①与氯化铁溶液发生显色反应 ②苯环上有2个邻位取代基
③能发生银镜反应 ④能发生水解反应
。
29.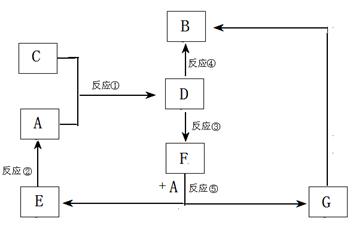 (16分)、A、B、C、D、E、F、G七种物质间存在如图所示的转化关系,其中A、B、D、G含有同种元素。
(16分)、A、B、C、D、E、F、G七种物质间存在如图所示的转化关系,其中A、B、D、G含有同种元素。
已知:(Ⅰ)A为金属单质; B为红褐色固体;E为密度最小的气体;G为浅绿色溶液。
(Ⅱ)D为黄色溶液,能与硝酸银溶液反应生成不溶于稀硝酸的白色沉淀。
(Ⅲ)D能将某种氧化物氧化为F,F是含有三种元素的化合物。
请回答下列问题:
(1)上述反应中属于置换反应的是 (填序号)。
(2)G生成B有多种途径。若在G的溶液中加入与G等物质的量的Na2O2,恰好使G转化为B,写出该反应的离子方程式:
反应③(即D将某种氧化物氧化为F)的离子方程式
(3)D的水溶液显酸性,请用离子方程式解释原因
(4)实验室制取C的化学方程式为
对气体C进行如下实验。已知整个反应过程中,每消耗0.1mol KI,转移的电子数约为3.612×1023 个。请按照要求填空:
|
实验步骤 |
实验现象 |
用化学用语解释 |
|
将少量气体通入淀粉KI溶液 |
溶液最初变成 色 |
(用离子方程式表示) |
|
继续通入气体 |
溶液逐渐变成无色 |
(用化学方程式表示) |
28.(14分)为测定含有Na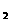 O杂质的Na
O杂质的Na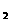 O
O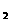 样品的纯度,甲、乙、丙三位同学设计了不同的方案。
样品的纯度,甲、乙、丙三位同学设计了不同的方案。
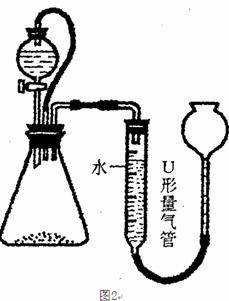
甲:用图l所示装置,通过测定Na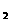 O
O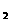 与C0
与C0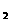 反应生成0
反应生成0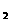 的体积来测定样品的纯度。
的体积来测定样品的纯度。
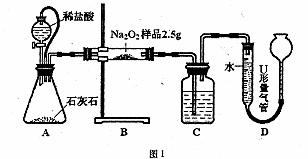
(1)C中所盛的药品是
(2)A中橡皮管的作用是
(3)利用该实验方案所测Na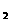 O
O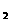 的纯度明显偏大,其原因可能是 (填选项字母)。
的纯度明显偏大,其原因可能是 (填选项字母)。
a.装置A、B中的空气对测定结果产生了影响
b.装置C中的空气对测定结果产生了影响
c.读数时U形量气管中的液面左高右低
d.读数时U形量气管中的液面左低右高
乙、丙两同学在研究Na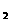 O
O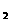 与水反应的实验时,观察到以下实验现象:Na
与水反应的实验时,观察到以下实验现象:Na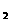 O
O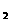 与水反应,放出大量的热,产生大量气体;反应后的溶液中滴入几滴酚酞,溶液先变红,振荡后又褪色;再往溶液中加入少许Mn02:粉末,又产生大量气体;当不再产生气体时,再滴加几滴酚酞,溶液又变红,且振荡后不褪色。分析了这些实验现象后,他们分别设计了如下方案。
与水反应,放出大量的热,产生大量气体;反应后的溶液中滴入几滴酚酞,溶液先变红,振荡后又褪色;再往溶液中加入少许Mn02:粉末,又产生大量气体;当不再产生气体时,再滴加几滴酚酞,溶液又变红,且振荡后不褪色。分析了这些实验现象后,他们分别设计了如下方案。
乙:用图2所示装置,称取2.5 g样品,测得与水反应生成氧气的体积为112 mL(标准状况),然后将溶液先用硫酸中和,再用0.2 mol/L KMn0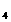 酸性溶液滴定,消耗KMn0
酸性溶液滴定,消耗KMn0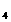 酸性溶液30
mL
酸性溶液30
mL
(已知:滴定过程中生成了Mn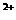 和氧气)。
和氧气)。
(4)滴定过程中发生反应的离子方程式为
(5)滴定终点的颜色变化为
(6)计算Na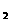 O
O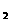 样品的纯度是:
样品的纯度是:
27.(15分)如图所示,A、G、I均为单质,其中A、G为金属且都常被用作输电线,且G单质有特殊颜色,B为黑色粉末,L是由两种元素组成的盐,它是家庭厨房必备物品。请回答:
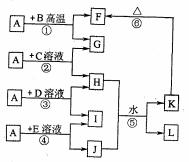
(1)L的电子式为
(2)指出F在工业上的一种用途
(3)反应②的离子方程式为
(4)若利用反应④设计成原电池,其负极反应式为
(5)除反应⑤外,还有多种化学反应可由H生成K。下列物质能与H反应生成K的是
(填选项字母)
a.CO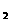 b.NaHCO
b.NaHCO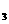 c.NaHSO
c.NaHSO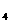 d.NaClO e.NH
d.NaClO e.NH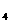 NO
NO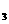 f.NH
f.NH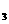 ·H
·H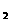 O
O
(6)反应①中,当有4.0g B参加反应时,放出的热量为20.1kJ,则该反应的热化学方程式为
13.下列叙述正确的是( )
A.将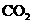 通入
通入 溶液中至饱和,无沉淀产生;再通入
溶液中至饱和,无沉淀产生;再通入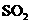 ,产生沉淀
,产生沉淀
B.在稀硫酸中加入铜粉,铜粉不溶解;再加入NaNO3固体,铜粉仍不溶
C.向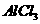 溶液中滴加氨水,产生白色沉淀;再加入过量
溶液中滴加氨水,产生白色沉淀;再加入过量 溶液,沉淀消失
溶液,沉淀消失
D.纯锌与稀硫酸反应产生氢气的速率较慢;再加入少量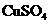 固体,速率不改变
固体,速率不改变
第Ⅱ卷 非选择题(共174分)
12.以下是分离乙酸乙酯、乙酸、乙醇的混合物的流程图,图中圆括号内填入适当的试剂,方括号内填入适当的分离方法,方框内是有关物质的名称。下列说法正确的是( )
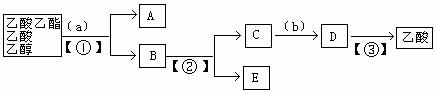
A.a为NaOH溶液,①为蒸馏 B.②、 ③均为蒸馏,①为分液
C.②为分液,C中含有醋酸钠 D.b可以是硫酸,也可以是盐酸
11.已知下列热化学方程式:
(1)CH3COOH(l)+2O2(g) === 2CO2(g)+2H2O(l) △H1= -870.3 kJ·mol-1
(2)C(s)+O2(g) === CO2(g) △H2= -393.5 kJ·mol-1
(3)H2(g)+O2(g) === H2O(l) △H3= -285.8 kJ·mol-1
则反应2C(s)+2H2(g)+O2(g)===CH3COOH(l) 的△H为( )kJ·mol-1
A.+488.3 B.-244.15 C.-488.3 D. +244.15
10、下列比较中,正确的是( )
A.同温度同物质的量浓度时,HF比HCN易电离,则NaF溶液的pH比NaCN溶液大
B.0.2
mol ·L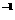 NH4Cl和0.1
mol·L
NH4Cl和0.1
mol·L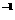 NaOH溶液等体积混合后:
NaOH溶液等体积混合后:
c(NH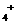 )>c(Cl
)>c(Cl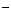 )>c(Na
)>c(Na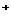 )>c(OH
)>c(OH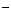 )>c(H
)>c(H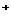 )
)
C.物质的量浓度相等的H2S和NaHS混合溶液中:
c(Na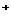 )+c(H
)+c(H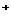 )=c(S
)=c(S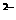 )+c(HS
)+c(HS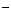 )+c(OH
)+c(OH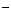 )
)
D.同浓度的下列溶液中,①NH4Al(SO4)2、②NH4Cl、③CH3COONH4、④NH3·H2O;c(NH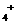 )由大到小的顺序是:①>②>③>④
)由大到小的顺序是:①>②>③>④
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com