
题目列表(包括答案和解析)
16. 下列溶液中各微粒的浓度关系正确的是
A. 0.2 mol/L的CH3COOH溶液与0.1 mol/L CH3COOH溶液中c(H+)之比为2:1
B. 0.1 mol/L NaHCO3溶液中,c(Na+) = 2c(CO32-) + c(HCO3-) + c(H2CO3)
C. 0.1 mol/L 的NaHA溶液,其pH = 4,则c(HA-)> c(A2-)> c(H2A)
D. 只含Na+、CH3COO-、H+、OH-的酸性溶液中,c(H+)>c(CH3COO-)>c(Na+)>c(OH-)
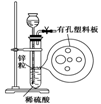
15. 右图为实验室制氢气的简易装置。若在加稀硫酸时,发现锌粒与稀硫酸没有接触而稀硫酸
|
不够了,为使该反应顺利进行,可以从长颈漏斗中加入的试剂是 ①食盐水 ②KNO3溶液 ③适量稀硫酸铜溶液 ④Na2CO3溶液 ⑤CCl4 ⑥浓氨水 A. ①③⑤ B. ①②③ C. ④⑤⑥ D. ①②③⑤ |
 |
14. 下列有关物质性质、结构的表述均正确,且存在因果关系的是
|
|
表述1 |
表述2 |
|
A. |
钠的金属性比铝强 |
钠原子核外电子数比铝少 |
|
B. |
金刚石的熔点高于晶体硅 |
原子半径Si大于C,键能Si-Si小于C-C |
|
C. |
离子晶体一般硬度较大,难压缩 |
离子晶体中阴、阳离子排列很有规律 |
|
D. |
相同条件下,分别完全燃烧等量的正丁烷和异丁烷,放出的热量相同 |
正丁烷与异丁烷互为同分异构体 |
13. 食品香精菠萝酯的生产路线(反应条件略去)如下:
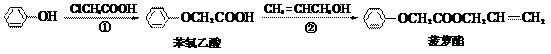 下列叙述错误的是
下列叙述错误的是
A. 步骤①产物中残留的苯酚可用FeCl3溶液检验
B. 步骤②产物中残留的CH2=CHCH2OH可用溴水检验
C. 苯酚和菠萝酯均可与酸性KMnO4溶液发生反应
D. 苯氧乙酸和菠萝酯均可与H2在一定条件下发生反应
12. NA代表阿伏加德罗常数,下列有关叙述正确的是
A. 1mol苯分子中含有碳碳双键数为3NA B. 1mol氯化氢分子中含H+ 离子数为NA
C. 16 g CH4与18 g NH4+ 所含质子数均为NA D. 4.6 g钠与盐酸完全反应失去电子数为0.2NA
11. 根据下表信息,判断0.10mol/L的下列各溶液pH值最大的是
|
A. CH3COONa B. Na2CO3 C. Na2S D. Na3PO4 |
|
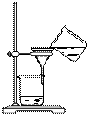
10. 从海带中提取碘的实验过程中,涉及到下列操作,其中正确的是
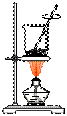 |
 |
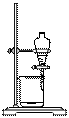 |
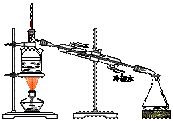 |
|
A. 海带灼烧成灰 B. 过滤得含I-溶液 C. 放出碘的苯溶液 D. 分离碘并回收苯 |
9. 下图装置中,小试管内为红墨水,具支试管内盛有pH=4的雨水和生铁片。观察:开始导管内液面下降,一段时间后导管内液面回升,略高于小试管液面。以下有关解释合理的是
|
A. 生铁片中的碳是原电池的阳极,发生还原反应 B. 雨水酸性较强,生铁片仅发生析氢腐蚀 C. 墨水回升时,碳极反应式为:O2 + 2H2O + 4e → 4OH- D. 具支试管中溶液pH逐渐减小 |
 |
8. 下列各组物质由于浓度不同而能发生不同氧化还原反应的是
①Cu与HNO3溶液;②NaOH与AlCl3溶液;③Zn与H2SO4溶液;④Na与O2反应
A. ①③ B. ①② C. ③④ D. ①④
7. 下列事实不能用勒夏特列原理解释的是
A.打开啤酒瓶盖,产生大量气泡
B.氢气与碘蒸气的平衡体系,加压后颜色加深
C.制取乙酸丁酯时,加入过量的乙酸
D.配制氯化铁溶液时,加入少量盐酸
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com