
̀âÄ¿Áбí(°üÀ¨´đ°¸ºÍ½âÎö)
28.(15·Ö) ̉ÑÖª£º
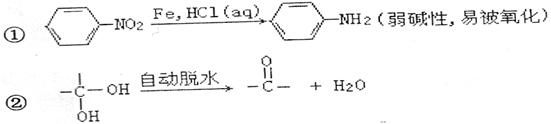
¹¤̉µÉÏ̉Ô±½ºÍC8H602Br2(ÏÔËáĐÔ¡µÎªÔÁϺϳÉ̉»ÖÖ²úÉúµçÄܵÄĐÂĐÍKEVLARºÏ³ÉÏËά£¬Éú²úÁ÷³̀Ϊ£º
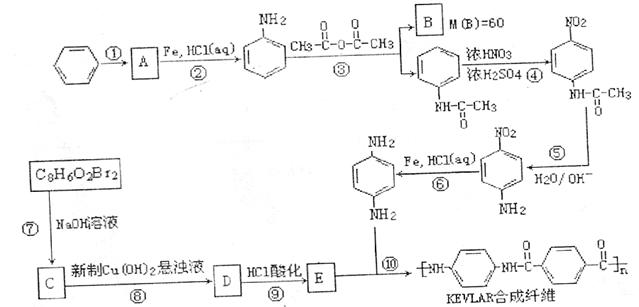
27. (16·Ö)
ÓĐÁ½ÖÖλÓÚ¶̀ÖÜÆÚµÄÏàÁÚÖÜÆÚ¡¢ÏàÁÚÖ÷×åµÄ·Ç½đÊôÔªËØX¡¢Y¡£̉ÑÖªÁ½ÔªËØ×î¸ß¼ÛÑơ»¯ÎïµÄË®»¯Îï¾ùΪǿËá¸ù¾ƯÏÂͼת»¯¹Øϵ(·´Ó¦̀ơ¼₫¼°²¿·Ö²úÎZÂÔÈ¥)£¬»Ø´đÏÂÁĐÎỀâ:
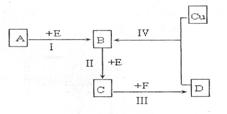
(1)ÈôA¡¢B¡¢C¡¢D¾ùΪº¬XÔªËصĻ¯ºÏÎÇ̉AµÄ̉»¸ö·Ö×ÓÖĐÖ»º¬ÓĐ10¸öµç×Ó£¬Ộ:
¢ÙAµÄ·Ö×Ó¹¹ĐÍΪ¡¡¡¡¡¡¡¡¡¡¡¡¡¡
¢Ú·´Ó¦IµÄ»¯Ñ§·½³̀ʽΪ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
¢Û»¯ºÏÎïNaX3ÊǺϳÉ"´ï·Æ"µÄÖĐ¼ä»îĐÔÎïÖÊ£¬ NaX3ÊÜײ»÷ºóÉú³ÉNa3XºÍÁí̉»ÖÖÆø̀åµ¥ÖÊ
ÇëĐ´³ö¸Ă·´Ó¦µÄ»¯Ñ§·½³̀ʽ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡¡¡¡¡¡
(2)ÈôA¡¢B¡¢C¡¢D¾ùΪº¬YÔªËصĻ¯ºÏÎÇ̉AµÄĦ¶ûÖÊÁ¿Îª120 g-mol-1£¬Ộ:
¢Ù·´Ó¦¢ôµÄÈÜ̉º¼ÓÈÈƠô¸ÉËùµĂµÄ¾§̀åÊôÓÚ¡¡¡¡¡¡¡¡¡¡¡¡ ¾§̀å(̀î"Àë×Ó"¡¢"·Ö×Ó"¡¢"Ô×Ó").
¢Ú·´Ó¦IµÄ»¯Ñ§·½³̀ʽΪ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
¢ÛÈô×ÆÉƠ6gA²úÉúµÄB(Æø̀¬)È«²¿×ª»¯ÎªC(Æø̀¬)ʱ·Å³ö9.83 KJÈÈÁ¿£¬ÇëĐ´µÚ¢̣²½·´Ó¦µÄÈÈ»¯Ñ§·½³̀ʽ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
26.(1) H202µÄË®Âå̉ºÎª¶₫ÔªÈơËᣬ¿Æѧ¼̉¶ÔH202½á¹¹µÄÈÏʶ¾ÀúÁ˽ÏΪÂ₫³¤µÄ¹ư³̀£¬×î³ơËûĂÇ̀á³öÁËÁ½ÖÖ ¹Ûµă:¡¡ a. 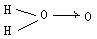 ¡¡(ʽÖĐ0¡ú0±íʾ¹²Óõç×Ó¶ÔÓÉÇ°̉»¸öÑơÔ×Ó̀ṩ¡µºÍb.
¡¡(ʽÖĐ0¡ú0±íʾ¹²Óõç×Ó¶ÔÓÉÇ°̉»¸öÑơÔ×Ó̀ṩ¡µºÍb. 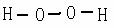 ¡¡¡¡
¡¡¡¡
¢ÙÇëÓõç×Óʽ±íʾbµÄ½á¹¹
¢ÚĐ´³öH202ÔÚË®ÈÜ̉ºÖеĵçÀë·½³̀ʽ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
(2)¢ÙÓõ¥ÖʵâºÍÂÈËá¼Ø¿É̉ÔÖÆµĂµâËá¼Ø£¬ÆäÖĐÉæ¼°µÄ̉»¸ö·´Ó¦Îª:
¡¡¡¡ I2+KCl03+H2O¡úKH(IO3)2+KCl+Cl2¡ü.̣̉´ËÓĐÈËÈÏΪI2µÄÑơ»¯ĐÔÇ¿ÓÚÂÈÆø£¬Äă¡¡¡¡¡¡¡¡ (̀î "ͬ̉â"»̣"²»Í¬̉⣬£¬)¸Ă¹Ûµă£¬ÀíÓÉÊÇ¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
¢ÚÓĂµç»¯Ñ§·½·¨̉²¿É̉ÔÖƵâËá¼Ø.ÔÀíÊÇ̉ÔʯīΪÑô¼«£¬²»Đâ¸ÖΪ̉ơ¼«£¬̉Ե⻯¼ØéÅ̉ºÎªµç½âÖÊÈÜ̉º£¬ÔÚ ̉»¶¨µçÁ÷ºÍζÈϽøĐеç½â¡´Í¬Ê±²»¶Ï½Á°èµç½âÖÊÈÜ̉º¡µÆäµç½â×Ü·´Ó¦Ê½Îª:
̉»¶¨µçÁ÷ºÍζÈϽøĐеç½â¡´Í¬Ê±²»¶Ï½Á°èµç½âÖÊÈÜ̉º¡µÆäµç½â×Ü·´Ó¦Ê½Îª:
KI+3H20¡¡¡¡¡¡¡¡ KI03+3H2¡ü¡¡ ³öÑô¼«µÄµç¼«·´Ó¦Ê½¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
13.ÓĐ100mlMgCl2ºÍAlCl3µÄ»́ºÏÈÜ̉º£¬ÆäÖĐc(Mg2+)Ϊ0.2mol/L£¬c(Cl-)Ϊ1.3mol/L£¬̉ªÊ¹Mg2+ת»¯Îª³Áµí·ÖÀë³öÀ´£¬ÖÁÉÙĐè¼Ó2mol/LNaOHÈÜ̉º̀å»ưÊÇ
A. 40mL ¡¡¡¡¡¡¡¡B. 60mL ¡¡¡¡ ¡¡¡¡¡¡C. 80mL ¡¡ ¡¡¡¡¡¡D. 120mL
12.ÏÂÁĐ˵·¨ƠưÈ·µÄÊÇ
A.Na+¡¢Fe3+¡¢Cl-¡¢SCN-ÄÜ´óÁ¿¹²´æÓÚͬ̉»ÈÜ̉ºÖĐ ¡¡¡¡
B.̀¼ËáÇâÄÆÈÜ̉ºÓë×ăÁ¿µÄÇâÑơ»¯±µÈÜ̉º»́ºÏºó£¬ÆäÀë×Ó·½³̀ʽΪ: HC03- + Ba2++OH£½BaC03¡ư+H2O
C.ÈôR2-ºÍM+µÄµç×Ó²ă½á¹¹Ïàͬ£¬ỘÔ×ÓĐ̣ÊưµÄ±È½ÏΪ: R>M
D.ÈôXÔ×ÓÖеÄÖÊ×ÓÊưΪa£¬ÖĐ×ÓÊưΪb£¬ỘXµÄÖÊÁ¿ÊưΪ: a-b
11.º£ÄϵĶ¾ôø¶¹¡¢¶¾»Æ¹ÏµÈ¶¾Êß²ËÖĐº¬ÓĐ½ûÓĂÅ©̉©Ë®°·Ạ́Á×£¬Ë®°·Ạ́Á׵Ľṹ¼̣ʽÈç̀â11ͼËùʾ:¶Ô¸Ă»¯ºÏÎïµÄÏÂÁĐĐđÊöƠưÈ·µÄÊÇ ¡¡
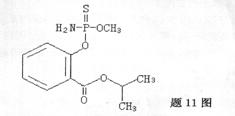
A.¸Ă»¯ºÏÎïÊôÓÚ·¼Ïằ₫ ¡¡ ¡¡
B.¸Ă»¯ºÏÎïµÄ·Ö×ÓʽΪC11H14NPS ¡¡
C¸Ă»¯ºÏÎïÄÜ·¢Éú¼Ó¾Û·´Ó¦¡¢Ë®½â·´Ó¦ºÍ´×»¯·´Ó¦
D.¸Ă»¯ºÏÎïÖĐÖÁÉÙÓĐ7¸ö̀¼Ô×ÓÔÚͬ̉»Æ½Ăæ¡¡
10. ¼ºÖª·´Ó¦ mA(g) + nB(g)¡¡¡¡¡¡ qC(g)µÄƠư·´Ó¦ÎªÎüÈÈ·´Ó¦£¬ m+n£¼q£¬ÔÚºăÈƯĂܱƠÈƯÆ÷ÖĐ·´Ó¦´ïµ½Æ½ºâʱ£¬ ÏÂÁĐ˵·¨ƠưÈ·µÄÊÇ
¼ºÖª·´Ó¦ mA(g) + nB(g)¡¡¡¡¡¡ qC(g)µÄƠư·´Ó¦ÎªÎüÈÈ·´Ó¦£¬ m+n£¼q£¬ÔÚºăÈƯĂܱƠÈƯÆ÷ÖĐ·´Ó¦´ïµ½Æ½ºâʱ£¬ ÏÂÁĐ˵·¨ƠưÈ·µÄÊÇ
A. AµÄƠư·´Ó¦ËÙÂÊÊÇBµÄÄæ·´Ó¦ËÙÂ浀 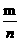 ¡¡±¶¡¡
¡¡±¶¡¡
B.ͨÈëÏ¡ÓĐÆø̀åʹѹǿÔö´ó£¬Æ½ºâ½«ÄæỊ̈̉ƶ¯
C.ÈôƽºâʱA¡¢BµÄת»¯ÂÊÏàµÈ£¬ËµĂ÷·´Ó¦¿ªÊ¼Ê±A¡¢BµÄÎïÖʵÄÁ¿Ö®±ÈΪn:m
D.Éư¸ßζȣ¬»́ºÏÆø̀åµÄƽ¾ùÏà¶Ô·Ö×ÓÖÊÁ¿±ä´ó
9. Èç̀â9ͼÈøʾµÄʵÑéÖĐ£¬ÄܴﵽʵÑéÄ¿µÄµÄÊÇ
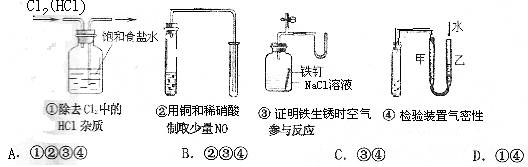
8. ÏÂÁĐ˵·¨²»ƠưÈ·µÄÊÇ
A. NaClºÍSiO2¾§̀åÈÛ»¯Ê±£¬¿Ë·₫Á£×Ó¼ä×÷ÓĂÁ¦µÄÀàĐͲ»Ïàͬ
B.½«ÉƠºÚµÄÍË¿É́Èë¾Æ¾«µÆ»đÑæµÄÑæĐÄÓÖ±äº́É«¹âÁÁ
C.ÂÈ»¯ÑÇ̀úÈÜ̉º³¤ÆÚÉ¢·ÅÓÚ¿ƠÆøÖĐ»ạ́̉±»Ñơ»¯¶ø³Ê»ÆÉ«
D.ỂÎÂÏÂ.ijÈÜ̉ºÖĐÓÉË®µçÀë³öµÄc(H+)=10-6mol.L -I£¬Ộ´ËÈÜ̉º¿ÉÄÜÊÇÏ¡Ạ́Ëá
7.ÏÂÁи÷Ñ¡ÏîËùÊöµÄÁ½¸öÁ¿£¬Ç°Ơß̉»¶¨´óÓÚºóƠßµÄÊÇ
A.ͬÎÂÏ·ֱđÔÚ100gË®ÖĐ×î¶àÄÜÈܽâµÄÎ̃Ë®CuS04ºÍCuS04¡¤5H2OµÄÖÊÁ¿
B.´¿Ë®ÔÚ25¡æºÍ90¡æʱµÄpHÖµ
C. 25¡æʱ£¬µÈ̀å»ưµÄpH¶¼µÈ3µÄÑÎËáºÍAlCl3ÈÜ̉ºÖĐ£¬¼ºµçÀëµÄË®·Ö×ÓÊư
D.ÔÚ·´Ó¦NH3+NO¡úN2+H2OÖĐ£¬±»Ñơ»¯ºÍ±»»¹ÔµÄNÔ×ÓÊư
¹ú¼ÊÑ§Đ£ÓÅÑ¡ - Á·Ï°²áÁбí - ÊỒâÁбí
º₫±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨Æ½̀¨ | ÍøÉÏÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | µçĐÅƠ©Æ¾Ù±¨×¨Çø | ÉæÀúÊ·ĐéÎ̃Ö÷̉åÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com