
题目列表(包括答案和解析)
25.已知A、B、C、D、E均为中学化学中常见物质,在一定条件下相互转化关系如下图所示(反应条件和部分产物已省略)。

请回答:
(1)若A为金属单质,B、C为非金属单质,且常温下B、C均为无色气体,D为黑色固体,则B的化学式为 ,A与E在一定条件下反应生成D的化学方程式为
。
(2)若A为非金属单质,且常温下为黄绿色气体,B为金属单质,C为酸,且C的组成中含有与A相同的元素。则构成非金属单质A的元素原子结构示意图为 ,C的化学式为 ,A与E在一定条件下反应生成D的离子方程式为
。
24.为探究 Na、Mg、Al的金属活动性顺序,某课外小组同学进行了如下实验:
|
实 验 |
1.将一小块金属钠放入滴有酚酞溶液的冷水中。 2.将一小段用砂纸打磨后的镁带放入试管中,加入少量水,加热至水沸腾,冷却后,向试管中滴加酚酞溶液。 3.将一小段镁带投入稀盐酸中。 4.将一小片铝投入稀盐酸中。 |
他们记录的实验现象有:
|
实验现象 |
①剧烈反应,迅速生成大量的气体。 ②浮在水面上,熔成小球,不断游动,小球渐小最终消失,溶液变红。 ③反应不剧烈,产生无色气体。 ④有气体产生,溶液变成红色。 |
请帮助该小组同学补充下列实验报告中的内容:
(1)在下表中填写与实验相对应的实验现象序号:
|
实 验 |
1 |
2 |
3 |
4 |
|
实验现象 |
|
|
|
|
(2)写出钠与水反应的化学方程式 。
(3)实验结论是 。
答案:(1)
|
实 验 |
1 |
2 |
3 |
4 |
|
实验现象 |
② |
④ |
① |
③ |
(2)2 Na + 2 H2O == 2 NaOH + H2↑
(3)金属活动性顺序为 Na > Mg > Al
23.某实验小组同学在配制100 mL 0.1 mol/L的Na2CO3溶液时,进行的实验操作有:
① 将称量好的Na2CO3固体放入小烧杯中,加适量蒸馏水溶解。为加速溶解,可用
(填仪器名称)搅拌。
② 将①所得溶液冷却到室温后,小心转入 (填仪器名称)中。
③ 继续加蒸馏水至液面距刻度线1-2 cm处,改用 (填仪器名称),小心滴加蒸馏水至溶液凹液面最低点与刻度线相切。
④ 用少量蒸馏水洗涤烧杯和玻璃棒2-3次,每次洗涤的液体都要小心转入容量瓶,并轻轻摇匀。
⑤ 将容量瓶瓶塞塞紧,充分摇匀。
请回答:
(1)正确的实验操作顺序为 (填序号)。
(2)所配溶液中Na+ 物质的量浓度是 。
(3)取出20 mL配制好的溶液,此溶液中Na2CO3的物质的量浓度为 。
答案: ①玻璃棒 ②100mL容量瓶 ③胶头滴管
(1)①②④③⑤ (2)0.2 mol/L (3)0.1 mol/L
22.在两支分别盛有Al(OH)3的试管中,向其中一支中滴加足量盐酸,观察到的现象是 ,发生反应的离子方程式为 ;向另一支中滴加足量NaOH溶液,观察到的现象是 ,发生反应的离子方程式为 。由此说明Al(OH)3是一种 氢氧化物。
21.为除去下列各种物质中的少量杂质,选择除杂试剂填写在下表中:
|
物质 |
杂质 |
除杂试剂 |
|
Na2SO4 |
Na2CO3 |
|
|
FeCl2 |
CuCl2 |
|
|
Fe |
Al |
|
20. 粗盐水经过滤后仍含有少量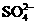 、
、 、
、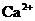 等杂质离子。为除掉这些杂质离子,常采用以下实验步骤:
等杂质离子。为除掉这些杂质离子,常采用以下实验步骤:
①加入过量BaCl2溶液,沉淀后,过滤;
②在步骤①所得滤液中加入过量NaOH溶液,沉淀后,过滤;
③在步骤②所得滤液中加入过量碳酸钠溶液,沉淀后,过滤;
④在步骤③所得滤液中加入适量盐酸,即可得到纯净的NaCl溶液。
请回答:
(1)步骤①中加入BaCl2溶液必须过量,其目的是 ,发生反应的离子方程式为 。
(2)步骤③发生反应的离子方程式为 、
。
19.在工农业生产和日常生活中经常用到下列物质:①Si、②(NH4)2SO4、③Ca(ClO)2、④Al(OH)3、⑤ Fe2O3 。其中,可用于制造硅芯片的是 (填序号,下同);可用于杀菌、消毒的是 ;可用作化肥的是 ;可用作红色油漆和涂料的是 ;医疗上可用作胃酸中和剂的是 。
18.铜与浓硫酸发生反应的化学方程式为:Cu + 2 H2SO4(浓) △ CuSO4+ SO2↑ + 2 H2O,其中铜元素的化合价 (填“升高”或“降低”),被 (填“氧化”或“还原”,下同);浓H2SO4作 剂,具有 性。在该反应中,若消耗了1 mol Cu,则生成 mol SO2 。
17.氨是一种重要的化工产品,通常是 色、 具有 气味的气体,密度比空气的 (填“大”或“小”), (填“易”或“难”)溶于水。实验室收集氨气应采用 法,制取氨气的化学方程式为
。
21.已知: 与

“智能型”高分子,在生物工程中有广泛的应用前景。PMAA就是一种“智能型”高分子,可应用于生物制药中大分子和小分子的分离。下列是以物质A为起始反应物合成PMAA的路线:
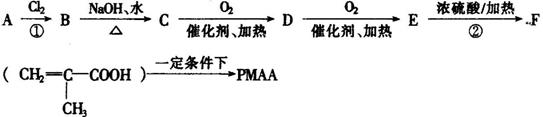
根据上述过程回答下列问题:
(1)分别写出A和PMAA的结构简式:A ,PMAA 。
(2)上述过程中①、②反应类型分别是:① 、② 。
(3)分别写出C→D和E→F的化学方程式:w.w.^w.k.&s.5*高.考.资.源.网
C→D: ;
E→F: 。
(4)E在有浓硫酸和加热的条件下,除了能生成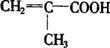 外还可能生成一种具有六元环的产物(用结构简式表示):
外还可能生成一种具有六元环的产物(用结构简式表示):
w.w.^w.k.&s.5*高.考.资.源.网
。
w.w.^w.k.&s.5*高.考.资.源.网
w.w.^w.k.&s.5*
高.考.资.源.网
高☆考♂资♀源?网

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com