
题目列表(包括答案和解析)
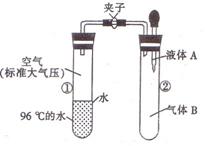
13、如图所示,夹子开始处于关闭状态,将液体A滴人
试管②与气体B充分反应,打开夹子,可发现试管①内
的水立刻沸腾了。则液体A和气体B的组合不可能是
下列的
A.氢氧化钠溶液.二氧化碳 B.水.氨气
C.氢氧化钠溶液.一氧化氮 D.水.二氧化氮
12.常温下,测得某无色溶液中由水电离出的C(H+)=1×10-13mol·L-1,则该溶液中一定能共存的离子组是
A.AlO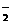 、NO
、NO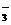 、Na+、Cl- B.Mg2+、SO
、Na+、Cl- B.Mg2+、SO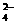 、Na+、CIO-
、Na+、CIO-
 C.Fe3+、NO3-、K+、SO
C.Fe3+、NO3-、K+、SO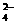 D.Ba2+、K+、NO
D.Ba2+、K+、NO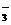 、Cl-
、Cl-
11.将S02通入Fe(NO3)3溶液中,溶液由棕黄色变为浅绿色,但立即又变为棕黄色;继续滴人BaC12 溶液,产生白色沉淀。在上述一系列变化过程中,最终被还原的是
A . S02 B . Cl- C . Fe3+ D . N03-
10.右图表示在某溶液中滴加Ba(OH)2溶液时,沉淀的
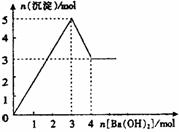 物质的量随Ba(OH)2的物质的量的变化关系。该
物质的量随Ba(OH)2的物质的量的变化关系。该
溶液的成分可能是
A、MgSO4 B、KAl(SO4)2
C、Al2(SO4)3 D、NaAlO2
9.水热法制备Fe3O4纳米颗粒的反应是3Fe2++2S2O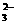 +O2+xOH-
+O2+xOH- Fe3O4+S4O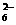 +2H2O,下列说法中,正确的是:
+2H2O,下列说法中,正确的是:
A.每生成1mol
Fe3O4,反应转移的电子总数为3mol B.Fe2+和S2O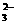 都是还原剂
都是还原剂
C.1mol Fe2+被氧化时,被Fe2+还原的O2的物质的量为1/3mol D.x=2
8.下列除去杂质的方法正确的是
A.除去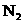 中的少量
中的少量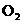 :通过灼热的CuO粉末,收集气体
:通过灼热的CuO粉末,收集气体
B.除去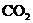 中的少量HCl:通入
中的少量HCl:通入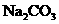 溶液,收集气体
溶液,收集气体
C.除去 溶液中的少量
溶液中的少量 :加入足量铁屑,充分反应后,过滤
:加入足量铁屑,充分反应后,过滤
D.除去KCl溶液中的少量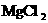 :加入适量NaOH溶液,过滤
:加入适量NaOH溶液,过滤
7.下列离子方程式,正确的是
A.Ca(ClO)2溶液中通入少量SO2气体:
H2O +SO2 + Ca2+ + 2ClO- === CaSO3↓+ 2HClO
B.向NH4HCO3 溶液中加入足量Ba(OH)2溶液
NH4+ +HCO3- + 2OH- === H2O + CO32- + NH3·H2O
C.向FeCl2溶液中加足量溴水
2Fe2+ + Br2 === 2Fe3++ 2Br-
D.NaAlO2溶液中通入过量CO2
2AlO2- +CO2+3H2O===2Al(OH)3↓+CO32-
6.下列对有关实验的描述不正确的是
A.在浓氨水中加入生石灰可以制取少量的NH3
 B.用水就可以一次性鉴别溴苯、苯、乙酸三种物质
B.用水就可以一次性鉴别溴苯、苯、乙酸三种物质
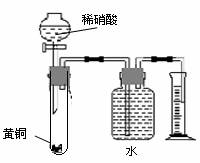
C.用如图所示的装置可以测定黄铜(Cu、Zn合金)中Zn的含量
D.除去粗盐中的Ca2+、Mg2+、SO42-,依次加入的物质可以是
H2O、 Ba(OH)2、Na2CO3、HCl
5.阿伏加德罗常数约为6.02×1023mol-1,下列叙述正确的是
A.标准状况下,22.4 L甲苯所含的分子数约为6.02×1023
B.14g乙烯和丙烯的混合物中,含有共用电子对数目为3×6.02×1023
C.0.1 L 3 mo1·L-1的NH4NO3溶液中含有的NH4+数目为0.3×6.02×1023
D.常温常压下,18.0 g重水(D2O)所含的电子数约为10×6.02×1023
4.右图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。据此下列说法正确的是
 A.该试剂的物质的量浓度为9.2 mol·L-1
A.该试剂的物质的量浓度为9.2 mol·L-1
B.该硫酸50 mL与足量的铜反应可得到标准状况下SO2 10.3 L
C.配制200 mL 4.6 mol·L-1的稀硫酸需取该硫酸50 mL
D.该硫酸与等体积的水混合所得溶液的质量分数小于49%
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com