
题目列表(包括答案和解析)
3、为了探究MnO2的催化效果,需要用30%的H2O2溶液(密度按1g/cm3)配制浓度为3%的H2O2溶液(密度按1g/cm3)100mL。配制过程中除了用到量筒、烧杯、100mL容量瓶外,还需用到的玻璃仪器名称是 ,需用量筒量取 mL30%的H2O2溶液。MnO2催化H2O2分解的化学方程式为 ,反应结束后将液体与MnO2分离的实验操作名称叫 。
2、该小组为研究在不同酸碱性的溶液中MnO2的氧化能力,他们控制KI溶液的浓度和MnO2固体的质量相同,恒定实验温度在298K,设计如下对比实验:
|
实验 |
外加试剂 |
现象 |
|
A |
1滴0.2mol/LNaOH溶液 |
不变色 |
|
B |
1滴水 |
缓慢变浅棕褐色 |
|
C |
1滴0.1mol/L硫酸 |
迅速变棕褐色 |
(1)该小组从上述对比实验中,可以得出的结论是 。
(2)写出在酸性条件下MnO2氧化I-的离子方程式 。
MnO2在酸性溶液中具有强氧化性,可被还原为Mn2+,它还对H2O2的分解具有良好的催化效果。某兴趣小组通过实验研究MnO2性质。
1、该小组设计了如下4个方案以验证MnO2的氧化性,可行的是 。
A.把MnO2固体加入到FeSO4溶液中,再加入KSCN溶液,观察溶液是否变红
B.把MnO2固体加入到FeCl3溶液中,再加入KSCN溶液,观察溶液是否变红
C.把MnO2固体加入到Na2SO3溶液中,再加入BaCl2溶液,观察是否有白色沉淀生成
D.把MnO2固体加入到稀盐酸中,观察是否有黄氯色气体生成
5、若向100mL盐A的溶液中加入10g金属单质B的粉末,充分搅拌后,过滤,烘干得10.16g固体,则滤液中溶质的物质的量浓度为 。(假设溶液体积不变)
4、电解100mL盐A的溶液一段时间后,断开电路,取出电极,测得所得到的气体D在标准状况下的体积为5.6mL,则电解后溶液的pH为 。(假设溶液体积不变)
3、E的稀溶液与F溶液反应的离子方程式为 。
2、A溶液与Na2O2反应的总化学方程式为 。
已知A为中学化学中的一种盐,B、C为日常生活中常见的金属。通常条件下D为无色无味气体,无色气体G遇空气变红棕色。已知用惰性电极电解A溶液一段时间后,产物只有C、D和E的稀溶液。各物质之间的转化关系如下图(部分反应产物已略去)。
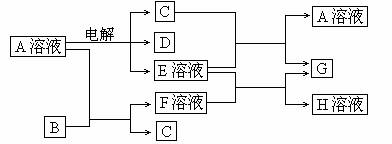
请回答下列问题:
1、A的化学式为 。
7、将17.9gAl、Fe、Cu组成的合金溶于足量的NaOH溶液中,产生气体3.36L(标准状况)。另取等质量的合金溶于过量的稀硝酸中,生成6.72L NO(标准状况,唯一还原产物),向反应后的溶液中加入过量的NaOH溶液,得到沉淀的质量为
A.33.2g B.25.4g C.22.4g D.19.6g
第Ⅱ卷 非选择题(共58分)
6、常温下,一定量的醋酸与氢氧化钠溶液发生中和反应。下列说法正确的是
A.当溶液中c(CH3COO-)=c(Na+)时,醋酸与氢氧化钠恰好完全反应
B.当溶液中c(CH3COO-)=c(Na+)时,一定是氢氧化钠过量
C.当溶液中c(CH3COO-)=c(Na+)>c(H+)=c(OH-)时,一定是醋酸过量
D.当溶液中c(Na+)>c(CH3COO-)>c(OH-)>c(H+)时,一定是氢氧化钠过量
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com