
题目列表(包括答案和解析)
8.X、Y、Z、W、R是5种短周期元素,其原子序数依次增大。X是周期表中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等。下列说法正确的是 ( )
A.元素Y、Z、W具有相同电子层结构的离子,其半径依次增大
B.元素Y、R分别与元素X形成的化合物的热稳定性:XmY>XmR
C.元素X不能与元素Y形成化合物X2Y2
D.元素W、R的最高价氧化物的水化物都是强酸
7.下列说法或表示方法正确的是 ( )
A.在稀溶液中,H+(aq)+ OH-(aq)= H2O(l) △H =-57.3 kJ·mol-1,若将含0.5 mol H2SO4的浓硫酸与含1 mol NaOH的溶液混合,放出的热大于57.3 kJ
B.由C(石墨)= C(金刚石) △H = +1.90 kJ/mol可知金刚石比石墨稳定
C.在200℃、101kPa时,1molH2与碘蒸气反应生成HI放热14.9kJ。该反应的热化学方程式为:H2(g)+I2(g)=2HI(g) △H =-14.9kJ/mol
D.在101 kPa时,2 g H2 完全燃烧生成液态水,放出285.8 kJ热量,表示氢气燃烧的热化学方程式表示为:2H2(g)+ O2(g)= 2H2O(l) △H =-285.8 kJ/mol
6.常温下已知两种一元弱酸HX和HY,如果向NaX溶液中通入CO2气体,只能生成HX和NaHCO3;向NaY溶液中通入CO2,则生成HY和Na2CO3。下列有关叙述正确的是
( )
A.酸性由强到弱:H2CO3>HX>HY
B.结合H+能力:CO32->Y->X->HCO3-
C.同浓度的NaX和 NaY溶液的pH前者大
D.向NaX溶液中通入足量CO2后的离子浓度:
c(X-)>c(Na+)>c(HCO3-)>c(OH-)
5.设阿伏加德罗常数的数值为NA ,下列说法正确的是 ( )
A.1 mL 1 mol·L-1 FeCl3溶液滴入沸腾的水中,所得胶体的粒子数为0.001NA
B.15.6g 过氧化钠与二氧化碳反应时,转移的电子数为0.4NA
C.常温常压下,46 g的NO2和N2O4混合气体含有的原子数为3NA
D.t℃时,pH =6 的纯水中,含10-6NA个OH-
4.某无色溶液中只可能含有Na+ 、Ba2 +、 Cl一、 Br一、SO32一、SO42一中的几种离子,对该溶液进行下列实验,实验操作和现象如下表:
|
步骤 |
操 作 |
现 象 |
|
(1) |
取少量溶液滴加几滴石蕊试液 |
溶液变蓝 |
|
(2) |
另取少量溶液滴加过量氯水,再加入CCl4振荡,静置 |
上层无色,下层呈橙红色 |
|
(3) |
取(2)上层溶液,加入过量Ba(NO3)2溶液和稀HNO3,过滤 |
有白色沉淀产生 |
|
(4) |
向(3)的滤液中加入过量AgNO3溶液和稀HNO3 |
有白色沉淀产生 |
下列结论正确的是 ( )
A.肯定含有 Na+、 Br一、SO32一 B.肯定没有 Ba2 +、Cl一、Br一
C.不能确定 Na+ 、 SO32一、SO42一 D.只含有 Cl一、 SO32一、SO42一
3.在陆地生态系统研究中,2H、13C、15N、18O、34S等常用做环境分析指示原子。下列说法中正确的是 ( )
A.32S与33S的核外电子数相等,是同一种核素
B.13C和15N原子核内的质子数相差2
C.1H216O和 1H218O均能与金属钠剧烈反应
D.2H+的酸性比1H+的酸性更强
2.下列说法正确的是 ( )
A.吸热反应只有在点燃或加热条件下才能发生
B.燃料电池总反应一定是氧化还原反应,且一定是可自发进行的吸热反应
C.一个吸热的自发进行的反应一定是墒增大的反应
D.向10mL 0.1mol/LAgNO3溶液中滴加足量的NaCl溶液能够使Ag+浓度降到0 mol/L
1.下列关于化学基本概念和基本理论的几点认识中正确的是 ( )
A.原子是化学变化中的最小微粒,通过复杂的化学反应可以产生新的原子
B.有电子转移的过程不一定产生电流,但其化学反应一定是氧化还原反应
C.胶体区别于其他分散系的本质特征是具有丁达尔现象
D.强电解质溶液的导电能力一定强于弱电解质溶液
2.可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Al 27 S 32 Cl 35.5 K 39 Fe 56
第I卷(选择题)
本卷包括14小题,每小题3分,共42分。在每题列出的四个选项中,只有一项是最符
合题目要求的
24、(9分)取等物质的量浓度的NaOH溶液两份A和B,每份50mL,向其中各通入一定量的CO2,然后各取溶液10mL,分别将其稀释为100mL,分别向稀释后的溶液中逐滴加入0.1mol/L的盐酸,标准状况下产生CO2气体体积与所加盐酸体积之间的关系如下图所示。
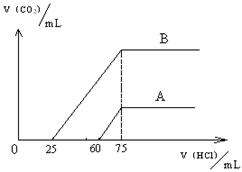
试回答下列问题:
(1)曲线A表明,原溶液中通入CO2后,所得溶液中的溶质为(写化学式) __________________,其物质的量之比为 ;加盐酸后产生CO2体积的最大值为 mL(不考虑CO2的溶解,下同)。
(2)曲线B表明,原溶液中通入CO2后,所得溶液中的溶质为(写化学式) _____________,其物质的量之比为 ;
(3)计算原NaOH溶液的物质的量浓度(写出计算过程)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com