
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
13ЃЎNAДњБэАЂЗќМгЕТТоГЃЪ§ЃЌЯТСаа№ЪіДэЮѓЕФЪЧ
A.10mLжЪСПЗжЪ§ЮЊ98%ЕФH2SO4ЃЌгУЫЎЯЁЪЭжС100mLЃЌH2SO4ЕФжЪСПЗжЪ§ЮЊ9.8%
BЃЎдкH2O2+Cl2=2HCl+O2ЗДгІжаЃЌУПЩњГЩ32gбѕЦјЃЌдђзЊвЦ2NAИіЕчзг
CЃЎБъзМзДПіЯТЃЌЗжзгЪ§ЮЊNAЕФCOЁЂC2H4ЛьКЯЦјЬхЬхЛ§дМ22.4LЃЌжЪСПЮЊ28g
DЃЎвЛЖЈЮТЖШЯТЃЌ1L 0.50 molЁЄL-1NH4ClШмвКгы2L 0.25molЁЄL-1NH4ClШмвККЌNH+4ИіЪ§ВЛЭЌ
12ЃЎЯТСаРызгЗНГЬЪНЪщаДе§ШЗЕФЪЧ
A.Й§СПЕФSO2ЭЈШыNaOHШмвКжаЃКSO2+2OH-ЃНSO2-3+H2O
BЃЎFe(NO3)3ШмвКжаМгШыЙ§СПЕФHIШмвКЃЛ2Fe3++2I-=2Fe2++I2
CЃЎNaNO2ШмвКжаМгШыЫсадKMnO4ШмвКЃК
2MnO-4+5NO-2+6H+ЃН2Mn2++5NO-3+3H2O
DЃЎNaHCO3ШмвКжаМгШыЙ§СПЕФBa(OH)2ШмвКЃК
ЁЁ2HCO-3+Ba2++2OH-=BaCO3Ё§+2H2O+CO2-3
11ЃЎЯТСаИїзщРызгвЛЖЈФмДѓСПЙВДцЕФЪЧ
A.КЌгаДѓСПFe3+ЕФШмвКжаЃКNH+4ЁЂNa+ЁЂCl-ЁЂSCN-
BЃЎдкЧПМюШмвКжаЃКNa+ЁЂK+ЁЂЃлAl(OH)4Ѓн-ЁЂCO2-3
CЃЎдкc(H+)=10-13molЁЄL-1ЕФШмвКжаЃКNH+4ЁЂAl3+ЁЂSO2-4ЁЂNO-3
DЃЎдкpH=1ЕФШмвКжаЃКK+ЁЂFe2+ЁЂCI-ЁЂNO-3
10ЃЎ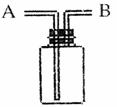 гУгвЭМЫљЪОзАжУНјааШчЯТЪЕбщЃЌВЛФмДяЕНЪЕбщФПЕФЕФЪЧ
гУгвЭМЫљЪОзАжУНјааШчЯТЪЕбщЃЌВЛФмДяЕНЪЕбщФПЕФЕФЪЧ
AЃЎЦПжаЪЂТњЫЎЃЌДгBПкНјЦјЃЌгУХХЫЎЗЈЪеМЏH2
BЃЎЦПжаЪЂЪЪСПХЈСђЫсЃЌДгAПкНјЦјРДИЩдяCO2
CЃЎДгBПкНјЦјЃЌгУХХПеЦјЗЈЪеМЏNO2
DЃЎЦПжазАТњЫЎЃЌAПкСЌЕМЙмВЂЩьШыСПЭВжаЃЌДгBПкНјЦјЃЌгУХХЫЎЗЈВтСПЩњГЩO2ЕФЬхЛ§
9ЃЎ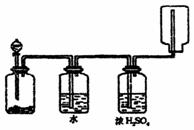 гвЭМзАжУПЩвдгУРДЗЂЩњЁЂЯДЕгЁЂИЩдяЁЂЪеМЏ(ВЛПМТЧЮВЦјДІРэ)ЦјЬхЃЌИУзАжУПЩгУгк
гвЭМзАжУПЩвдгУРДЗЂЩњЁЂЯДЕгЁЂИЩдяЁЂЪеМЏ(ВЛПМТЧЮВЦјДІРэ)ЦјЬхЃЌИУзАжУПЩгУгк
AЃЎЖўбѕЛЏУЬКЭЫЋбѕЫЎЗДгІЩњГЩбѕЦј
BЃЎХЈАБЫЎКЭЩњЪЏЛвЛьКЯЩњГЩАБЦј
CЃЎNa2SO3КЭХЈH2SO4ЛьКЯЩњГЩSO2
DЃЎаПСЃгыЯЁбЮЫсЛьКЯЩњГЩH2
8ЃЎ19.2gЭИњЪЪСПЕФХЈЯѕЫсЗДгІЃЌЭШЋВПзїгУКѓЃЌЙВЪеМЏЕНЦјЬх11.2 L(БъзМзДПі)ЃЌЗДгІЯћКФЕФHNO3ЕФЮяжЪЕФСППЩФмЪЧ
AЃЎ0.5molЁЁЁЁЁЁ BЃЎ0.8molЁЁЁЁЁЁ C.1.1molЁЁЁЁЁЁ D.1.2mol
7ЃЎЮяжЪбѕЛЏадЁЂЛЙдадЕФЧПШѕЃЌВЛНігыЮяжЪЕФНсЙЙгаЙиЃЌЛЙгыЮяжЪЕФХЈЖШКЭЗДгІЮТЖШЕШгаЙиЁЃЯТСаИїзщЮяжЪЃКЂйCuгыHNO3ШмвКЃЛЂкCuгыFeCl3ШмвКЃЛЂлZnгыH2SO4ШмвКЃЛЂмFeгыHClШмвКЁЃгЩгкХЈЖШВЛЭЌЖјЗЂЩњВЛЭЌбѕЛЏЛЙдЗДгІЕФЪЧ
AЃЎЂйЂлЁЁЁЁЁЁ BЃЎЂлЂмЁЁЁЁЁЁЁЁЁЁ CЃЎЂйЂкЁЁЁЁЁЁ DЃЎЂйЂлЂм
6ЃЎ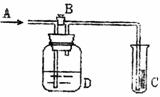 МћгвЭМ(A)ДІЭЈШыCl2ЃЌЕБЙиБе(B)ЗЇЪБЃЌ(C)ДІЕФЪЊШѓЕФКьВМЬѕУЛгаУїЯдБфЛЏЃЌЕБДђПЊ(B)ЗЇЪБЃЌ(C)ДІЕФЪЊШѓКьВМЬѕж№НЅЭЪЩЋЃЌдђ(D)ЦПжазАЕФШмвКЪЧ
МћгвЭМ(A)ДІЭЈШыCl2ЃЌЕБЙиБе(B)ЗЇЪБЃЌ(C)ДІЕФЪЊШѓЕФКьВМЬѕУЛгаУїЯдБфЛЏЃЌЕБДђПЊ(B)ЗЇЪБЃЌ(C)ДІЕФЪЊШѓКьВМЬѕж№НЅЭЪЩЋЃЌдђ(D)ЦПжазАЕФШмвКЪЧ
AЃЎХЈH2SO4ЁЁЁЁ BЃЎNaOHШмвКЁЁ CЃЎЫЎЁЁЁЁЁЁЁЁ DЃЎБЅКЭЪГбЮЫЎ
5.ЛЏбЇЪЕбщжаЃЌГЃНЋШмвКЛђЪдМСНјааЫсЛЏЃЌЯТСаЫсЛЏДІРэЕФДыЪЉжае§ШЗЕФЪЧ
A.ЖЈадМьбщSO2-3ЃЌПЩгУHNO3ЫсЛЏЕФBaCl2ШмвК
B.ЮЊСЫЬсИпKMnO4ШмвКЕФбѕЛЏФмСІЃЌгУбЮЫсНЋЦфЫсЛЏ
C.МьбщФГШмвКжаЪЧЗёКЌCl-ЃЌгУHNO3ЫсЛЏЕФAgNO3ШмвК
D.ХфжЦFeCl2ШмвКЪБЭЈГЃМгЩйСПHNO3ЫсЛЏЃЌМѕаЁЦфЫЎНтГЬЖШ
4ЃЎвбжЊЯТСаЮяжЪдквЛЖЈЬѕМўЯТбѕЛЏ KIЪБЃЌздЩэЗЂЩњШчЯТБфЛЏЃКFe3+ЁњFe2+ЃЌMnO-4ЁњMn2+ЃЌCl2ЁњCr-ЃЌHNO3ЁњNO2ЁЃШчЙћЗжБ№гУЕШЮяжЪЕФСПЕФЯТСаетаЉЮяжЪгызуСПЕФKIЗДгІЃЌЕУЕНI2зюЩйЕФЪЧ
A.Fe3+ЁЁЁЁЁЁЁЁЁЁ B.MnO4-ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ C.Cl2ЁЁЁЁЁЁЁЁЁЁ DЃЎHNO3
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com