
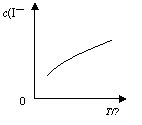
43、已知:①改变影响化学平衡的一个因素,平衡将向着能够减弱这种改变的方向移动,如升高温度,平衡将向吸热方向移动。②I2与KI溶液发生如下反应:I2(aq)+I-(aq) I3-(aq),达到平衡后溶液中I-的浓度c(I-)随温度T的变化如图所示。下列有关说法正确的是
I3-(aq),达到平衡后溶液中I-的浓度c(I-)随温度T的变化如图所示。下列有关说法正确的是
 A.固体碘微溶于水,实验室配制较浓“碘水”时,可将固体碘溶于
A.固体碘微溶于水,实验室配制较浓“碘水”时,可将固体碘溶于
一定浓度的KI溶液中
B.反应I2(aq)+I-(aq) I3-(aq)的
△H > 0
I3-(aq)的
△H > 0
C.在I2的KI水溶液中加入CCl4或H2O2均可使溶液中c(I3-)增大
D.依此原理,Cl2在一定浓度的NaCl溶液中溶解度增大
42、下列离子方程式书写正确的是
A.NaHCO3溶液中加过量的Ba(OH)2溶液:2HCO3-+Ba2++2OH-=BaCO3↓+2H2O+CO32-
B.Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I-=2Fe2++I2
C.氯气溶于水:Cl2
+ H2O 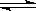 2H+
+ Cl— + ClO—
2H+
+ Cl— + ClO—
D.向NaAlO2溶液中通入过量CO2:AlO2- + CO2 + 2H2O = Al(OH)3↓+ HCO3-
41、某化学反应2X(g)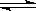 Y(g)+Z(g)在4种不同条件下进行,Y、Z起始浓度为0,反应物X的浓度(mol·L-1)随反应时间(min)的变化情况如下表:
Y(g)+Z(g)在4种不同条件下进行,Y、Z起始浓度为0,反应物X的浓度(mol·L-1)随反应时间(min)的变化情况如下表:
|
实验 序号 |
 时间 时间浓度 温度 |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
|
1 |
800℃ |
1.0 |
0.80 |
0.67 |
0.57 |
0.50 |
0.50 |
0.50 |
|
2 |
800℃ |
1.0 |
0.60 |
0.50 |
0.50 |
0.50 |
0.50 |
0.50 |
|
3 |
800℃ |
C |
0.92 |
0.75 |
0.63 |
0.60 |
0.60 |
0.60 |
|
4 |
820℃ |
1.0 |
0.40 |
0.25 |
0.20 |
0.20 |
0.20 |
0.20 |
下列说法不正确的是
A.C >1.0
B.实验2可能使用了催化剂
C.实验3比实验2先达到化学平衡状态
D.前10分钟,实验4的平均化学反应速率比实验1的大
50、2012年某高校化学工作者创建了“元素立体周期律”,在原来二维周期表横列(X轴)和纵列(Y轴)基础上,增加了一个竖列(Z轴)。Z轴按“中质差”(中子数和质子数之差△Z=N-P)自上而下,递增顺序排列。原“二维元素表”中的相对原子质量由同位素“中质和”(中子数和质子数之和A=N+P)替代。下列说法正确的是
A.“中质和”相同的核素一定是同一元素
B.“中质差”相同的核素一定是同一元素
C.N 2 -P 2 = A×△Z
D.至2008年,人们发现108种元素有m种同位素,说明中质差一定有m种
B组题:(B组供基础较好、重点中学、提高班、培优、竞赛的学生使用。突显实力,不定项选择题)
49、右图为元素周期表短周期的一部分,且M、X、Y、Z为主族元素,下列
说法正确的是
|
|
M |
|
|
X |
Y |
Z |
A.Y的氢化物的沸点一定比M的氢化物的沸点高
B.Z的最高价氧化物对应的水化物有可能是弱电解质
C.这四种元素形成的晶体单质都是分子晶体
D.单质M的的晶体中可能含有共价键和分子间作用力
48、用惰性电极电解AgNO3溶液,在阳极上收集到0.28L气体(标准状况下),用NaOH溶液中和电解生成的酸需要250mL,则NaOH溶液的物质的量浓度为
A.0.05mol·L-1 B.0.10mol·L-1 C.0.15mol·L-1 D.0.20mol·L-1
47、下列推断正确的是
A.明矾是一种复盐,则NaAlO2也是一种复盐
B.CaCO3的溶解度小于Ca(HCO3)2,则Na2CO3的溶解度小于NaHCO3
C.在Ca(ClO)2溶液中分别通入CO2、SO2,前者生成CaCO3沉淀,则后者也生成CaSO3沉淀
D.S、Cl两种元素为同周期元素,H2SO4为强酸,则HClO4也为强酸
46、下列说法正确的是
A.无水硫酸铜的吸水性较浓硫酸强
B.将石灰石、纯碱、石英在玻璃熔炉中高温熔融可制得玻璃
C.把铜片和铁片用导线连接后一起插入三氯化铁溶液中,在铜片表面出现一层铁
D.取5mL 0.1 mol·L-1 FeCl3溶液,滴加0.1 mol·L-1 KI溶液5~6滴,再加入少量KSCN溶液,溶液呈红色,说明该反应有一定的限度
45、管道煤气的主要成分是CO、H2和少量甲烷。相应的热化学方程式为
2H2(g)+O2(g)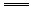 2H2O(l);△H=-571.6 kJ·mol-1
2H2O(l);△H=-571.6 kJ·mol-1
2CO(g)+O2(g)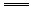 2CO2(g);△H=-566 kJ·mol-1
2CO2(g);△H=-566 kJ·mol-1
CH4(g)+2O2(g)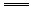 CO2(g)+2H2O(l);△H=-890.3kJ·mol-1
CO2(g)+2H2O(l);△H=-890.3kJ·mol-1
当使用管道煤气的用户改烧天然气后,在相同条件下燃烧等体积的燃气,理论上所获得的热值,后者大约是前者的
A.0.8倍 B.1.3倍 C.1.6倍 D.3.1倍
44、对于在密闭容器中、一定条件下进行的可逆反应N2(g)+3H2(g)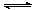 2NH3(g),能说明反应已达到平衡状态的是
2NH3(g),能说明反应已达到平衡状态的是
A.各物质体积分数相等 B.c(NH3)保持不变
C.各物质浓度相等 D.c(NH3)∶c(N2)∶c(H2)=2∶1∶3
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com