
29、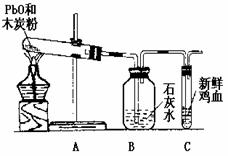 小强、小明和小梅三同学在学习了木炭还原氧化铜的实验后,提出如下问题:“木炭与一氧化铅(化学式为PbO)反应生成铅的同时产生的气体一定全部为二氧化碳吗?”请你和他们一起对产物中气体的成分进行研究,并回答有关问题。
小强、小明和小梅三同学在学习了木炭还原氧化铜的实验后,提出如下问题:“木炭与一氧化铅(化学式为PbO)反应生成铅的同时产生的气体一定全部为二氧化碳吗?”请你和他们一起对产物中气体的成分进行研究,并回答有关问题。
(1)猜想:小强认为:反应产生的气体全部
为二氧化碳。小明认为:反应产生的气体
全部为一氧化碳。小梅认为:反应产生的
气体既有二氧化碳又有一氧化碳。
(2)设计实验:根据各自的猜想,他们共同设计了实验,实验装置如右图(他们在实验
中进行了规范操作和细致的观察)。
(3)现象与结论:如果小强猜想正确,装置B、C中的实验现象是
;如果小明猜想正确,装置B、C中的实验现象是
。如果小梅猜想正确,装置B、C中的实验现象是
(4)此实验装置有不足之处,请你对该装置进行改进,具体措施是
。
(5)根据上述实验及学习的木炭与CuO、Fe2O3的反应,请你归纳出单质碳的一项重要用途是 。
28、(1)市场上销售的香肠、盐水鸭、榨菜、豆腐干等食品,常采用真空包装。真空包装的目的是除去空气,使大多数微生物因缺少 气而受到抑制,停止繁殖,同时防止食品发生缓慢 而变质。
(2)茶叶、肉松、膨化食品等常采用真空充气包装,即将食品装入包装袋,抽出包装袋内空气,再充人防止食品变质的气体,然后封口。真空充气包装能使食品保持原有的色、香、味及营养价值,防止食品受压而破碎变形。
[提出问题]充入食品包装袋中的气体是什么?
[猜想与验证]
可能是N2。实验初步验证的方法及现象:
充人的气体还可能是:① ;②
27、若取质量均为mg镁和铁,分别投入到50g溶质质量分数相同的硫酸中,充分反应均产生0.2g氢气。可推断出:
①充分反应后,一定有剩余的金属是_____
②m的取值范围为____________,反应中消耗掉金属镁的质量为____________
③硫酸中H2SO4质量分数为_______
26、某课外兴趣小组,确立了“酸碱中和生成的正盐溶液的性质”作为研究课题,在研究
中他们发现,正盐虽然不能电离出氢离子或氢氧根离子,但是其溶液却不一定呈中性,
有的呈酸性,有的呈碱性。为什么呢?盐溶液的酸碱性与什么有关呢?由“组成、结构
决定物质性质”的观点出发,他们又进一步从组成特征上去找原因, 发现正盐溶液的酸
碱性与对应的酸和碱的强弱有关。他们将实验结果统计如下:
|
酸 |
碱 |
相应的正盐 |
溶液的pH |
|
HCl
(强酸) |
NaOH
(强碱) |
NaCl |
7 |
|
H2SO4(强酸) |
KOH (强碱) |
K2SO4 |
7 |
|
H2CO3(弱酸) |
NaOH
(强碱) |
Na2CO3 |
> 7 |
|
H3PO4(弱酸) |
KOH (强碱) |
K3PO4 |
> 7 |
|
HNO3 (强酸) |
Cu(OH)2 (弱碱) |
Cu(NO3)2 |
< 7 |
|
HCl
(强酸) |
Fe(OH)3 (弱碱) |
FeCl3 |
< 7 |
⑴请你根据上表归纳出正盐溶液的酸碱性与对应酸、碱的强弱关系:(至少写2条)
⑵根据他们的发现,请你判断硝酸钠、硝酸铁、硫酸铜、氯化钾、磷酸钠、碳酸钾六种溶液的酸碱性,其中溶液呈酸性的是 _________、呈碱性的是 、呈中性的是 。
25、小明学习了盐酸、硫酸后,知道它们的化学性质有许多相似之处。由此他想通过实
验探究食醋中的主要成分醋酸的化学性质。他的推测可能有哪些?(写出两点即可)
(1)___________ ____ (2)______
24、变色眼镜的玻璃片中含溴化银(AgBr),溴化银见光分解为银单质(Br2),眼镜片自动变
暗。光线弱时,单质溴与银化合生成溴化银,眼镜片变亮。试写出上述两种变化的化
学方程式:见光_______ _______________避光______ ______________
23、混盐一般是由一种阳离子与两种酸根离子组成的盐,如:Ca(NO3)Cl。漂白粉中有一种混盐CaOCl2(其中钙元素化合价为+2,氧元素化合价为-2)。(1)请将该混盐改写成如Ca(NO3)Cl的形式,其化学式表示为 。(2)该混盐中氯元素的化合价为 。
22、俄国化学家门捷列夫在总结前人经验的基础上,通过艰辛的努力,终于提出了现代元素周期表的雏形。下表为元素周期表的部分示意图,表中数字为各元素原子的质子数,利用下表回答相关问题:
|
H 1 |
|
He 2 |
|||||||||||||||
|
Li 3 |
Be 4 |
|
B 5 |
C 6 |
N 7 |
O 8 |
F 9 |
Ne 10 |
|||||||||
|
Na 11 |
Mg 12 |
Al 13 |
Si 14 |
P 15 |
S 16 |
Cl 17 |
Ar 18 |
||||||||||
|
① |
② |
|
|
|
|
|
|
|
|
|
|
③ |
|
|
|
|
|
(1)用符号表示:带两个单位负电荷且质子数为8的离子 (写一种)。
AB2型化合物 (写一种)。
(2)去年底重庆开县发生天然气“井喷”事件。喷出的气体中有一种有毒的含有18个
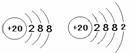 质子的A2B型气体,其水溶液是一种无氧酸,请用符号和数字表示:3个A2B分子 。
质子的A2B型气体,其水溶液是一种无氧酸,请用符号和数字表示:3个A2B分子 。
(3)研究表中各元素原子的质子数,可发现元素从左向
|
请预测质子数为20的元素在表中的位置 (填①、②、③)。该元素离子的
结构示意图是 。(填“甲”或“乙”)
21、从给定化合价的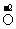 、
、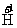 、
、 、
、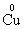 、
、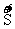 五种元素中,选择适当的元素写出下列有关物质的化学式:酸性氧化物_________;无氧酸_________;单质__________。
五种元素中,选择适当的元素写出下列有关物质的化学式:酸性氧化物_________;无氧酸_________;单质__________。
20、某化工厂电解食盐水前,先要除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于
水,然后进行①过滤、②加过量的NaOH溶液、③加适量盐酸、④加过量Na2CO3溶液、
⑤加过量BaCl2溶液等五项操作,其中正确的操作顺序是
A、①、④、②、⑤、③ B、④、①、②、⑤、③
C、②、⑤、④、①、③ D、⑤、②、④、①、③
第Ⅱ卷 非选择题(共60分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com