
|
 32、有一农民从市场买回一袋钾肥,其包装袋上的部分内容如下图所示。为确定该化肥纯度(即K2SO4的质量分数)是否符合标准。技术人员称取10g样品,加入适量水溶解后,与足量的BaCl2溶液充分反应。过滤、洗涤、烘干沉淀,测得其质量为11.65g。试通过计算确定该化肥纯度是否符合包装袋上的说明。(假设化肥中的杂质不与BaCl2溶液反应)
32、有一农民从市场买回一袋钾肥,其包装袋上的部分内容如下图所示。为确定该化肥纯度(即K2SO4的质量分数)是否符合标准。技术人员称取10g样品,加入适量水溶解后,与足量的BaCl2溶液充分反应。过滤、洗涤、烘干沉淀,测得其质量为11.65g。试通过计算确定该化肥纯度是否符合包装袋上的说明。(假设化肥中的杂质不与BaCl2溶液反应)

33、将氧化铜和木炭粉(不含杂质)按一定
质量比混合,充分研磨均匀后,称取10.0g置于试管中,如
右图所示装置。在隔绝空气的情况下,对试管中的混合物加
热至高温。待充分反应后,冷却。称得试管中残余固体为
31、长途运输鱼苗时,人们常在水中加入少量过氧化钙(CaO2)固体。甲、乙两位同学发现往水中投入过氧化钙时产生气泡。提出问题:当把过氧化钙投入足量水中时,最终会生成什么物质呢?
进行猜想:甲同学认为:生成氧化钙和氧气;
乙同学认为:生成氢氧化钙和氧气。
(1)你认为 同学的猜想是错误的,其理由是
(2)请设计一个实验方案来验证另一个同学的猜想是正确的,并填入下表空格中。
|
实验步骤及操作方法 |
预期的实验现象 |
结论 |
|
1.取少量过氧化钙放入试管中, 加足量水, ___________________________。 |
|
有氧气生成 |
|
2.________________________ ___________________________ ___________________________ |
出现浑浊 |
|
(3)运输鱼苗时,在水中加入少量过氧化钙的主要目的_____________ __________________________________________________________
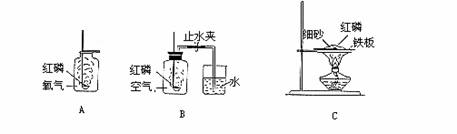 29、某实验小组进行有关红磷燃烧的系列实验(如下图)。
29、某实验小组进行有关红磷燃烧的系列实验(如下图)。
(1)实验一:如图A所示,将点燃的红磷插入集气瓶中,红磷在氧气中剧烈燃烧, 可看到集气瓶中产生大量 _____ ,该反应的化学方程式为 ________________ ,其基本反应类型是 反应;
(2)实验二:如图B所示,将过量红磷点燃插入集气瓶中,塞紧橡皮塞,待燃烧停止并冷却到室温后,打开止水夹,可观察到烧杯中的水被吸进集气瓶内,吸进水的体积大约占原瓶内空气体积的1/5,此实验的目的是_____
_____________________________________________________
(3)实验三:如图C所示,将少量红磷放置在一块铁板上,再用细砂完全覆盖,用酒精灯加热铁板一段时间,看不到明显现象,这是因为_________ _______
______________________________________;撤去酒精灯后,立即将砂子拨开露出红磷,看到红磷燃烧,这是因为 。
30、科学探究重在提出问题、作出猜想,并能用事实来验证。炎热的夏季,你一定想喝一杯冰水解暑。某冷饮店出售一种特制的冰水,由服务员在水中加入一些雪状的物质,该物质一放入水中立即冒出大量气泡,很快就得到一杯清凉可口的冰水,饮用时有碳酸饮料的口感。
(1)请你判断雪状的物质是 ;
(2)请你设计两个实验分别验证这种物质的成分。(注意按序号填写答案)
|
|
操作步骤 |
实验现象 |
|
方法一 |
① |
② |
|
方法二 |
③ |
④ |
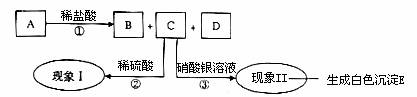
28、 A、B、C、D、E是初中化学中常见的化合物,其中A为白色固体,B为无色气体,E为不溶于稀硝酸的白色沉淀,它们的关系如图所示。
请回答下列问题:
(1)白色沉淀E为 ;
(2)若现象I为“生成白色沉淀”,则A的化学式可能为 (写出一种即可);
反应①的化学方程式为 ______________________ ,反应②的化学方程式为 ________ ;
(3)若现象I为“无明显变化”,则A的化学式可能为 或 等。
27、芯片是所有电脑、“智能家电”的核心部件,它是以高纯度的单质硅(硅的元素符号为Si)为材料制成的。用化学方法制得高纯硅的反应原理为
①SiO2+2C===Si+2CO↑ ②Si+2Cl2=== SiCl4 ③SiCl4+2H2== Si+4HCl
请回答:
⑴上述反应中属于置换反应的是________(填序号)。
⑵SiCl4中硅元素的化合价是_______
⑶反应①中碳单质表现了______________性(填“氧化”或“还原”)。
⑷反应①中生成有剧毒的CO,它能与人体血液中的血红蛋白结合,使血红蛋白不能很好地与氧气结合,从而使人体缺氧而造成“煤气中毒”。如果发现有人“煤气中毒”,你将采用哪些救治措施?(只回答一种即可)_____________________。
26、“物质的组成与结构决定物质的性质”是化学学科中的重要观点。按照这一观点讨论下列的问题:
过氧化氢是一种常用的杀菌消毒剂,其原因是过氧化氢分子中含有一种叫做“过氧基”(下图①中虚线框标出的部分)的结构。据此推测下列②-④的物质中,可用作杀菌消毒剂的___________
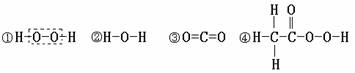
25、硒元素具有抗衰老,抑制癌细胞的功能,它的化学性质与硫相似,元素符号为Se,它对应的含氧酸的化学式是H2SeO4,这种酸应读作 ,其与氢氧化钠溶液反应的化学方程式是 。
24、对公共场所用过氧乙酸溶液进行消毒是预防非典型肺炎的措施之一。已知过氧乙酸(X)是一元酸,有较强的腐蚀性,并易按下式分解:2X=2C2H4O2+O2↑,则其化学式是___________,保存和配制过氧乙酸不宜使用_____________(填“铁”或“玻璃”或“塑料”或“陶瓷”)材料制成的容器。
23、 A、B、C代表三种单质,甲、乙、丙、丁代表四种化合物。在常温下单质B和化合物甲的颜色、状态相同,其中甲中氧元素的质量分数为20%,甲与稀硫酸反应生成乙,在一定条件下,它们之间有如下反应:
甲 + B → 丁 + A 乙 + C → 丙 + A
请回答下列问题:
(1)化合物甲的化学式______________;单质C的化学式_______________。
(2)写出下面各物质反应的化学方程式:(要注明反应条件)
甲与B___________________________________________________。
乙与C____________________________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com