
1£Æœ¬ÕºÀ˘ 汉ªØ Ù”⁄ªØ—ß±‰ªØµƒ «

A£Æ∂‘≤£¡ß∆¨∫Ù∆¯°° B£Æ¿Ø÷Ú»º…’°°°° c£Æ ™“¬¡¿∏…°° D£Æµ∆≈ðÕ®µÁ∑¢π‚
33£Æ”…”⁄µÿ«Úµƒ∂˛—ıªØúæÁ‘ˆ£¨”…¥À≤˙…˙µƒ°∞Œ¬ “–ß”¶°± π◊‘»ª‘÷∫¶∆µ∑±∑¢…˙£¨2004ƒÍµ◊”°∂»—Û∑¢…˙µƒ¥Ûµÿ’º∞∫£–•‘Ï≥…µƒ≤“æÁ π ¿»Àº«“‰”Ö¬°£œ˚≥˝°∞Œ¬ “–ß”¶°±µƒ”––ߥΠ© «π„∑∫÷≤ ˜‘Ï¡÷°£“—÷™180g∆œÃ—ë(C6H12O6)ÕÍ»´»º…’ ±∑≈»»2804KJ£¨Ã´—Ù√ø∑÷÷”∂‘µÿ«Ú±Ì√Ê∑¯…‰ƒÐ¡øŒ™2.1J/cm2£ª÷≤ŒÔÕ®π˝π‚∫œ◊˜”√…˙≥…∆œÃ—ë∫Õ—ı∆¯°£…Ëπ‚∫œ◊˜”√ ±Ã´—كСø¿˚”√¬ Œ™10%£¨√ø∆¨ ˜“∂√ʪ˝“‘10cm2º∆À„£¨’‚—˘µƒ ˜“∂100∆¨“™∫œ≥…1.8g∆œÃ—루Œ £∫
(1)–Ëπ‚’’∂ý≥§ ±º‰£ø
(2)»Ùø’∆¯÷–∫¨CO2÷ ¡ø∑÷ ˝Œ™0.3%£¨–Ë“™±Í◊º◊¥øˆœ¬ø’∆¯∂ý…Ÿ…˝£ø(±Í◊º◊¥øˆœ¬ø’∆¯√Ð∂»Œ™1.29g/L)
(3)»Ù±Í◊º◊¥øˆœ¬—ı∆¯√Ð∂»Œ™1.429g/L£¨Œ π‚∫œ◊˜”√ ±≥˝…˙≥…1.8g∆œÃ—루ªπ∑≈≥ˆ—ı∆¯∂ý…Ÿ…˝£ø
31£Æ[—–æøøŒÃ‚]£∫ÃΩæø»»ÀÆ∫¯µ◊≤øÀÆπ∏µƒ÷˜“™≥…∑÷
[≤È‘ƒ◊ ¡œ]£∫∏√–°◊ÈÕ¨—ßÕ®π˝≤È‘ƒ◊ ¡œ÷™µ¿£¨ÃÏ»ªÀÆ÷–“ª∞„∂º∫¨”–Ca2+°¢Mg2+°¢HCO3-µ»¿Î◊”£¨‘⁄º”»» ±£¨’‚–©¿Î◊”«˜”⁄…˙≥…»ÐΩ‚∂»∏¸–°µƒŒÔ÷ --ÀÆπ∏(÷˜“™≥…∑÷Œ™ÃºÀ·—Œ°¢ºÓµƒªÏ∫œŒÔ)°£Õ¨ ±£¨À˚√«ªπ≤È‘ƒµΩœ¬¡–”–πÿŒÔ÷ µƒ»ÐΩ‚–‘£∫
|
°° ŒÔ÷ |
Ca(HCO3)2 |
°°Mg(HCO3)2 |
Ca(OH)2 |
Mg(OH)2 |
CaCO3 |
MgCO3 |
|
°°»ÐΩ‚–‘ |
°° ø…»Ð |
°° ø…»Ð |
°° Œ¢»Ð |
°° ≤ª»Ð |
°° ≤ª»Ð |
°° Œ¢»Ð |
[÷≥ˆ≤¬œÎ]£∫ÀÆπ∏µƒ÷˜“™≥…∑÷“ª∂®∫¨”–Mg(OH)2∫Õ°°°°°° £¨ø…ƒÐ∫¨”–Ca(OH)2∫Õ°°°° °£
[…˺∆∑Ω∞∏]£∫
(1)º◊Õ¨—ß‘⁄…’±≠÷–∑≈»Î…Ÿ¡ø—–ÀȵƒÀÆπ∏£¨º”»Î ¡ø’Ù¡ÛÀÆ≥‰∑÷Ω¡∞Ë£¨»°…œ≤„«Â“∫º”»Î°°°° £¨√ª”–∞◊…´≥¡µÌ£¨Àµ√˜ÀÆπ∏÷–ŒÞCa(OH)2£ª
(2)““Õ¨—߅˺∆œ¬¡– µ—È◊∞÷√£¨Ω¯“ª≤Ω»∑∂®ÀÆπ∏÷–∫¨”–úÀ·—Œµƒ≥…∑÷£¨≤Ω÷Ë»Áœ¬£∫
¢Ÿ∞¥Õº◊È◊∞“«∆˜£¨Ω´50gÀÆπ∏ ‘—˘∑≈»Î◊∂–Œ∆ø÷–£¨º”»Î◊„¡øƒ≥À·»Ð“∫£ª
¢⁄≤‚¡ø“ª∂® ±º‰ƒ⁄∏…‘ÔπЃ⁄ŒÔ÷ ‘ˆº”µƒ÷ ¡ø(º˚œ¬¡–«˙œþ)£ª
¢€¥˝◊∂–Œ∆ø÷–≤ª‘Ÿ≤˙…˙∆¯≈ð ±£¨¥Úø™ªÓ»˚B£¨¥”µºπÐA¥¶ª∫ª∫πƒ»Î“ª∂®¡øµƒø’∆¯£ª
¢Ð‘Ÿ¥Œ≥∆¡ø∏…‘ÔπЃ⁄ŒÔ÷ ‘ˆº”µƒ÷ ¡ø£ª
¢ð÷ÿ∏¥¢€∫բеƒ≤Ÿ◊˜£¨÷±÷¡∏…‘ÔπЃ⁄ŒÔ÷ ÷ ¡ø≤ª±‰°£
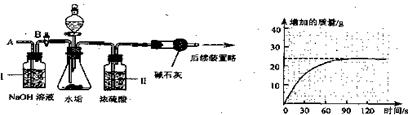
a£Æ≤Ω÷Ë¢ŸÀ˘º”µƒÀ·»Ð“∫ «°°°°°°°°°°°°°°°°°° £ª
b£Æ◊∞÷√¢Úµƒ◊˜”√ «°°°° °°°°°°°°°°°°°°°°°°°°°°£ª¥”µºπÐA¥¶ª∫ª∫πƒ»À“ª∂®¡øµƒø’∆¯ ±£¨◊∞÷√Iµƒ◊˜”√ «°°°°°°°°°°°°°°°°°°°°°°°°°° £ª
c£Æ—–æø–‘–°◊ȵƒÕ¨—ßæ≠π˝ºÚµ•º∆À„£¨»œŒ™ÀÆπ∏÷–“ª∂®∫¨”–MgCO3£¨¿Ì”… «°°°°°°°°°° °£
[ µ—ÈΩ·¬€]Õ®π˝…œ ˆÃΩæøø…÷™£∫ÀÆπ∏µƒ÷˜“™≥…∑÷”–°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
30£Æƒ≥Õ¨—ßΩ´“ª–°∞¸Õ≠∑€∫Õ–ø∑€µƒªÏ∫œŒÔ∑≈»Î“ª∂®¡øµƒœıÀ·“¯»Ð“∫÷–£¨ π∆‰≥‰∑÷∑¥”¶∫Ûπ˝¬À£¨µ√µΩπÃÃÂ∫Õ¿∂…´¬À“∫£¨≤¢∂‘¬À“∫µƒ◊È≥…Ω¯––ÃΩæø°£
(1)–ø∫ÕœıÀ·“¯»Ð“∫∑¥”¶µƒªØ—ß∑Ω≥Ã Ω°°°°°°°°°°°°°°°°°°°°°°°°°°°° °°°°°°°°°°°°°£
(2)Õ¨—ß√«∂‘¬À“∫÷–À˘∫¨µƒ»Ð÷ ◊ˆ≥ˆ∂ý÷÷≤¬œÎ£¨∆‰÷–”–¡Ω÷÷≤¬œÎø…ƒÐ≥…¡¢£¨’‚¡Ω÷÷≤¬œÎ «£∫
¢Ÿ»Ð÷ Œ™°°°°°°°°°°°°°°°°°°°°°°°°°° £ª¢⁄»Ð÷ Œ™°°°°°°°°°°°°°°°°°°°°°°°° °£
|
∑Ω∞∏ °° |
°°°° µ—È≤Ÿ◊˜ °° |
°°°° µ—Èœ÷œÛ °° |
°° Ω·°°°° ¬€ °° |
|
∑Ω∞∏“ª |
°° |
°° |
≤¬œÎ°°°°°° ≥…¡¢ |
|
∑Ω∞∏∂˛ |
°° |
°° |
≤¬œÎ°°°°°° ≥…¡¢ |
29£Æº◊À·(HCOOH)Õ®≥£ «“ª÷÷ŒÞ…´“◊ª”∑¢µƒ“∫ã¨À¸‘⁄≈®¡ÚÀ·◊˜”√œ¬“◊∑÷Ω‚£¨∑¥”¶∑Ω≥Ã ΩŒ™£∫HCOOH CO°¸+H2O°£ƒ≥øŒÕ‚ªÓ∂Ø–°◊ȵƒÕ¨—ß”˚”√∏√∑¥”¶¿¥÷∆»°CO£¨≤¢ªπ‘≠∫Ï◊ÿ…´µƒ—ıªØÃ˙∑€ƒ©°£œ÷”–œ¬¡–“«∆˜ªÚ◊∞÷√π©—°‘Ò£∫
CO°¸+H2O°£ƒ≥øŒÕ‚ªÓ∂Ø–°◊ȵƒÕ¨—ß”˚”√∏√∑¥”¶¿¥÷∆»°CO£¨≤¢ªπ‘≠∫Ï◊ÿ…´µƒ—ıªØÃ˙∑€ƒ©°£œ÷”–œ¬¡–“«∆˜ªÚ◊∞÷√π©—°‘Ò£∫
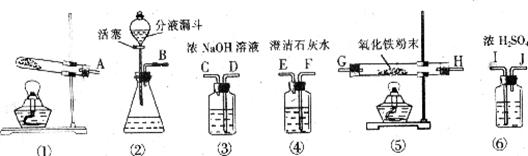
(1)”√º◊À·µŒ»Î≈®¡ÚÀ·µƒ∑Ω∑®÷∆»°CO£¨”¶—°°°°°°°°°°° (ÃÓ–Ú∫≈)◊∞÷√£ª»Áπ˚“™≥˝»•CO∆¯ÃÂ÷–ªÏ”–…Ÿ¡øµƒº◊À·£¨◊Ó∫√—°‘Ò…œÕº÷–°°°°°°°°°° (ÃÓ–Ú∫≈)Ω¯––œ¥∆¯°£
(2)”√…œ ˆ∑Ω∑®÷∆»°µƒCOªπ‘≠—ıªØÃ˙£¨≤¢ºÏ—È∆¯ÃÂ≤˙ŒÔ£¨‘Ú∏˜“«∆˜µƒΩ”ø⁄¡¨Ω”À≥–ÚŒ™°° ___________________________________________(ÃÓ◊÷ƒ∏)°£
(3)‘⁄∂‘—ıªØÃ˙∑€ƒ©º”»»«∞£¨Œ™∞≤»´∆º˚£¨”¶Ω¯––µƒ“ªœÓ÷ÿ“™≤Ÿ◊˜ «°°°°°°°°°°°°°° °£
(4)¥”ø™ ºº”»»µΩ µ—ÈΩ· ¯£¨—ıªØÃ˙∑€ƒ©µƒ—’…´±‰ªØŒ™°°°°°°°°°°°°°°°°°°°°°°°° £¨∑¥”¶∑Ω≥Ã ΩŒ™°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
(5)…œ ˆ µ—ȵƒŒ≤∆¯≤ªƒÐ÷±Ω”≈≈∑≈µΩø’∆¯÷–£¨«Îƒ„Àµ≥ˆ“ª÷÷¥¶¿ÌŒ≤∆¯µƒ∑Ω∑®£∫°°°°°°°° °£
28£Æ–°√˜Õ¨—ß‘⁄ π”√°∞≥˝π∏檰±»•≥˝»»ÀÆ∫¯÷–µƒÀÆπ∏ ±£¨∑¢œ÷”–¥Û¡øµƒ∆¯≈ð≤˙…˙£¨¡™œÎÀÆπ∏µƒ÷˜“™≥…∑÷ «ÃºÀ·∏∆°£–°√˜≤¬œÎ°∞≥˝π∏檰±µƒ≥…∑÷÷–ø…ƒÐ”–À·°£
¢ŸŒ™÷§ µ◊‘º∫µƒ≤¬œÎ£¨–°√˜¥”º“÷–”÷’“¿¥¡Ω¿ý≤ªÕ¨µƒŒÔ÷ Ω¯–– µ—È£∫
µ—È“ª£∫°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° £ª
µ—È∂˛£∫°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
æ≠ µ—È£¨–°√˜µ√≥ˆ°∞≥˝π∏檰±µƒ”––ß≥…∑÷÷–“ª∂®”–À·µƒΩ·¬€°£
¢⁄–°√˜œÎ ‘÷∆“ª∆ø°∞≥˝π∏檰±£¨ƒ„»œŒ™HCl°¢H2SO4¡Ω÷÷À·÷–µƒ°°°°°°°°°°°° ∏¸∫œ £¨¿Ì”… «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
¢€Ω·∫œ…œ√Ê∂‘°∞≥˝π∏檰±µƒ¡ÀΩ‚£¨‘⁄ π”√°∞≥˝π∏檰± ±”¶◊¢“‚°°°°°°°°°°°°°°°°°°°°°°°° °£
27£Æ–°√˜°¢–°≈Ù∫Õ–°∑º»˝ŒªÕ¨—ß‘⁄“ª∆ÃΩæø¿Ø÷Ú»º…’£¨À˚√«Ω´∂Ã≤£¡ßµºπÐ≤»Ηʖƒ£¨∑¢œ÷¡Ì“ª∂À“≤ø…“‘µ„»º°£
(1)[÷≥ˆŒ Â]µºπпԓª∂®”–ø…»º–‘∆¯Ã£¨∆¯ÃÂ≥…∑÷ø…ƒÐª· « ≤√¥ƒÿ£ø
(2)[≤¬œÎ]–°√˜»œŒ™£∫ø…ƒÐ «¿Ø÷Ú≤ªÕÍ»´»º…’ ±≤˙…˙µƒCO°£
°°°°°°°°°°°° –°≈Ù»œŒ™£∫ø…ƒÐ «¿Ø÷Ú Ð»»∫Û≤˙…˙µƒ’Ù∆¯°£
°°°°°°°°°°°° –°∑º»œŒ™£∫ø…ƒÐ…œ ˆ¡Ω÷÷«Èøˆ∂º”–°£
(3)[…˺∆ µ—È∑Ω∞∏]«Îƒ„∞Ô÷˙À˚√«…˺∆“ª∏ˆºÚµ•µƒ µ—È∑Ω∞∏£¨¿¥≈–∂œƒƒ“ª÷÷∑÷Œˆ «’˝»∑µƒ_____________________________________________________________________________°£
(4)[œ÷œÛ”ÎΩ·¬€]»Áπ˚–°√˜µƒ≤¬œÎ’˝»∑£¨œ÷œÛ”¶ «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
°°°°°°°°°°°°°°°°°° »Áπ˚–°≈Ùµƒ≤¬œÎ’˝»∑£¨œ÷œÛ”¶ «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
°°»Áπ˚–°∑ºµƒ≤¬œÎ’˝»∑£¨œ÷œÛ”¶ «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
(5)»Áπ˚”√CnH2n+2±Ì æ¿Ø÷Úµƒ÷˜“™≥…∑÷£¨∆‰»º…’µƒªØ—ß∑Ω≥Ã ΩŒ™£∫°°°°°°°°°°°°°°°° °£
26£Æ◊‘»ªΩÁµƒøÛŒÔ÷–”–“ª÷÷÷ÿæß ØøÛ£¨À¸µƒ÷˜“™≥…∑÷ «BaSO4£¨À¸≤ª»Ð”⁄»Œ∫ŒÀ·°¢ºÓ∫ÕÀÆ£¨¥ø檵ƒ¡ÚÀ·±µø…π©“Ω¡∆µ»∑Ω√Ê”¶”√°£ƒ≥Õ¨—ß”√÷ÿæß Ø∫ÕΩπÃøŒ™‘≠¡œ£¨÷∆»°¥ø檡ÚÀ·±µ£¨≤ø∑÷¡˜≥ûÁœ¬(…ËøÛŒÔ÷–‘”÷ ≤ª”ÎΩπÃø∑¥”¶£¨“≤≤ª»Ð”⁄ÀÆ)£∫
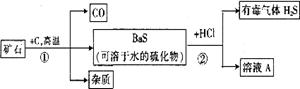
(1)≤Ω÷Ë¢Ÿ÷–£¨ƒƒ–©‘™ÀÿµƒªØ∫œº€…˝∏þ£¨ƒƒ–©‘™ÀÿµƒªØ∫œº€ΩµµÕ£ø°°°°°°°°°°°°°°°°°°°°°° £ª
(2)≤Ω÷Ë¢⁄÷–»Ð“∫A÷–»Ð÷ µƒªØ—ß Ω£∫°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° £ª
(3)–¥≥ˆ¿˚”√»Ð“∫A÷–µƒ»Ð÷ Œ™÷˜“™‘≠¡œ÷∆»°BaSO4µƒªØ—ß∑Ω≥Ã Ω£∫°°°°°°°°°°°°°°°° £ª
(4)≤Ω÷Ë¢⁄≤˙…˙”–∂æ∆¯ÃÂH2S£¨”¶º”“‘∏ƒΩ¯£¨Œ™ π µ—Èº»≤ª≤˙…˙H2S”÷ƒÐªÒµ√¥øæªBaSO4£¨«Îƒ„÷≥ˆ∏ƒΩ¯“‚º˚°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° £ª”–πÿ∑¥”¶µƒªØ—ß∑Ω≥Ã Ω «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
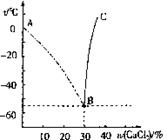
25£ÆΩ´“ª÷÷—Œ»Ð”⁄ÀÆ£¨ª· πÀƵƒ±˘µ„(ƒ˝πõ„)ΩµµÕ£¨±˘µ„ΩµµÕ∂ý…Ÿ”ΗŒ‘⁄»Ð“∫÷–µƒ÷ ¡ø∑÷ ˝”–πÿ°£»Áπ˚Ω´¥À—Œ»Ð“∫ΩµŒ¬°£‘Ú‘⁄¡„∂»“‘œ¬ƒ≥Œ¬∂»ª·Œˆ≥ˆ±˘°£µ´µ±—Œ‘⁄»Ð“∫÷–µƒ÷ ¡ø∑÷ ˝±»Ωœ¥Û ±£¨‘⁄Ω´»Ð“∫¿‰»¥µƒπ˝≥Ã÷–œ»Œˆ≥ˆµƒπÃÃÂ≤ª «±˘∂¯ «—Œµƒæßð£»ÁÕºÀ˘ 棨∫·◊¯±ÍŒ™¬»ªØ∏∆»Ð“∫÷–»Ð÷ µƒ÷ ¡ø∑÷ ˝£¨◊ð◊¯±ÍŒ™Œ¬∂»£¨ ‘ÃÓø’ªÚºÚ¥£∫
 °°
°°
(1)¬»ªØ∏∆»Ð“∫ø…”√◊˜¿‰∂≥º¡£¨µ±ŒÞÀƬ»ªØ∏∆”ÎÀƪÏ∫œµƒ÷ ¡ø±»Œ™°°°°°° °° ±(ÃÓ–¥◊ÓºÚ’˚ ˝±»)£¨¿‰»¥–ßπ˚◊Ó∫√°£
(2)÷∏≥ˆ¡ΩÃı«˙œþ∑÷±±Ì 浃æþÃÂ∫¨“£∫
«˙œþAB£∫°°°°°°°°°°°°°°°°°°°°°°°°°°°° £ª
«˙œþBC£∫°°°°°°°°°°°°°°°°°°°°°°°°°° °£
(3)Ω´10°Ê ±38%µƒ¬»ªØ∏∆»Ð“∫ΩµŒ¬µΩ®C40°Ê ±£¨œ¬¡–”–πÿÀµ∑®’˝»∑µƒ «°°°° (ÃÓ–Ú∫≈)°£
A£Æ¥À ±»Ð“∫¥¶”⁄≤ª±•∫Õ◊¥Ã¨°°
B£Æ»Ð“∫÷–Œˆ≥ˆ¡À¬»ªØ∏∆æßÃÂ
C£Æ»Ð“∫÷–“—æ≠”–±˘Œˆ≥ˆ°°°° °°°°
D£Æ¥À ±±˘°¢¬»ªØ∏∆æßÃÂ∫Õ¬»ªØ∏∆±•∫ջГ∫π≤¥Ê
E£Æ¥À ±¬»ªØ∏∆æßÃÂ∫Õ¬»ªØ∏∆±•∫ջГ∫π≤¥Ê
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com