
4.根据下列哪项能判断镁带的燃烧是化学变化
A.发出耀眼强光 B.生成白色固体 C.放出大量的热 D.以上各项中的任意一项
3.每年的6月5日世界环境日,环境保护是我国的一项基本国策,空气的净化日益受到人们的关注。下列气体组中的各种气体都属于空气污染物的是
A.二氧化硫 一氧化碳 二氧化氮 B.二氧化碳 一氧化碳 氮气
C.氧气 二氧化碳 氮气 D.氮气 氧气 一氧化碳
2.下列实验操作不正确的是
A.点燃镁带必须用坩埚钳夹持,不能用手拿
B.实验过程中的废液应倒入水池,并用大量水冲刷
C.向试管中加铜绿粉末时可以用纸槽代替药匙加入药品
D.实验结束时要整理好实验台后方能离开实验室
1.下列现象与铜绿无关的是
A.遇到稀盐酸时放出大量气泡 B.加热一段时间后变成黑色粉末
C.加热时试管口有水滴滴出 D.在空气中燃烧产生耀眼强光
29.甲同学在某食品包装袋内,发现有一个装有白色颗粒固体A的小纸袋,上面写着“生石灰干燥剂,请勿食用”。甲同学随手将小纸袋拿出来放到空气中,经过一段时间后,发现纸袋内的白色颗粒粘在一起成为块状固体B。请你与甲同学一起对块状固体B的成分进行探究。
(1)猜想一:块状固体B中除氧化钙外还可能有__________、_______。写出白色颗粒固体A在空气中转化为块状固体B的化学反应方程式________________________、________________________________。
(2)猜想二:块状固体溶于水可能有________现象(填“放热”或“吸热”)。请你设计实验验证你这一猜想_____________________________________________。
(3)取适量固体B加入盛有一定量水韵试管中,振荡、静置、过滤,得到白色固体C,就白色固体C的成分,甲、乙两同学进行讨论一起猜想。
甲:白色固体C可能是Ca(OH)2; 乙:白色固体C可能是CaCO3;
你认为白色固体C还可能是________________________。
设计实验证明你的猜想(写出有关的实验步骤、现象和结论)
|
实验步骤 |
现象及结论 |
|
|
|
28.小林同学发现铜制的眼镜框表面出现了绿色物质,通过化学学习知道该物质为铜锈,俗称铜绿,主要成分是Cu2(OH)2CO3。
[提出问题]:铜是在什么条件下锈蚀的?
[猜 想]:根据铜锈的化学式,猜想铜生锈可能是铜与水、________、 ________共同作用的结果。
[设计与实验]:借鉴“铁钉锈蚀条件的探究”实验,小林设计了“铜片锈蚀条件的探究”实验.如图所示:
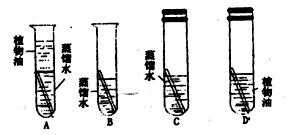
(1)实验较长时间后,发现________试管中的光亮铜片最先生锈(填序号)
(2)从优化实验的角度考虑,A实验他只考虑了水这个单一条件,C试管中除光亮的铜片、蒸馏水外,还有另外一种物质为________;
(3)B试管中除光亮的铜片外,还有另外两种物质________________;从B 试管的试验中,获得的结论是________________________________________;反应的化学方程式是____________________________________________________________。
[评价与改进]:我认为小林设计的“铜片锈蚀条件的探究”实验还不够完善,要得出正确结论,还要补充一个实验是________________________。
[反思与小结]通过铜片锈蚀条件的探究实验,我获得的启示是____________________。
写出一种防止铁、铜等金属制品的生锈的具体办法_______________________________。
请你提出一条延长食品保质期的建议__________________________________________。
27.我国化学家侯德榜先生发明的“侯氏制碱法”的基本原理是:在浓氨水中通入足量的CO2气体生成一种盐,然后在此溶液中加入细小食盐粉末,由于NaHCO3在该状态下溶解度很小,呈晶体析出。同时由于NaHCO3不稳定,加热后生成纯碱、水和CO2气体。根据以上叙述简要回答:
(1)用上述方法进行生产时所用的起始原料________(写出它们的化学式,下同。)
(2)最终产品是________________。
(3)①有关反应的化学方程式是______________________;______________________;________________________。
②在第二步反应中加入的是细小的食盐粉末,食盐磨细的目的是_______________。
(4)该生产过程中没有涉及的基本反应类型是________________。
(5)有人认为“候氏制碱法”的优点有四:
A.生产过程中部分产品可选为起始原料使用
B.副产品是一种可利用的氮肥
C.反应不需要加热
D.副产品不会造成环境污染
你认为其中正确的是________(用序号回答)。
26.某活动小组从工厂收集到了一些含有AgNO3的废液以及铁屑和锌屑的混合物。在回收银时他们将一定量的上述金属混合物加入到AgNO3的溶液中,充分反应后过滤,得到固体和浅绿色滤液(所含其它杂质不考虑)。为了探究滤液中溶质的组成,他们做出下列猜想:
①溶液为Fe(NO3)2; ②溶液为Fe(NO3)2和AgNO3;
③溶液为Zn(NO3)2和Fe(NO3)2; ④溶液为Zn(NO3)2、Fe(NO3)2和AgNO3
(1)上述猜想中,错误的是(填序号)________,其原因是________________________。
(2)有的同学认为滤液中溶质只有Zn(NO3)2,你认为是否正确?________________其原因是________________________________。
(3)某同学将一铜片放入滤液中,目的是________________________________。一段时间后铜片没有变化,上述正确猜想中可排除的是(填序号)_______________。
25.以下是同学们在学习溶液知识时实验报告中的部分内容,分析后请回答:
|
试管编号 |
加入液体 |
加入物质 |
现象 |
|
1 |
10ml水 |
少量食盐 |
不溶 |
|
2 |
10ml乙醇 |
少量食盐 |
溶解 |
|
3 |
10ml水 |
几小颗粒碘 |
不溶 |
|
4 |
10ml乙醇 |
几小颗粒碘 |
溶解 |
(1)在同一条件下,物质的溶解能力与________和________有关。
(2)除(1)中因素外,你认为固体物质的溶解能力还与外界条件________有关。如果外界条件和溶剂的种类确定,要比较硝酸钾和氯化钠的溶解能力,实验中需要控制的因素是________________________。
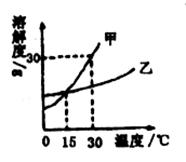
(3)根据上图甲、乙两种固体物质的溶解度曲线,你能获得的信息是(答出两条即可)________________________________;________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com