
18.有A、B、C、D、E、F六瓶不同物质的溶液,它们分别是NH3·H2O、Na2CO3、MgSO4、
NaHCO3、HNO3和BaCl2溶液中的一种。为了鉴别它们,各取少量溶液进行两两混合,实验结果如表所示,表中“↓”表示生成沉淀,“↑”表示生成气体,“-”表示观察不到明显现象,空格表示实验未做。试推断其中F是( )
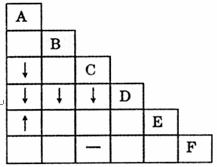
A.NaHCO3溶液 B.BaCl2溶液
C.MgSO4溶液 D.Na2CO3溶液
|
第II卷共7个小题。
17.碳酸铜和碱式碳酸铜[Cu2(OH)2CO3]均可溶于盐酸转化为氯化铜。在高温下这两种化合物均能分解生成氧化铜。溶解28.4g的上述混合物,消耗1.0mo·L-1盐酸l500mL。灼烧等量的上述混合物,得到的氧化铜质量是 ( )
A.15g B.20g C.30g D.35g
16.下表是四个反应的有关信息:
|
序号 |
氧化剂 |
还原剂 |
其它反应物 |
氧化产物 |
还原产物 |
|
① |
Cl2 |
FeBr2 |
|
|
FeCl3 |
|
② |
KMnO4 |
H2O2 |
H2SO4 |
O2 |
MnSO4 |
|
③ |
KClO3 |
HCl(浓) |
|
Cl2 |
Cl2 |
|
④ |
KMnO4 |
HCl(浓) |
|
Cl2 |
MnCl2 |
下列结论正确的是 ( )
A.第①组反应的氧化产物一定只有FeCl3(实为Fe3+)
B.氧化性比较:KMnO4>Cl2>Fe3+>Br2>Fe2+
C.还原性比较:H2O2>Mn2+>Cl-
D.第③组反应的产物还有KCl和H2O
15.X、Y、Z、M、N分别代表五种金属。有以下化学反应 ( )
①水溶液中:X+Y2 === X2+Y
②Z+2H2O(冷)=== Z(OH)2+H2↑
③M、N为电极与N盐溶液组成原电池,发生的电极反应为:M→M2++2e-
④Y可以溶于稀H2SO4中,M不被稀H2SO4氧化,则这五种金属的活动性由弱到强的顺序是
A.N<M<Y<X<Z B.N<M<X<Y<Z
C.M<N<Y<X<Z D.X<Z<N<M<Y
14.据媒体报道:以氢氧燃料电池为动力的公交车即将试运行。质子交换膜燃料电池(PEMFC)常作为电动汽车的动力源。该燃料电池(如图所示)以氢气为燃料,空气为氧化剂,铂作催化剂,用磺酸类物质作溶剂(导电离子是H+)。下列对该燃料电池的描述中正确的是 ( )
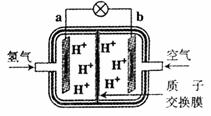
A.b为电池的负极
B.负极的反应式为:4H++O2+4e-→2H2O
 C.氢离子在电解质溶液中向b极移动
C.氢离子在电解质溶液中向b极移动
D.总的化学反应可表示为:2H2+O2 2H2O
13.下列反应的离子方程式正确的是 ( )
A.碳酸氢钠溶液与少量石灰水反应:
HCO-3+Ca2++OH-=CaCO3↓+H2O
B.单质铜与稀硝酸反应:Cu+2H++2NO3-=Cu2++2NO↑+H2O
C.向Fe(NO3)2溶液中加入盐酸:
3Fe2++4H++NO3- === 3Fe3++NO↑+2H2O
D.铝片跟氢氧化钠溶液反应:Al+2OH-+2H2O = [Al(OH)4]+H2↑
12.化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)的能量。已知白磷(P4)和P4O6的分子结构如下图所示;现提供以下化学键的键能:P-P198kJ·mol-1、P-O360kJ·mol-1、氧气分子内氧原子间的键能为498kJ·mol-1。则P4+3O2=P4O6的反应热△H为 ( )
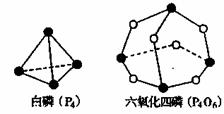
A.+1638kJ·mol-1 B.-1638kJ·mol-1
C.-126kJ·mol-1 D.+126kJ·mol-1
11.某溶液中含有HCO3-、SO2-3、CO2-3、CH3COO-等四种阴离子,向其中加入足量的Na2O2固体后,假设溶液体积无变化,溶液中离子浓度基本保持不变的是 ( )
A.CO2-3 B.HCO3- C.SO2-3 D.CH3COO-
9.目前,人类已经发现的非金属元素除稀有气体元素外有16种,下列对这16种非金属元素的判断不正确的是 ( )
①都是主族元素,原子的最外层电子数都大于3
②单质在反应中都只能作氧化剂
③对应的含氧酸都是强酸
④氢化物常温下都是气态,所以又叫气态氢化物
⑤气态氧化物与水反应都不会再生成气体
A.全部 B.只有①② C.只有①②③④ D.只有①②④⑤
|
A.电池反应为2Ag++Cu=2Ag+Cu2+的原电池中,铜作负极
B.电解法精炼粗铜时,精铜作阴极
C.铁的吸氧腐蚀的负极反应为2H2O+O2+4e- →4OH-
D.在镀件上镀铜时,铜作阳极
8.对于某些离子的检验及结论一定正确的是 ( )
A.加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32-
B.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42-
C.加入氢氧化钠溶液并加热,产生的气体能使湿润的红色石蕊试纸变蓝,一定有NH4+
D.加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com