
2.下列电子式书写正确的是 ( )

1.下列物质在变化过程中,只需克服分子间作用力的是 ( )
A.明矾溶解于水 B.高温下铁的熔化
C.干冰升华 D.氯化铵的“升华”
23.(7分)工业制备氯化铜时,常将浓盐酸用蒸汽加热到80℃左右,慢慢加入粗CuO粉末(含有杂质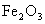 、
、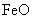 )充分反映,使之溶解,得到强酸性的混合溶液,欲从该混合溶液中制备纯净的
)充分反映,使之溶解,得到强酸性的混合溶液,欲从该混合溶液中制备纯净的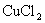 溶液。请参照下表给出的数据回答下列问题:
溶液。请参照下表给出的数据回答下列问题:
|
部分金属阳离子 |
 |
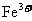 |
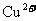 |
|
以氢氧化物形式沉淀完全是的pH |
≥9.6 |
≥3.7 |
≥6.4 |
(1)第一步出去 ,能否直接调整pH=9.6将
,能否直接调整pH=9.6将 转化为沉淀出去 (填“能”或“否”);理由是 。
转化为沉淀出去 (填“能”或“否”);理由是 。
若用强氧化剂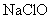 将
将 氧化为
氧化为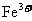 ,则加入
,则加入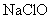 后,溶液的pH的变化是 。
后,溶液的pH的变化是 。
A.一定增大 B.一定减小 C.可能增大 D.可能减小
(2)除去溶液中的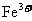 的方法是调整溶液的pH=3.7,现有下列试剂均可使强酸性溶液的pH调整到3.7,可选用的有
。
的方法是调整溶液的pH=3.7,现有下列试剂均可使强酸性溶液的pH调整到3.7,可选用的有
。
A.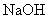 B.氨水 C.
B.氨水 C.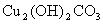 D.
D.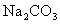 E.
E.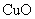 F.
F.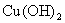
(3)亚铁盐在溶液中易被氧化,而实验室中需要纯净的亚铁盐溶液,那么保存亚铁盐溶液时应该如何防止亚铁盐氧化?
22.(7分)现有25℃时0.1mol/L的氨水,请回答以下问题:
(1)若向氨水中加入少量硫酸铵固体,此时溶液中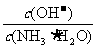 ,
,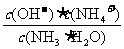 (填“增大”“减小”或“不变”)
(填“增大”“减小”或“不变”)
(2)若向氨水中加入稀硫酸,使其恰好完全中和,写出反应的离子方程式 。
(3)若向氨水中加入稀硫酸至溶液的pH=7,此时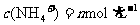 ,则
,则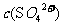 =
。
=
。
(4)若向氨水中加入pH=1的硫酸,且氨水与硫酸的体积比为1∶1;则所得溶液中各离子物质的量浓度由大到小的顺序是 。
21.(5分)一定条件下,在容积为1L的密闭容器中发生可逆反映: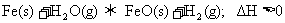 。在1000℃时,
。在1000℃时,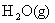 的平衡转化率
的平衡转化率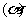 与体系总压强
与体系总压强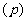 的关系如图所示:
的关系如图所示:
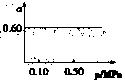
(1)写出该反应的平衡常数表达式K= ;当反应达到平衡后,再向容器中加入铁粉和水蒸气,则K ;升高温度,则K (后两空填“增大”“减小”或“不变”)。
(2)在1000℃时,若向上述容器中加入0.80mol铁粉和1.00mol水蒸气,达到平衡是,容器中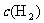 =
。
=
。
20.(11分)短周期元素A、B、C、D、E的原子序数依次增大,它们的原子核外电子层数之和为10;B的化合物种类繁多,数目庞大。C、D是空气中含量最多的两种元素;D、E两单质可形成两种不同的离子化合物。
(1)写出E的单质与A、D两元素形成的常见化合物反应的离子方程式 。
(2)由A、C、D三种元素所形成的常见盐溶液呈 性(填“酸”“中”或“碱”),其原因用离子方程式表示为 。
(3)B的相对分子质量最小的氢氧化物的燃烧为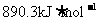 ,写出其燃烧的热化学方程式
。
,写出其燃烧的热化学方程式
。
(4)X、Y是均由C、D两元素组成的化合物,且C、D在X、Y中的价态相同,某温度下相互转化时的量变关系如图所示:
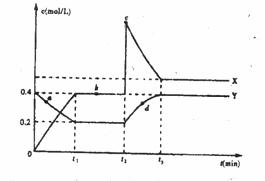
①X的化学式是 。
②图中a、b、c、d四点中,表示反应处于平衡状态的是 。
③该温度下,反应物Y转化为X的平衡常数为 。
④反应进行到t2时刻,改变的条件可能是 。
19.(12分)如图,p、q为直流电源两极,A由+2价金属单质X制成,B、C、D为铂电极,接通电源,金属X沉积于B极,同时C、D产生气泡。试回答:
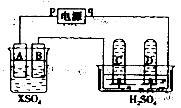
(1)p为 极,A极发生了 反应(填反应类型)。
(2)C为 极,试管里收集到 ;D为 极,试管里收集到 。
(3)C极的电极方程式是 。
(4)在电解过程中,测得C、D两极上产生的气体的实验数据如下:
|
时间(min) |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
阴极生成气体体积(cm3) |
6 |
12 |
20 |
29 |
39 |
49 |
59 |
69 |
79 |
89 |
|
阳极生成气体体积(cm3) |
2 |
4 |
7 |
11 |
16 |
21 |
26 |
31 |
36 |
41 |
仔细分析上表,请说出得到以上实验数据可能的原因是 。
(5)当反应进行一段时间后,A、B电极附近溶液的pH (填“增大”、“减小”或“不变”)。
(6)当电路中通过0.004mol电子时,B电极上沉淀金属X的质量为0.128g,则此金属的摩尔质量为 。
18.(7分)下列中学化学中常见的物质的转化关系图中,反应条件及部分反应物和产物未全部注明,已知A、D为金属单质,其它为化合物。
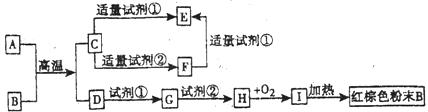
试判断:
(1)写出物质的化学式:A C I
(2)写出下列反应的方程式:
C→F的离子方程式
H→I的化学方程式
17.X、Y、Z是3种短周期元素,其中X、Y位于同一主族,Y、Z位于同一周期。X原子的最外层电子数是其电子层数的3倍。Z原子的核外电子数比Y原子少1。下列说法不正确的是
A.元素非金属行由弱到强的顺序为Z>Y>X
B.Y元素最高价氧化物对应水化物的化学式可表示为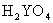
C.3种元素的气态氢化物中,Z的气态氢化物最稳定
D.原子半径有大到小的顺序为Z>Y>X
第Ⅱ卷(非选择题,共49分)
16.可逆反应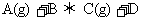 达到平衡是,下列说法不正确的是
达到平衡是,下列说法不正确的是
A.若增大A的浓度,平衡体系颜色加深,D不一定是具有颜色的气体
B.增大压强,平衡不移动,说明B、D必是气体
C.升高温度,C的百分含量减小,说明正反应是放热反应
D.若B是气体,增大A的浓度会使B的转化率增大
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com