
12.14g铁粉全部溶于某稀硝酸中,恰好反应,放出NO气体后得到溶液1L。称量所得溶液,发现比原硝酸溶液增重8g。则原溶液中硝酸的浓度为 ( )
A.0.6mol/L B.0.8 mol/L C.1.2 mol/L D.无法计算
11.如图所示下列叙述正确的是 ( )
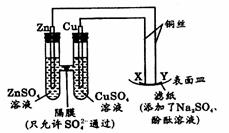
A.Y为阴极,发生还原反应
B.X为正极,发生氧化反应
C.Y与滤纸接触处有氧气生成
D.X与滤纸接触处变红
9.X和Y属于1-18号元素,X原子的最外层电子数是次外层电子数的一半;Y原子比X原子少一个或两个电子层,且最外层只有一个电子,则下列说法正确的是 ( )
A.两种元素的原子序数之差必小于10
B.可能形成XY、XY4(或Y4X)型化合物,每种原子达到8电子稳定结构
C.所形成的化合物都属于离子化合物
D.X与Y形成的化合物都具有较强的还原性
|
A.锌是正极,氧化银是负极
B.正极的电极反应式为Ag2O+H2O+2e-→2Ag+2OH-
C.溶液中OH-向正极移动,K+、H+向负极移动
D.在电池放电过程中,电解质溶液的酸碱性基本保持不变
8.向一定的K2CO3溶液中缓慢地滴加稀盐酸,并不断搅拌。随着盐酸的加入,溶液中离子数目也相应地发生变化。如图所示,四条曲线与溶液中的离子的对应关系,完全正确的是 ( )
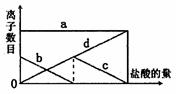
A.a:Cl-;b:K+;c:CO32-;d:HCO3-
B.a:K+;b:CO32-;c:Cl-;d:HCO3-
C.a:K+;b:CO32-;c:HCO3-;d:Cl-
D.a:K+;b:HCO3-;c:Cl-;d: CO32-
7.短周期的A、B两种元素,A原子半径小于B原子半径,两种元素可形成A是正价的AB2型化合物,下列关于两元素的叙述正确的是
①A、B可能属于同一周期 ②A是B的前一周期元素
③A只能是金属元素 ④A可能是第二周期ⅡA族或ⅣA族元素
下列选项正确的是 ( )
A.①③ B.②③ C.②④ D.②③④
6.自然界中存在一种尖晶石,主要成分的化学式可表示为MgAl2O4,可作为宝石。已知该尖晶石中混有Fe2O3。取一定量样品5.4g,恰好完全溶解在一定浓度100mL盐酸溶液中,则盐酸浓度可能是 ( )
A.1.2 mol·L-1 B.2.8 mol·L-1 C.3.6 mol·L-1 D.4.9 mol·L-1
5.下列反应的离子方程式书写正确的是 ( )
A.过量的铁与浓硝酸反应:Fe+6H++3NO3-=Fe3++3NO2↑+3H2O
B.1mol·L-1的Na[Al(OH)4]溶液和2.5mol·L-1的盐酸等体积混合:
2[Al(OH)4]-+5H+=Al(OH)3↓+Al3++5H2O
C.次氯酸钙溶液中通入过量CO2:2ClO-+CO2+H2O=2HClO+CO32-
D.在碳酸氢镁溶液中通入过量Ca(OH)2溶液:
Mg2++2HCO3-+Ca2++2OH-=MgCO3↓+CaCO3↓+2H2O
4.NA代表阿伏加德罗常数,下列叙述不合理的是 ( )
A.常温常压下,22.4L N2所含的分子数小于NA
B.有1mol CH3COO-的醋酸钠溶液中,Na+数目略大于NA
C.8.0gCu2S和CuO的混合物中含有铜原子数为0.1NA
D.0.1mol Fe与0.1mol Cl2充分反应,转移的电子数为0.3NA
3.将下列各组溶液进行相互反应,根据溶液加入的先后顺序和反应过程中出现的现象,就可以进行鉴别的是 ( )
A.稀硫酸和NaHCO3溶液 B.CaCl2溶液和Na2CO3溶液
C.Ba(OH)2溶液和NaHSO4溶液 D.KOH和Al2(SO4)3溶液
2.生产原子弹的重要核燃料是高浓缩的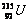 或
或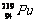 ,天然纯铀中
,天然纯铀中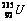 含量极低(0.7%,
含量极低(0.7%,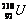 占99.3%),
占99.3%),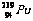 在自然界中不存在。
在自然界中不存在。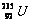 浓缩一直成为国际社会关注的焦点。下列说法正确的是 ( )
浓缩一直成为国际社会关注的焦点。下列说法正确的是 ( )
A.U和Pu都属于放射性元素,二者互为同素异形体
B.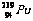 原子核外电子数为145
原子核外电子数为145
C.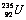 与
与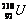 互为同位素,通常只能采用物理分离方法
互为同位素,通常只能采用物理分离方法
D.核反应能量与燃料燃烧的化学反应释放能量的原理相同
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com