
1Θ°œ¬Ν––π ω’ΐ»ΖΒΡ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ (ΓΓΓΓ )
ΓΓΓΓΓΓ AΘ°ΝρΥαΓΔ¥ΩΦνΓΔ¥ΉΥαΡΤΚΆ…ζ ·Μ“Ζ÷±π τ”ΎΥαΓΔΦνΓΔ―ΈΚΆ―θΜ·Έο
ΓΓΓΓΓΓ BΘ°≤ΜΆ§ΒΡΤχΧεΘ§»τΧεΜΐ≤ΜΒ»Θ§‘ρΥϋΟ«ΥυΚ§ΒΡΖ÷Ή” ΐ“ΜΕ®≤ΜΒ»
ΓΓΓΓΓΓ CΘ°Φ“”Ο“ΚΜ·ΤχΓΔΧλ»ΜΤχ“‘ΦΑΥ°ΟΚΤχΒΡΈο÷ ≥…Ζ÷ΕΦ τ”Ύ”–ΜζΈο
ΓΓΓΓΓΓ DΘ°Κ§”–“θάκΉ”ΒΡΜ·ΚœΈο“ΜΕ®Κ§”–―τάκΉ”
31Θ°œρ8gΕΰΦέΫπ τΒΡ―θΜ·ΈοΙΧΧε÷–Φ”»κœΓH2SO4Θ§ ΙΤδ«ΓΚΟΆξ»Ϊ»ήΫβΘ§“―÷ΣΥυœϊΚΡΒΡΝρΥαΧεΜΐΈΣ100mlΓΘ‘ΎΥυΒΟ»ή“Κ÷–≤ε»κ≤§ΒγΦΪΫχ––ΒγΫβΘ§Ά®Βγ“ΜΕΈ ±ΦδΚσΘ§‘Ύ“ΜΗωΒγΦΪ…œ ’–≈ΒΫ224ml―θΤχ(±ξΉΦΉ¥Ωω)Θ§‘ΎΝμ“ΜΗωΒγΦΪ…œΈω≥ωΗΟΫπ τ1.28gΓΘ
ΓΓ (1)ΗυΨίΦΤΥψ»ΖΕ®Ϋπ τ―θΜ·ΈοΒΡΟϊ≥ΤΓΘ
ΓΓ (2)ΦΤΥψΆ®ΒγΚσΝρΥα»ή“ΚΒΡΈο÷ ΒΡΝΩ≈®Ε»(»ή“ΚΧεΜΐΑ¥100mlΦΤΥψ)ΓΘ
30Θ°(14Ζ÷)Ρ≥―–ΨΩ–‘―ßœΑ–ΓΉιΒΡΆ§―ßΕ‘¬ΧΖ· ή»»Ζ÷ΫβΒΡ«ιΩωΫχ––ΧΫΨΩΓΘ
ΓΓ (1)Ή Νœ±μΟςΘ§‘ΎΦ”»»ΧθΦΰœ¬»ΐ―θΜ·ΝρΨΏ”–±»Ϋœ«ΩΒΡ―θΜ·–‘ΓΘΦΉΆ§―ß»œΈΣΘ§¬ΧΖ· ή»»Ζ÷ΫβΒΡ≤ζΈο «FeOΓΔSO3ΓΔH2OΓΘΡψ÷ß≥÷ΦΉΆ§―ßΒΡΙέΒψ¬πΘΩΥΒΟςΡψΒΡάμ”…
ΓΓΓΓΓΓΓΓ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΘΜ
ΓΓ (2) Β―ι «ΫβΨωΈ ΧβΒΡ÷Ί“Σ ÷ΕΈΓΘ““Ά§―ß”Ο»γœ¬ΉΑ÷ΟΆ®Ιΐ Β―ιά¥ΧΫΨΩ¬ΧΖ· ή»»Ζ÷ΫβΒΡ≤ζΈο«ιΩω(Φ”»»ΦΑΦ–≥÷ΉΑ÷ΟΈ¥Μ≠≥ω)ΘΚ
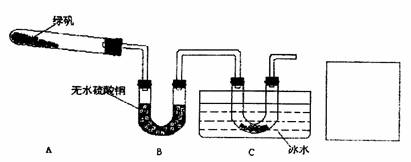
ΓΓΓΓ Β―ιΙΐ≥Χ÷–ΖΔœ÷ΘΚΉΑ÷ΟA÷–”–≤–ΝτΙΧΧεΘ§ΉΑ÷ΟB÷–ΈόΥ°ΝρΥαΆ≠±δάΕΘ§ΉΑ÷ΟC÷–ΒΡU–Έ
Ιή÷–”–Έό…ΪΨßΧε≥ωœ÷ΓΘΜΊ¥πœ¬Ν–Έ ΧβΘΚ
ΔΌ‘ΎΉΑ÷ΟCΒΦΙή≥ωΩΎ¥ΠΜΙ”Π”–ΒΡ Β―ιœ÷œσ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΘΜ
ΔΎΉΑ÷ΟA÷–≤–ΝτΒΡΙΧΧε «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΘΜΉΑ÷ΟC÷–ΒΡU–ΈΙή÷–Έό…ΪΨßΧε «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΘΜ
Δέ““Ά§―ßΈΣΝΥ―ι÷Λ¬ΧΖ· ή»»Ζ÷ΫβΒΡΥυ”–≤ζΈοΘ§‘ΎCΉΑ÷ΟΚσΝ§Ϋ”ΝΥ“ΜΗωΉΑ÷ΟΘ§≤Δ―Γ”ΟΝΥΚœ ΒΡ“©ΤΖ≤ΜΫω¥οΒΫΝΥ Β―ιΡΩΒΡΒΡΕχ«“ΜΙΤπΒΫΝΥ“ΜΨΌΝΫΒΟΒΡ–ßΙϊΓΘ«κΡψ‘ΎCΉΑ÷ΟΚσΒΡΖΫΩρ÷–Μ≠≥ωΗΟΉΑ÷ΟΘ§≤ΔΉΔΟς―Γ”ΟΒΡ“©ΤΖΓΘ
Δή–¥≥ω¬ΧΖ· ή»»Ζ÷ΫβΒΡΜ·―ßΖΫ≥Χ ΫΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
29Θ°(12Ζ÷)≤βΕ®ΝρΥαΆ≠ΨßΧε(CuSO4ΓΛ5H2O)άοΫαΨßΒΡΥ°ΒΡΚ§ΝΩΘ§ Β―ι≤Ϋ÷ηΈΣ
(1)―–ΡΞΘΜ
(2)‘Ύέαέω÷–≥ΤΝΩ―υΤΖmgΘ§≤ΔΦ«¬ΦΉΑ”– ‘―υΒΡέαέωΒΡ÷ ΝΩm1gΘΜ(3)Φ”»»ΘΜ(4)ά以ΘΜ
(5)≥ΤΝΩΘΜ(6)÷ΊΗ¥(3)-(5)ΒΡ≤ΌΉςΘ§÷±ΒΫΝ§–χΝΫ¥Έ≥ΤΝΩΒΡ÷ ΝΩ≤ν≤Μ≥§Ιΐ0.1gΈΣ÷ΙΘ§Φ«¬ΦΉνΚσΥυΒΟ ΐΨίm2gΘΜ(7)ΗυΨίΚΆ Β―ιΉ ΝœΦΤΥψΝρΥαΆ≠ΫαΨßΥ°Κ§ΝΩΓΘ«κΜΊ¥πœ¬Ν–Έ ΧβΓΘ
ΓΓ (1)œ÷”–έαέωΓΔέαέω«·ΓΔ»ΐΫ≈ΦήΓΔΡύ»ΐΫ«ΓΔ≤ΘΝßΑτΓΔΆ–≈ΧΧλΤΫ(¥χμά¬κ)ΓΔ“©≥ΉΓΔΝρΥα
ΓΓΓΓΓΓΓΓ Ά≠ΨßΧε―υΤΖΒ» Β―ι”ΟΤΖΘ§Ϋχ––ΗΟ Β―ι ±Θ§»±…ΌΒΡ Β―ι”ΟΤΖ «ΘΚΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
ΓΓ(2)‘Ύ”ΟΆ–≈ΧΧλΤΫ≥ΤΝΩΩ’έαέωΒΡ÷ ΝΩ ±Θ§»γΙϊΧλΤΫΒΡ÷Η±ξœρΉσΤΪΉΣΘ§ΥΒΟς
ΓΓΓΓΓΓ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
ΓΓ(3)ΗΟ Β―ι÷–≤Ϋ÷η(4)”Π‘ΎΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ (Χν“«ΤςΟϊ≥Τ)÷–Ϋχ––Θ§’β―υ≤ΌΉςΒΡΡΩΒΡ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΘ§Ζώ‘ρ≤βΕ®ΫαΙϊΜαΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ (ΧνΤΪΗΏΓΔΤΪΒΆ)
ΓΓ (4) Β―ι≤Ϋ÷η(6)ΒΡΡΩΒΡ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
ΓΓ (5)ΗυΨί≤βΒΟΒΡΉ ΝœΘ§ΦΤΥψΙέΝρΥαΆ≠ΨßΧεάοΫαΨßΒΡΥ°ΒΡΖ÷Ή” ΐΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
ΓΓ (6)»τ≤ΌΉς’ΐ»ΖΕχ Β―ι≤βΒΟΝρΥαΆ≠ΨßΧε÷–ΫαΨßΒΡΥ°Κ§ΝΩΤΪΒΆΘ§Τδ‘≠“ρΩ…Ρή”–(Χν―ΓœνΒΡ±ύΚ≈)ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
AΘ°±Μ≤β―υΤΖ÷–Κ§”–Φ”»»≤ΜΜ”ΖΔΒΡ‘”÷
BΘ°±Μ≤β―υΤΖ÷–Κ§”–Φ”»»“ΉΜ”ΖΔΒΡ‘”÷
CΘ° Β―ι«Α±Μ≤β―υΤΖ“―”–≤ΩΖ÷ ßΥ°
DΘ°Φ”»»«ΑΥυ”ΟέαέωΆξ»ΪΗ…‘ο
28Θ°(8Ζ÷)Ά®≥Θ»ΥΟ«Α―≤πΩΣ1molΡ≥Μ·―ßΦϋΥυΈϋ ’ΒΡΡήΝΩΩ¥≥…ΗΟΜ·―ßΦϋΒΡΦϋΡήΓΘΦϋΡήΒΡ¥σ–Γ
Ω…ΚβΝΩΜ·―ßΦϋΒΡ«Ω»θΘ§“≤Ω…”Ο”ΎΙάΥψΜ·―ßΖ¥”ΠΒΡΖ¥”Π»»(ΓςH)Θ§Μ·―ßΖ¥”ΠΒΡΓςHΒ»”ΎΖ¥”Π÷–ΕœΝ―Ψ…Μ·―ßΦϋΒΡΦϋΡή÷°ΚΆ”κΖ¥”Π÷––Έ≥…–¬Μ·―ßΦϋΒΡΦϋΡή÷°ΚΆΒΡ≤νΓΘ
|
Μ·―ßΦϋ |
Si-O |
Si-Cl |
H-H |
H-Cl |
Si-Si |
Si-C |
|
ΦϋΡή/kJΓΛmol-1 |
460 |
360 |
436 |
431 |
176 |
347 |
«κΜΊ¥πœ¬Ν–Έ ΧβΘΚ
ΓΓ (1)±»Ϋœœ¬Ν–ΝΫΉιΈο÷ ΒΡ»έΒψΗΏΒΆ(ΧνΓΑ>Γ±ΜρΓΑ<Γ±)SiCΓΓΓΓΓΓΓΓΓΓ SiΘΜSiCl4ΓΓΓΓΓΓΓΓΓΓ SiO2
ΓΓ (2)”“ΆΦΝΔΖΫΧε÷––ΡΒΡΓΑΓώΓ± ±μ ΨΙηΨßΧε÷–ΒΡ“ΜΗω‘≠Ή”Θ§«κ‘ΎΝΔΖΫΧεΒΡΕΞΒψ”ΟΓΑΓώΓ±±μ Ψ≥ω”κ÷°Ϋτ
|
ΓΓ (3)ΙΛ“Β…œΗΏ¥ΩΙηΩ…Ά®Ιΐœ¬Ν–Ζ¥”Π÷Τ»ΓΘΚSiCl4(g)+2H2(g)ΓΓΓΓ Si(s)+4HCl(g)
ΓΓΓΓΓΓΓΓ ΗΟΖ¥”ΠΒΡΖ¥”Π»»ΓςH=ΓΓΓΓΓΓΓΓΓΓ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
27Θ°(9Ζ÷)Ϋώ”–“ΜΜλΚœΈοΒΡΥ°»ή“ΚΘ§÷ΜΩ…ΡήΚ§”–“‘œ¬άκΉ”÷–ΒΡ»τΗ…÷÷ΘΚK+ΓΔNH4+ΓΔCl-ΓΔMg2+ΓΔBa2+ΓΔCO32-ΓΔSO42-Θ§œ÷»Γ»ΐΖί100mL»ή“ΚΫχ––»γœ¬ Β―ιΘΚ
ΓΓ (1)ΒΎ“ΜΖίΦ”»κAgNO3»ή“Κ”–≥ΝΒμ≤ζ…ζ
ΓΓ (2)ΒΎΕΰΖίΦ”ΉψΝΩNaOH»ή“ΚΦ”»»ΚσΘ§ ’Φ·ΒΫΤχΧε0.04mol
ΓΓ (3)ΒΎ»ΐΖίΦ”ΉψΝΩBaCl2»ή“ΚΚσΘ§ΒΟΗ…‘ο≥ΝΒμ6.27gΘ§Ψ≠ΉψΝΩ―ΈΥαœ¥Β”ΓΘΗ…‘οΚσΘ§≥ΝΒμ÷ ΝΩΈΣ2.33gΓΘΗυΨί…œ ω Β―ιΘ§Ής≥ω≈–ΕœΘΚ
ΓΓΓΓΓΓΓΓ ΗΟ»ή“Κ÷–“ΜΕ®¥φ‘ΎΒΡ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
ΓΓ ΓΓΓΓΓΓΗΟ»ή“Κ÷–“ΜΕ®≤Μ¥φ‘ΎΒΡ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
ΓΓΓΓΓΓΓΓ ΗΟ»ή“Κ÷–Ω…Ρή¥φ‘ΎΒΡ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
26Θ°(11Ζ÷)“―÷ΣFeBr2»ή“Κ÷–Ά®»κΉψΝΩΒΡCl2 ±…ζ≥…FeCl3ΚΆBr2ΓΘΨί¥ΥΜΊ¥πœ¬Ν–Έ ΧβΓΘ
(1)–¥≥ωΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ Ϋ≤Δ±ξ≥ωΒγΉ”ΉΣ“ΤΒΡΖΫœρΚΆ ΐΡΩΓΘ
ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
ΓΓ (2)Β±”–12Ηωe-ΉΣ“Τ ±Θ§±ΜΜΙ‘≠ΒΡΈο÷ Ζ÷Ή” ΐ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
ΓΓ (3)÷Η≥ω―θΜ·ΦΝΚΆΜΙ‘≠ΦΝΓΘ―θΜ·≤ζΈοΚΆΜΙ‘≠≤ζΈοΘ§Χν»κœ¬±μ
|
―θΜ·ΦΝ |
ΜΙ‘≠ΦΝ |
―θΜ·≤ζΈο |
ΜΙ‘≠≤ζΈο |
|
ΓΓ |
ΓΓ |
ΓΓ |
ΓΓ |
25Θ°(12Ζ÷)ΒγΫβ‘≠άμ‘ΎΜ·―ßΙΛ“Β÷–”–ΙψΖΚ”Π”ΟΓΘœ¬ΆΦ±μ Ψ“ΜΗωΒγΫβ≥ΊΘ§ΉΑ”–ΒγΫβ“ΚaΘΜXΓΔY «ΝΫΩιΒγΦΪΑεΘ§Ά®ΙΐΒΦœΏ”κ÷±ΝςΒγ‘¥œύΝ§ΓΘ«κΜΊ¥π“‘œ¬Έ ΧβΘΚ
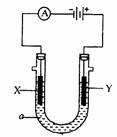
ΓΓ (1)»τXΓΔYΕΦ «Εη–‘ΒγΦΪΘ§a «±ΞΚΆNaCl»ή“ΚΘ§ Β―ιΩΣ Φ ±Θ§Ά§ ±‘ΎΝΫ±ΏΗςΒΈ»κΦΗΒΈΖ”ΧΣ ‘“ΚΘ§‘ρ
ΓΓΓΓΓΓΓΓ ΔΌΒγΫβ≥Ί÷–XΦΪ…œΒΡΒγΦΪΖ¥”Π ΫΈΣΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
ΓΓΓΓΓΓΓΓΓΓ ‘ΎXΦΪΗΫΫϋΙέ≤λΒΫΒΡœ÷œσ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
ΔΎYΒγΦΪ…œΒΡΒγΦΪΖ¥”Π ΫΈΣΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΘ
ΓΓ Φλ―ιΗΟΒγΦΪΖ¥”Π≤ζΈοΒΡΖΫΖ® «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
ΓΓ (2)»γΙϊ“Σ”ΟΒγΫβΖΫΖ®ΨΪΝΕ¥÷Ά≠Θ§ΒγΫβ“Κa―Γ”ΟCuSO4»ή“ΚΘ§‘ρ
ΓΓΓΓΓΓΓΓ ΔΌXΒγΦΪΒΡ≤ΡΝœ «ΓΓΓΓΓΓΓΓΓΓΓΓ Θ§ΒγΦΪΖ¥”Π Ϋ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
ΔΎYΒγΦΪΒΡ≤ΡΝœ «ΓΓΓΓΓΓΓΓΓΓΓΓ Θ§ΒγΦΪΖ¥”Π Ϋ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
(ΥΒΟςΘΚ‘”÷ ΖΔ…ζΒΡΒγΦΪΖ¥”Π≤Μ±Ί–¥≥ω)
24Θ°(6Ζ÷)”ΟΔΌNa2CO3ΓΔΔΎNaOHΓΔΔέBaCl2ΓΔΔή―ΈΥαΉς ‘ΦΝΘ§≥ΐ»ΞNaCl»ή“Κ÷–Κ§”–…ΌΝΩCa2+ΓΔMg2+ΚΆSO42-άκΉ”(ΟΩ÷÷ ‘ΦΝ÷ΜΡή Ι”Ο“Μ¥Έ)ΓΘ
ΓΓΓΓ Φ”»κ ‘ΦΝΥ≥–ρΘΚΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
ΓΓΓΓ ”–ΙΊάκΉ”Ζ¥”ΠΖΫ≥Χ ΫΘΚ
ΓΓΓΓ ΒΎ“Μ≤ΫΘΚΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
ΓΓ ΓΓΒΎΕΰ≤ΫΘΚΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
ΓΓΓΓ ΒΎ»ΐ≤ΫΘΚΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
ΓΓΓΓ ΒΎΥΡ≤ΫΘΚΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
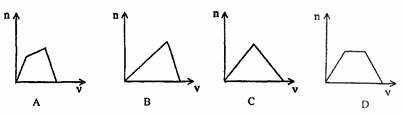
23Θ°ΫΪΉψΝΩCO2Ά®»κKOHΚΆCa(OH)2ΒΡΜλΚœœΓ»ή“Κ÷–Θ§…ζ≥…≥ΝΒμΒΡΈο÷ ΒΡΝΩ(n)ΚΆΆ®»κCO2ΧεΜΐ(V)ΒΡΙΊœΒ’ΐ»ΖΒΡ «ΓΓ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ (ΓΓΓΓ )
|
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com