
3.某氯化镁溶液的密度为d g·cm─3,其中镁离子的质量分数为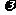 ,a mL该溶液中Cl─的物
,a mL该溶液中Cl─的物
质的量为: ( )
A.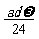 mol B.
mol B.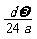 mol C.
mol C.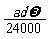 mol D.
mol D.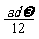 mol
mol
2.下列反应的离子方程式书写正确的是: ( )
A.硫酸镁溶液与氢氧化钡溶液反应:SO42─+Ba2+== BaSO4↓
 B.澄清石灰水与碳酸氢钙溶液反应:Ca2++HCO3─+OH─==
CaCO3↓+H2O
B.澄清石灰水与碳酸氢钙溶液反应:Ca2++HCO3─+OH─==
CaCO3↓+H2O
C.实验室用浓盐酸与MnO2反应制Cl2:MnO2+2H++2Cl─ Cl2↑+Mn2++H2O
D.氯气通入冷水中: Cl2+ H2O == ClO─+Cl─+2H+
1.下列说法正确的是: ( )
①正常雨水的pH为7.0,酸雨的pH小于7.0
②严格执行机动车尾气排放标准有利于防止大气污染
③使用二氧化硫和某些含硫化合物进行增白的食品对人体健康产生损害
④使用氯气对自来水消毒过程中,生成的有机氯化物可能对人体有害
⑤食品厂产生的含丰富氮、磷营养素的废水可长期排向水库养鱼
A.①②③ B.①④⑤ C.②③④ D.③④⑤
24.(6分)将一定量氧化铜粉末加入到100mL0.5mol/L的硫酸中,微热至氧化铜全部溶解,再向该蓝色溶液中加入铁粉10克充分反应后过滤,烘干,得干燥的固体物质仍为10克。
(1)参加反应的铁为多少克?
(2)原加入的氧化铜为多少克?
(3)最后得到的溶液仍为100mL,其物质的量浓度为多少?
23.(5分)(1)可以验证镁、铝的金属性强弱的实验是 。
(a)将在空气中放置已久的这两种元素的块状单质分别放入热水中
(b)将这两种元素的单质粉末分别和同浓度的盐酸反应
(c)将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
(d)比较这两种元素的气态氢化物的稳定性
(2)现有MgCl2溶液、AlCl3溶液、NaOH溶液、氨水、盐酸等几种物质,试设计实验方案证明镁、铝的金属性强弱。
22.(9分)短周期元素形成的纯净物A、B、C、D、E是转化关系如下图所示,物质A与物质B之间的反应不在溶液中进行(E可能与A、B两种物质中的某种相同)。
|


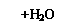
|



|
|


|


请回答下列问题:
(1)若C是离子化合物,D是一种强碱,写出C的一种化学式 。
(2)若E的水溶液呈现弱酸性,D是既能溶于强酸、又有溶于强碱的化合物。
①用电离方程式解释D既能溶于强酸,又能溶于强碱的原因。
。
②用等式表示E与NaOH溶液反应后生成正盐的溶液中所有离子浓度之间的关系
。
(3)若C是一种气体,D是一种强酸,则:
①C与水反应的化学方程式为 。
②有人认为“浓H2SO4可以干燥气体C”。某同学为了验证该观点是否正确,用下图装置进行实验。实验过程中,浓H2SO4中未发现有气体逸出,且变为红棕色,则你得出的结论是 。

③已知常温下物质A与物质B生成1mol气体C的焓变为-57.07kJ, 1 mol气体C与H2O反应生成D溶液和E气体的焓变为-46kJ,写出物质A与物质B及水生成D溶液的热化学方程式 。
21.(4分)某化学反应的反应物和产物如下:
KMnO4 + KI+ H2SO4→ MnSO4 + I2 + KIO3 + K2SO4 + H2O
(1)该反应的氧化剂是 (2)如果该反应方程式中I2和KIO3的系数都是5
①KMnO4的系数是 ②在上面的化学反应式上标出电子转移的方向和数目。
(3)如果没有对该方程式中的某些系数作限定,可能的配平系数有许多组。原因是
。
20.(5分)下列中学化学中常见物质的转化关系图中,反应条件及部分反应物和产物未全部注明,已知A、D为金属单质,其他为化合物。试推断:
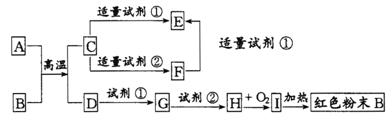
(1)写出物质的化学式:
A:_______ C:________ I:________
(2)写出下列反应的方程式:
C→F的离子方程式
H→I的化学方程式
19.(7分)X、Y、Z、W四种化合物均由短周期元素组成,其中X含有四种元素,X、Y、Z的焰色反应均为黄色,W为无色无味气体。这四种化合物具有下列转化关系(部分反应物、产物及反应条件已略去)。请回答:
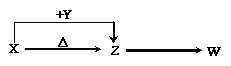
(1)W的电子式是 。(2)X与Y在溶液中反应的离子方程式是
(3)X含有的四种元素之间(二种、三种或四种)可组成多种化合物,选用其中某些化合物,利用右图装置(夹持固定装置已略去)进行实验,装置III中产生白色沉淀,装置V中可收集到一种无色气体。

①装置Ⅰ中反应的化学方程式是 。
装置Ⅱ中物质的化学式是 。
②用Ⅹ含有的四种元素中的两种组成的某化合物,在催化剂存在下制备并收集纯净干燥的装置Ⅴ中气体,该化合物的化学式是 ,所需仪器装置是 (从上图选择必要的装置,填写编号)。
18.(9分)某化学小组欲探究铁及其化合物的氧化性和还原性,请回答下列问题:
(1)除胶头滴管外,你认为本实验必不可缺少的一种玻璃仪器是 。
(2)请帮他们完成以下实验报告:
实验目的:探究铁及其化合物的氧化性和还原性。
试剂:铁粉、FeCl3溶液、FeCl2溶液、氯水、锌片、铜片。
实验记录(划斜线部分不必填写):
|
序号 |
实验内容 |
实验现象 |
离子方程式 |
实验结论 |
|
① |
在FeCl2溶液中滴入适量氯水 |
溶液由浅绿色变为棕黄色 |
|
Fe2+具有还原性 |
|
② |
在FeCl2溶液中加入锌片 |
|
Zn+Fe2+=Zn2++Fe |
|
|
③ |
在FeCl3溶液中加入足量铁粉 |
|
Fe+2Fe3+=3
Fe2+ |
Fe3+具有氧化性 |
|
④ |
|
|
|
Fe3+具有氧化性 |
实验结论:Fe只有还原性,Fe3+只有氧化性,Fe2+既有氧化性,又有还原性。
(3)根据以上结论判断,下列物质中既有氧化性,又有还原性的有: 。(填序号)
A.Cl2 B.Na C.Na+ D.Cl- E.SO2 F.NO2
(4)亚铁盐在溶液中易被氧化,而实验室中需要纯净的亚铁盐溶液。那么保存亚铁盐溶液时应该 防止亚铁盐被氧化。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com