
2.火星探测器发回的信息表明,火星上存在针铁矿[化学式FeO(OH)]和黄钾铁矾[化学式KFe3(SO4)2(OH)n],从而证明火星表面曾经存在过水。这一发现被《人民日报》评为2006世界大十新闻之首。已知两种矿物中铁的价态想同,则黄钾铁矾中n值为 ( )
A.4 B.5 C.6 D.7
1.2007年3月温家宝总理在十届全国人大五次会议上提出“要大力抓好节能降耗、保护环境”,下列举措与这一主题不吻合的是 ( )
A.用“绿色化学”工艺,使原料完全转化为产物
B.推广燃煤脱硫技术,防治SO2污染
C.推广垃圾的分类存放、回放、处理
D.大量使用农药化肥,提高粮食产量
29.某同学利用废铁屑(含少量铜等不与盐酸反应的杂质)来制备FeCl3·6H2O,并测定该废屑中铁的纯度,设计了下列实验装置图。A中放有m克废铁屑,烧杯中盛有过量的过氧化氢溶液。
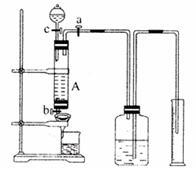
完成下列问题:
(1)如何检查装置A的气密性: 。
(2)实验时打开a,关闭b,从分液漏斗内向A中加过量的稀盐酸,观察到的现象是 ;滴加盐酸时,发现反应速率较相同浓度盐酸与铁粉反应要快,其原因是 。
(3)待A中的物质反应完成后,打开b,进行过滤,滤液过滤到盛有过氧化氢的烧杯中,发生反应的化学方程式为: 。
(4)要从烧杯内溶液得到FeCl3·6H2O晶体,主要操作包括:
(5)实验室若没有过氧化氢,可用下列 试剂代替(填选项)。
A.过量稀硝酸 B.过量氯水 C.过量氨水 D.过量氢氧化钠溶液
(6)若要测废铁屑中铁的纯度,测出放出气体的体积V(实验中导管体积忽略不计,已折算成标准状况,单位:L),则废铁屑纯度为 (用m、V的代数式表示)
28.已知两个羟基同时连在同一碳原子上的结构是不稳定的,它要发生脱水反应:
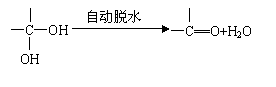

现有分子式C9H8O2X2(X为一未知元素)的物质M,可在一定条件下发生上述一系列反应:
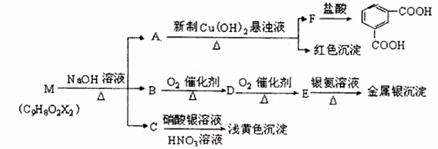
试回答下列问题:
(1)X为 (填元素符号);
(2)A中所含的官能团为 (填名称),上述转化中其中属于氧化反应的共有 步(填数字);M与NaOH溶液共热时的反应类型是 反应。
(3)M的结构简式为 。
(4)写出下列反应的化学方程:
①B→D ;
②E和银氨溶液反应的化学方程式: 。
27.(14分)X、Y、Z三种短周期元素,它们的原子序数之和为16。X、Y、Z三种元素的常见单质在常温下都是无色气体,在适当条件下可发生如下变化:一个B分子中含有的Z原子个数比C分子中少1个,B、C两种分子中的电子数均等于10。请回答下列问题:
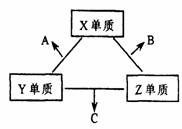
(1)X元素的周期表中的位置是 周期 族。
(2)分析同主族元素性质的递变规律,发现B、C物质沸点反常,这是因为它们的分子之间存在 。
(3)①C的电子式是 ,C分子的结构呈 形。
②C在一定条件下反应生成A的化学方程式是 。
③X、Y、Z三种元素可组成一种强酸W,C在适当条件下被W吸收生成一种盐。该盐的水溶液pH 7(填“大于”、“小于”、“等于”),其原因是(写出离子方程式) 。
26.(16分)物质X是中学化学中的常见由短周期元素组成的物质,X既能与稀硫酸反应,又能与氢氧化钠溶液反应。
(1)若X为氧化物,X的化学式是 。
(2)若X为单质,X用于焊接钢轨反应的化学方程式是 。
(3)若X与稀硫酸反应生成无色没有气味的气体A,与浓氢氧化钠溶液加热反应生成气体B。等物质的量的A和B在水溶液中反应又生成X。
X与稀硫酸反应的离子方程式是 ;
X与足量稀氢氧化钠溶液反应的离子方程式是 。
在宇航器中,可以不断的将座舱内的空气通过盛有金属过氧化物(以过氧化钠为例)的容器,以除去A,反应的化学方程式是 。
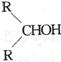
36.(15分)如图20-4所示:淀粉水解可产生某有机化合物A,A在不同的氧化剂作用下,可以生成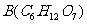 或
或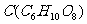 ,B和C都不能发生银镜反应。A、B、C都可以被强还原剂还原成为
,B和C都不能发生银镜反应。A、B、C都可以被强还原剂还原成为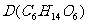 。B脱水可得到五元环的酯类化合物E或六元环的酯类化合物F。
。B脱水可得到五元环的酯类化合物E或六元环的酯类化合物F。
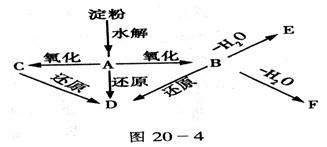
已知,相关物质被氧化的难易次序是:RCHO最易,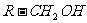 次之,
次之,
最难。
(1)请在下列空格中填写A、B、C、D、E、F的结构简式。
A:_______________; B:_______________; C:_______________;
D:_______________; E:_______________; F:_______________。
(2)请写出AgD的反应方程式:
35.(15分)在一定温度下,将2mol
A和2molB 两种气体混合于容积为2L的某密闭容器中,发生如下反应:3A(g)+B(g) xC(g)+2D(g) △H<0 ,2分钟末反应达到平衡状态,生成了0.8mol D,并测得C的浓度为0.4mol/L,请填写下列空白:
xC(g)+2D(g) △H<0 ,2分钟末反应达到平衡状态,生成了0.8mol D,并测得C的浓度为0.4mol/L,请填写下列空白:
(1)x值等于 ;
(2)A的转化率为 ;
(3)D的化学反应速率为 ;
(4)如果增大反应体系的压强,则平衡体系中C的质量分数 (填增大、减小或不变);如果改变外界条件使此反应的化学平衡常数增大,则此外界条件是
(5)如果上述反应在相同条件下从逆反应开始进行,开始加入C和D各4/3mol,要使平衡时各物质的体积分数与原平衡时完全相等,则还应加入 mol 物质。
34.(15分)X、Y、Z为短周期元素的单质,U、V为它们的化合物,这些物质之间的关系如图5-3所示,其中反应条件和某些产物已经略去:
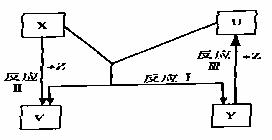
(1)如果X 、Y的组成元素是同主族的,写出反应Ⅰ的化学反应方程式:
、Y的组成元素是同主族的,写出反应Ⅰ的化学反应方程式:
①若已知V是水:______________________________________________;
②若已知U、V均为氧化物:________________________________。
(2)如果X、Y的组成元素不同主族时,按下列要求回答问题。
①X元素是地壳中含量最多的金属元素时,则X、Y、Z的化学式是:X为_________;Y为_____________;Z为___________。
②若Y元素在自然界中形成的化合物种类最多,则V、U的化学式是:V为______;U为_____________。
③若Z是氧化性最强的非金属,则反应Ⅰ的化学反应方程式:__________________
_____________________________________,则V为______________。
33. (15分)恒温下,将a mol N2与b
mol H2的混合气体通入一个固定容积的密闭容器中,发生如下反应:N2
(g) + 3 H2(g) 2NH3(g) △H<0
(15分)恒温下,将a mol N2与b
mol H2的混合气体通入一个固定容积的密闭容器中,发生如下反应:N2
(g) + 3 H2(g) 2NH3(g) △H<0
(1)若反应进行到某时刻t时,nt (N2) = 13mol,nt (NH3) = 6mol,则a =
(2)反应达平衡时,混合气体的体积为672L(标况下),其中NH3的含量(体积分数)为25%。则平衡时NH3的物质的量 = 。
(3)写出该反应的化学平衡常数表达式K=___________________。
(4)反应达平衡后,若降低温度,则该反应K值____________,N2的转化率__________(以上均填增大、减小或不变)。
(5)反应达平衡后,若向此容器中冲入He气,化学反应速率__________,(填增大、减小或不变),化学平衡将 移动(填“正向”,“逆向”或“不 ”)
选做题:(以下三题34、35、36小题自选一题作答,多做不给分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com