
22.在10ml0.1mo/L的纯碱溶液中,不断搅拌并逐滴加入1.2ml 1.0 mol/L盐酸,完全反应后标准状况下生成二氧化碳的体积为 ( )
A.2.24ml B.4.48ml
C.0ml D.13.44ml
|
21.X、Y、Z、W为四种短周期主族元素。其中X、Z同族,Y、Z同周期,W与X、Y既不同族也不同周期;X原子最外层电子数是核外电子层数的3倍;Y的最高正价与最低负价的代数和为6。下列说法正确的是 ( )
A.X元素形成的单质均为双原子分子
B.Y元素最高价氧化物对应水化物酸性比磷酸弱
C.原子序数由小到大的顺序为W<X<Y<Z
D.X与W形成的化合物沸点高于Z与W形成的化合物沸点
20.已知硫酸锰(MnSO4)和过硫酸钾(K2S2O8)两种盐溶液在银离子催化下可发生氧化还原反应,生成高锰酸钾、硫酸钾和硫酸。下列说法正确的是 ( )
A.反应中被氧化的元素是硫
B.2mol MnSO4,消耗8molH2O
C.1mol过硫酸钾(K2S2O8)参加反应时,转移1mole-
D.若该反应所用的硫酸锰改为氯化锰,当它跟过量的过硫酸钾反应时,锰元素被氧化
19.下列实验操作或实验方案中正确的是 ( )
①粗盐提纯时,为了加快过滤速率,可用玻璃棒搅拌过滤器中的液体
②利用固、液反应物混合的方法制取H2或O2,可采用相同的发生装置
③利用饱和食盐水,可除去氯气中混有的氯化氢气体
④向稀硫酸中加入废铁屑,然后加热蒸干即可得硫酸亚铁晶体
⑤测定硫酸铜晶体中结晶水含量时至少需要称量4次
⑥某无色溶液中加入Ba(NO3)2溶液,生成白色沉淀,加稀盐酸沉淀不消失,可确定有SO2-4存在
A.①②③ B.①③⑤
C.②④⑥ D.②③⑤
18.在淀粉碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝,在上述溶液中加入足量的亚硫酸钠溶液,蓝色逐渐消失。下列判断不正确的是 ( )
A.氧化性:ClO->I2>SO2-4
B.漂白粉溶液可使淀粉碘化钾试纸变蓝
C.向氯水中加入亚硫酸钠溶液,氯水褪色
D.次氯酸钠可以与亚硫酸钠共存
17.某结晶水合物的化学式为A·Xh2O,其相对分子质量为B。在60℃时,mg该晶体溶于ng水中,制得VmL密度为dg·mL-1的饱和溶液。下列表示式或判断正确的是( )
A.该溶液的物质的是浓度为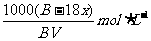
B.该温度下A的溶解度为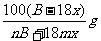
C.将10gA投入到饱和溶液中,析出的晶体大于10g,且溶液质量减少,但浓度不变
D.该溶液的质量分数为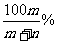
16.有一种蓝色晶体[可表示为:Mx[Fey(CN)6]],经X射线研究发现,其离子的结构特征是Fe3+和Fe2+互相占据立方体互不相邻的顶点,而CN-位于立方体的棱上。晶体中阴离子的最小结构单元如下图所示。下列说法正确的是 ( )
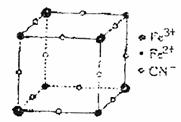
A.该晶体属于离子晶体,M呈+2价
B.该晶体属于离子晶体,M呈+1价
C.该晶体的化学式为M[Fe3(CN)6]
D.晶体中与每个Fe3+距离最近且等距离的CN-为3个
15.某强氧化剂[XO(OH)2]+被亚硫酸钠还原到较低价态,若还原2.4×10-3mol[XO(OH)2]+到较低态,需用20ml0.2mol/L Na2SO3溶液,则X元素的最终价态为 ( )
A.+1 B.+2 C.0 D.-1
14.下列说法正确的是 ( )
A.SO2气体通入到溴水中不是因为氧化还原反应而褪色
B.FeCl3、AlCl3、Na2CO3、H2SO4四种溶液不用任何试剂就可鉴别
C.12C、14C、C60都属于碳的同位素
D.PCl3、CCl4、N2分子中各原子都达到8电子结构
13.在CO2中混有少量的O2、H2S、HCl和水蒸气,现用四种试剂,即①浓硫酸;②CuSO4溶液;③饱和的碳酸氢钠溶液;④红热铜丝,除去上述杂质,得到纯净的CO2气体,此混合气体通过四种试剂的最合理的顺序是 ( )
A.②①③④ B.③②①④ C.③④①② D.④①②③
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com