
24.(14分)沼气、油田气和煤矿坑道气主要成分的分子结构特征为
,它与氯气反应的反应类型属于 反应。
某石油分馏产品中含分子式为C18Hm烷烃,m值等于 ,若该石油分馏产品是一种燃料,则应属于 (选填“汽油”、“煤油”“柴油”);对石油进行催化裂化目的是 ;对裂化产物通过进一步裂解,可以得到许多重要的化工原料。辛烷裂解的化学方程式为:
;
裂解气的成分之一CH3CH=CH2在一定条件下合成高分子化合物聚丙烯的化学方程式:
。
23.(16分)(1)海水淡化的方法中,主要方法 法历史最久,技术和工艺也比较完善,但成本较高。金属的冶炼有直接加热分解法、电解法和使用还原剂法。用HgO冶炼Hg的化学方程式为: ,铝热反应的化学方程式为:
。
(2)苯可以从 的干馏中得到,苯的特殊结构决定苯的特殊性质,例如苯 使酸性高锰酸钾溶液褪色(填“不能”“能”);把约1mL苯滴入1mL溴水中充分振荡后静置,出现的现象是: ;苯既能发生加成反应又能发生取代反应,由苯生成硝基苯的化学方程式为: ;
苯与H2发生加成反应的化学方程式为: 。
22.(20分)有机物A、B、C、D、E之间发生如下的转化
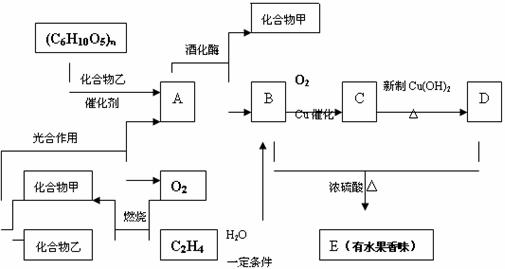
已知A含6个C原子,B、C、D都含2个C原子。A在酒化酶作用下发生的反应中,分子个数关系为:A -→ 2B + 2甲
(1)请写出下列转化的反应方程式
① (C6H10O5)n →A: 。
② A→B: ;
③ C→D: 。
(2)乙二醇( HO-CH2-CH2-OH )与上图中有机物D在浓硫酸和加热条件下反应的化学方程式为: ,反应类型为:
反应。
(3)实验室用下图所示的装置制取E,请回答下列问题:
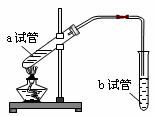
① a试管中浓硫酸的作用是:______________ ;
② b试管中饱和Na2CO3溶液的主要作用:
。
③ b试管里出现的现象为: 。
21.(12分)有V、W、X、Y、Z五种元素,它们的核电荷数依次增大,且都小于20;X、Z是金属元素;V和Z元素原子的最外层电子都只有一个;W和Y元素原子的最外层电子数相同,且W元素原子L层电子数是K层电子数的3倍;X元素原子的最外层电子数是Y元素原子最外层电子数的一半。由此可知:
(1)X在元素周期表中的位置是 。
(2)Y元素最高价氧化物对应水化物的分子式为 ,形成Z元素最高价氧化物对应水化物的化学键类型是 。
(3)V与W形成的常见化合物分子的电子式为 。
(4)Y与Z的化合物属于 (填“离子化合物”或“共价化合物”),该化合物的形成过程电子式为 。
20.已知离子方程式:5X-+XO3-+6H+=3X2+3H2O,若X为主族元素,据此判断:X元素的最高化合价为
A.+1 B.+4 C.+5 D.+7
19.通过实验来验证淀粉水解可以生成葡萄糖,其实验包括下列操作,这些操作的正确顺序是① 加入少量淀粉和水制成溶液 ② 加热煮沸 ③ 加入碱液中和酸 ④加入银氨溶液 ⑤ 加入少量稀硫酸 ⑥ 再加热
A.①②⑤⑥④③ B.①⑤②④⑥③
C.①⑤②③④⑥ D.①⑥④⑤③②
18.下列叙述中,错误的是
A.在平衡体系
PCl5(g)  PCl3(g)
+ Cl2(g) 中加入一定量的37Cl2,一段时间后37Cl存在于五氯化磷、三氯化磷和氯气这三种物质中
PCl3(g)
+ Cl2(g) 中加入一定量的37Cl2,一段时间后37Cl存在于五氯化磷、三氯化磷和氯气这三种物质中
B.CH3COOH与H18O-CH2CH3发生酯化反应是可逆反应,达到平衡后18O仅存在于乙醇和乙酸乙酯分子里,不可能存在于乙酸和水分子里
C.CH2Cl2没有同分异构体的事实证明了甲烷分子是以碳原子为中心的正四面体结构
D.在氧气中完全燃烧后生成物只有CO2和H2O的有机物一定是烃
17.下列物质,能使溴水因发生反应而褪色的是
A.CH3(CH2)16CH3 B.CH2==CH-COOH
C.苯 D.直馏汽油
16.在一定温度下,向容积为1 L的密闭容器中加入1 mol A气体和2 mol B气体,
发生反应:A(g) + 2B(g)  2C(g) 下列说法,属于该反应达到平衡标志的是
2C(g) 下列说法,属于该反应达到平衡标志的是
A.容器内A、B、C的浓度之比为1:2:2
B.单位时间消耗0.1 mol / L A同时生成0.2 mol / L C
C.容器内压强不随时间变化
D.容器内气体的平均相对分子质量不随时间变化
15.下列说法正确的是
A.需要加热的化学反应一定是吸热反应
B.绿色化学提倡化工生产提高原子利用率,避免反应中生成有污染的物质
C.H2-→H+H 的变化放出能量
D.鼓入大量空气(远远过量)使燃料完全燃烧,一定提高燃料的利用率
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com