
1.下列方法可用于制备卤化氢气体的是( )
A.NaCl与浓硝酸加热制备HCl B.NaF与浓硫酸加热制备HF
C.NaBr与浓磷酸加热制备HBr D.NaI与浓硫酸加热制备HI
7.过氧化氢的性质:过氧化氢中氧元素的化合价是 价,因此过氧化氢表现为即有 性又有 性,并以 性为主,过氧化氢的水溶液俗称 呈弱酸性。
a.化学性质:
(1) 当遇到强还原剂时,体现氧化性,如:
SO2 + H2O2 = ; Fe2+ + H2O2 + H+ =
(2) 当遇到强氧化剂时,体现还原性,如:MnO4- + H2O2 + H+ =
(3)不稳定性:H2O2 =
b.用途:
[例题解析]
[例1](2002年广东)已知硫酸锰(MnSO4)和过硫酸钾(K2S2O8)两种盐溶液在银离子催化下可发生氧化还原反应,生成高锰酸钾、硫酸钾和硫酸。
(1)请写出并配平上述反应的化学方程式:_________________________________;
(2)此反应的还原剂是_________,它的氧化产物是____ __。
(3)此反应的离子反应方程式可表示为: 。
若该反应所用的硫酸锰改为氯化锰,当它跟过量的过硫酸钾反应时,除有高锰酸钾、硫酸钾、硫酸生成外,其他的生成物还有 ___________
解题思路: 。
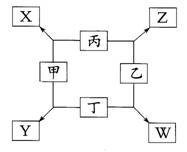 [例2]如图所示,已知:①甲、乙、丙、丁均为前三周期元素的单质。
②在一定条件下甲与丙和甲与丁都按物质的量之比1∶3反应,分别生成X和Y,在产物中元素甲呈负价。
③在一定条件下乙与丙和乙与丁都按物质的量之比1∶2反应,分别生成Z和W,在产物中元素乙呈负价。
请填空:
[例2]如图所示,已知:①甲、乙、丙、丁均为前三周期元素的单质。
②在一定条件下甲与丙和甲与丁都按物质的量之比1∶3反应,分别生成X和Y,在产物中元素甲呈负价。
③在一定条件下乙与丙和乙与丁都按物质的量之比1∶2反应,分别生成Z和W,在产物中元素乙呈负价。
请填空:
(1)甲是_______________ 乙是 。
(2)甲与丙反应生成X的化学方程式是 ______________________________。
(3)和丁反应生成W的化学方程式________________________________
解题思路: 。
[巩固练习]
5. 硫的四种价态间的含硫物质之间的网络关系
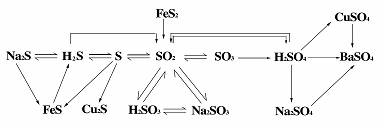
①H2S是具有 气味的 气体,其水溶液氢硫酸是一种具有挥发性的二元 酸,硫化氢、氢硫酸都具有强还原性可被碘水、溴水、氯水、FeCl3溶液、HNO3等氧化。H2S能燃烧,燃烧依反应条件不同而不同。
②硫与Fe、Cu反应时,由于其非金属性比氯 ,所以生成低价态的物质 。
③硫的氧化物有SO2和SO3,其中SO2是一种有 气味的气体,易液化, 溶于水-其水溶液叫 、二元弱酸。SO2是重要的大气污染物(其危害详见课本),防治方法有排烟除硫燃料脱硫等。
2.硫的氢化物、氧化物及其水化物的结构、性质
|
类别 |
氢化物 |
氧化物 |
氧化物水化物 |
|||
|
结 构 |
分子式 |
H2S |
SO2 |
SO3 |
H2SO3 |
H2SO4 |
|
化学键 |
|
|
|
|
|
|
|
晶体类型 |
|
|
|
|
|
|
|
物 理性质 |
色、味、态 |
|
|
|
|
|
|
毒性 |
|
|
|
|
|
|
|
化 学 性质 |
溶解性 |
|
|
|
|
|
|
与金属反应 |
|
不反应 |
不反应 |
|
|
|
|
稳定性 |
不稳定 |
稳定 |
较稳定 |
不稳定 |
稳定 |
|
|
水溶液的酸性强弱 |
弱酸性 |
|
|
|
|
|
|
检 验 |
使含Pb2+的湿润试纸变黑或与Cu2+反应生成CuS沉淀 |
|
|
|
|
4.硫单质与氢化物、氧化物的性质及化合价关系
强还原性 氧化性、还原性 强氧化性
 特别注意:中间价态的两类硫既有氧化性,又有还原性,SO2、H2SO3、Na2SO3以还原性为主。
特别注意:中间价态的两类硫既有氧化性,又有还原性,SO2、H2SO3、Na2SO3以还原性为主。
3.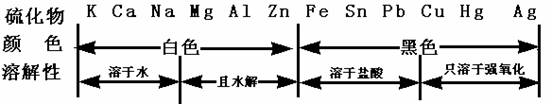 金属硫化物的颜色和溶解性
金属硫化物的颜色和溶解性
1.氧族元素的原子结构及性质递变规律
|
元素名称和符号 |
氧(O) |
硫(S) |
硒(Se) |
碲(Te) |
|||
|
原子结构 |
原子序数 |
|
|
|
|
||
|
结构示意图 |
|
|
|
|
|||
|
电子式 |
|
|
|
|
|||
|
主要化合价 |
|
|
|
|
|||
|
相同点 |
|
||||||
|
不同点 |
|
||||||
|
原子半径 |
|
||||||
|
物 理 |
颜色和状态 |
|
|
|
|
||
|
密度 |
|
||||||
|
性 质 |
熔、沸点 |
|
|||||
|
水、有机溶剂溶解度 |
|
||||||
|
化学反应 |
与金属反应 |
|
|
|
|
||
|
与非金属反应 |
|
|
|
|
|||
|
与化合物反应 |
|
|
|
|
|||
[小结]非金属性依次 ;金属性依次 。
3. 了解硫的氧化物对环境的污染及环境保护的意义

教与学方案 笔记与反思
[自学反馈]
2. 以硫元素为代表,了解氧族元素的单质、氢化物及其氧化物的重要性质;
2.用图3-5所示的实验过程,测定含Na2SO3的亚硫酸钠中Na2SO3的质量分数(Na:23克/摩;Ba:137克/摩;S:32克/摩).
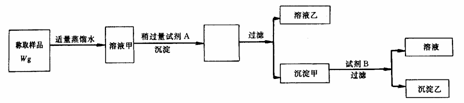
图3-5
测定沉淀乙(纯净干燥)的质量W1g,试回答:
(1)试剂A溶液是 ,检验A稍过量的方法是 ;
(2)试剂B溶液是 ,B的作用是 ;
(3)沉淀甲的化学式是 ,沉淀 乙的化学式是 ;
(4)沉淀甲与B反应的离子方程式是 ;
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com