
66.(9分)(1)I 染色体变异 基因重组
(2)DT ddTT
(3)花药离体培养 秋水仙素 抑制纺锤丝形成
(4)DDtt:Ddtt:ddtt=1:2:1
65.(6分)(1)5
(2) 虎鲸
(3)须鲸、虎鲸(缺一不得分)
(4)竞争 捕食 竞争
64.(6分)(1)③ (2)捕食 捕食者 被捕食者 (3)② b
63.(7分)(1)1/4 BB或Bb 2/3
(2) XBXB或XBXb XBXb 外祖母 XBXb
62.(5分)(1) 雄 (2)伴性遗传 (3) 4 2 (4)一
① Dt ② dt D_T_ D_tt ddT_ ddtt
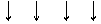 (三)
(六)
(三)
(六)
|
 (四)
(四)
DDTT ③ ④ ⑤ ddTT
Ⅰ Ⅱ
(1)要缩短育种年限,应选择的方法是 ,依据的变异原理是 ;另一种方法的育种原理是 。
(2)图中①和④基因组成分别为 、 。
(3)(三)过程采用的方法称为 ;(四)过程常用的化学药剂是 ,其作用原理是 。
(4)如将方法Ⅰ中获得的③⑤植株杂交,再让所得到的后代自交,则后代的基因型及其比例为 。

石家庄市第一中学
2009-2010 学年度第二学期高二年级期中考试生物试题答案及评分标准(文科)
卷I:单项选择题,每小题1分,共60分
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
14 |
15 |
|
A |
B |
D |
D |
B |
D |
C |
A |
D |
C |
B |
C |
A |
C |
D |
|
16 |
17 |
18 |
19 |
20 |
21 |
22 |
23 |
24 |
25 |
26 |
27 |
28 |
29 |
30 |
|
B |
C |
D |
D |
A |
D |
B |
C |
B |
D |
D |
C |
C |
B |
B |
|
31 |
32 |
33 |
34 |
35 |
36 |
37 |
38 |
39 |
40 |
41 |
42 |
43 |
44 |
45 |
|
A |
A |
D |
C |
B |
A |
C |
C |
D |
C |
D |
C |
C |
C |
D |
|
46 |
47 |
48 |
49 |
50 |
51 |
52 |
53 |
54 |
55 |
56 |
57 |
58 |
59 |
60 |
|
A |
B |
D |
C |
B |
D |
B |
D |
D |
C |
D |
B |
C |
A |
B |
卷Ⅱ:非选择题,每空1分,共40分
61.(7分)(1)(胸腺嘧啶)脱氧核苷酸
(2)胞嘧啶
(3)氢键 碱基对 特异
(4)双螺旋(结构)
(5)基因突变
 F1: DdTt
F1: DdTt
37.(4分) 晶体是质点(分子、离子或原子等)在空间有规则地排列、具有整齐外形、以多面体出现的固体物质。在空间里无限地周期性的重复能形成晶体的、具有代表性的最小单元,称为晶胞。一种Al-Fe合金的立体晶胞如下图所示。
|

请据此回答下列问题:
(1) 确定该合金的化学式____________。
(2) 若晶体的密度为ρ g/cm3,NA为阿伏加德罗常数,则此合金中最近的两个Fe原子之间的距离(用含ρ的代数式表示,不必化简)为___________________cm。
衡水中学2009-2010学年度第二学期期中考试
36、(4分)已知1molCO气体完全燃烧生成CO2气体放出283kJ的热量,1molH2气体完全燃烧生成液态水放出286kJ的热量,1molCH4气体完全燃烧生成CO2气体和液态水放出890kJ的热量
(1)写出H2完全燃烧的热化学方程式 。(2)若1molCH4气体完全燃烧生成CO2气体和水蒸气放出的热量 890kJ
(填>、<或=)
(3)若将amolCH4、CO和H2的混合气体完全燃烧,生成CO2气体和液态水,放出热量(Q)的取值范围是 。
(4)若将amolCH4、CO和H2的混合气体完全燃烧,生成CO2气体和液态水,且CO2和水的物质的量相等时,放出热量(Q)的取值范围是 。
35.(9分)某实验小组设计用50 mL1.0mol/L盐酸跟50mL1.1mol/L氢氧化钠溶液进行中和反应,测定中和热,中和热测定实验的关键是要比较准确地配制一定物质的量浓度的溶液,量热器要尽量做到绝热;在量热的过程中要尽量避免热量的散失,比较准确地测量出反应前后溶液温度的变化。回答下列问题:
(1)中和热的测定所需的玻璃仪器有
(2)本实验中用稍过量的NaOH的原因是 。
(3)在反应中若因为有放热现象,而造成少量HCl挥发,则测得的中和热数值 (填偏高、偏低或不变);
(4)该实验小组做了三次实验,每次取溶液各50mL,并记录如下原始数据。
|
实验序号 |
起始温度t1/℃ |
终止温度(t2)℃ |
温差(t2-t1)℃ |
||
|
盐酸 |
NaOH溶液 |
平均值 |
|||
|
1 |
25.1 |
24.9 |
25.0 |
31.6 |
6.6 |
|
2 |
25.1 |
25.1 |
25.1 |
31.8 |
6.7 |
|
3 |
25.1 |
25.1 |
25.1 |
31.9 |
6.8 |
已知盐酸、NaOH溶液密度近似为1.00g/cm3,中和后混和液的比热容 C=4.18J/(g·℃)则该反应的中和热为△H=_______________________________;
(5)若用等浓度的醋酸代替盐酸与NaOH溶液反应,则测得的中和热的数值会 (填偏高、偏低或不变),其原因 ;
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com