
13.若NA表示阿伏加德罗常数,下列说法错误的是 ( )
A.常温常压下,臭氧与氧气的混合气体4.8g中所含有的原子总数为0.3NA
B.含5.4 gAl3+的硫酸铝溶液中,含有的SO42-的数目是0.3NA
C.在标准状况下,4.48L C4H10含有极性键为2NA,含有非极性键为0.6NA
D.由化合态的氧元素得到0.1molO2需要转移电子0.4 NA 
12.下列说法中正确的是
( )
A.刚落下的酸雨随时间酸性逐渐增强,是由于雨水所含成分被不断氧化的原因
B.卤素元素从上到下,由于非金属性逐渐减弱,故氢卤酸的酸性依次减弱
C.因为氧化性:HClO>稀H2SO4,所以非金属性:Cl>S
D.钠原子在反应中失去的电子比铝原子少,故钠的金属性在理论上应弱于铝的金属性
11.已知磷酸分子 中,三个氢原子都可以跟重水分子(D2O)中的D原子发生氢交换。又知次磷酸(H3PO2)也可跟D2O进行氢交换,但次磷酸钠(NaH2PO2)却不能再跟D2O发生氢交换。由此可知次磷酸的分子结构为
( )
中,三个氢原子都可以跟重水分子(D2O)中的D原子发生氢交换。又知次磷酸(H3PO2)也可跟D2O进行氢交换,但次磷酸钠(NaH2PO2)却不能再跟D2O发生氢交换。由此可知次磷酸的分子结构为
( )
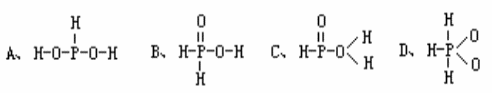

10.对三硫化四磷分子的结构研究表明,该分子中没有不饱和键,且各原子的最外层均已达到了8个电子的结构。则一个三硫化四磷分子中含有的共价键个数是 ( )
A.7 个 B.9 个 C.19 个 D.不能确定 
9.在一定体积的密闭容器中放入3升气体R和5升气体Q,在一定条件下发生反应:
2R(气)+5Q(气)= 3X(气)+nY(气)反应完全后,容器温度不变,混和气体的压强是原来的97.5%,则化学方程式中的n值是
( )
A.3 B.4 C.5 D.6
8.在一定温度下,已知有关某溶液的一些数据:①溶液的质量,②溶剂的质量,③溶液的体积,④溶质的摩尔质量,⑤溶质(气体)的体积(Vm已知),⑥溶液的密度,⑦溶液的质量分数.利用下列各组数据计算该溶液的物质的量浓度,不能算出的一组是( ) 
A.③⑤
B.②④⑤⑥ C.①④⑥ D.①②③④ 
7.某溶液中大量存在的五种离子: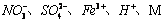 (M代表一种离子),其物质的量之比为:
(M代表一种离子),其物质的量之比为: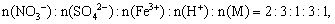 则M可能为( )
则M可能为( )
A.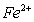 B.
B.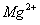 C.
C.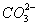 D.
D.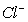

6.下列离子方程式正确的是
( )
A.向NaHSO4溶液中滴加过量Ba(OH)2溶液:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O
B.用碳酸钠溶液吸收少量二氧化硫:2CO32-+SO2+H2O=2HCO3-+SO32-
C.向FeCl3溶液中加入铜片:Fe3++Cu=Fe2++Cu2+
D.向碳酸氢钠溶液中加入氢氧化钠:HCO3-+ OH-==CO2↑+H2O
5.下列各组离子在给定条件下可能大量共存的是
( )
A.在酸性溶液中:NH4+、K+、S2O32-、Cl-
B.有SO42-存在的溶液中:H+、Mg2+、Ba2+、I--
C.在碱性溶液中:K+、SO32-、Br-、S2-
D.下列无色溶液中:Na+、S2-、AlO2-、CrO42-
4.关于反应:①2C2H2(g)
+ 5O2(g) = 4CO2 (g) + 2H2O(l) ΔH= -2600kJ/mol ;
②2CO(g)+O2(g)=2CO2(g);△H=-566kJ/mol ;
③CH4(g)+H2O(g)
=CO(g)+3H2(g) ΔH=+216 kJ/mol下列叙述正确的是 ( )
A.CO的燃烧热为-283 kJ/mol 
B.在③反应时,若加入催化剂,可以使ΔH减小
C.若有3.2g CH4与足量水蒸汽按③反应,则放出热量是43.2 kJ
D.若生成相同质量的CO2,则放出的热量C2H2大于CO
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com