
11.2008年诺贝尔化学奖表彰了发现和研究绿色荧光蛋白质(GFP)的科学家。据研究报道:GFP在厌氧条件下不能发射荧光,而增加氧分子会渐渐开始发光。生色团是GFP发出荧光的物质基础,如下图所式的结构形成了GFP生色团的核心。






下列有关GFP的说法正确的是
A.遇强还原剂Na2SO3 或FeSO4时,GFP会发射更强荧光

B.该生色团的肽链结构中含有甘氨酸单元
C.该生色团结构中没有手性碳原子 
D.温度超过70℃时,GFP因变性其荧光会消失 
10.下列离子方程式书写正确的是

A.过量的氯气通入FeCl2溶液中反应:Fe2+ + Cl2 = Fe3+ + 2Cl- 
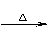 B.将数滴乙醛溶液滴加到呈碱性的新制氢氧化铜悬浊液里并加热产生砖红色沉淀:
B.将数滴乙醛溶液滴加到呈碱性的新制氢氧化铜悬浊液里并加热产生砖红色沉淀:
2Cu(OH)2
+ CH3CHO +OH― Cu2O↓ + CH3COO― + 3H2O 

 C.向偏铝酸钠溶液中通人少量二氧化碳:AlO2-+ CO2 + 2H2O
= Al(OH)3↓+HCO3-
C.向偏铝酸钠溶液中通人少量二氧化碳:AlO2-+ CO2 + 2H2O
= Al(OH)3↓+HCO3- 
D.碳酸钠溶液中加入少量的苯酚:CO32- + →
+ HCO3- 

9.氯乙酸C1CH2COOH的酸性强于CH3COOH,这是因为C1是一种强吸电子基团,能使-OH上的H原子具有更大的活动性,有的基团属于斥电子基团,能减弱-OH上的H原子的活动性,这些作用统称为“诱导效应”,请根据以上规律对下列说法作出判断,其中错误的说法是 
A.已知-C6H5属于吸电子基团,故C6H5COOH的酸性比CH3COOH强 
B.CH3COOH的酸性弱于HCOOH,是由于CH3COOH分子存在斥电子基团甲基的缘故 
C.HCOOH显酸性,而H2O显中性,是由于HCOOH分子中存在吸电子基团羧基的缘故 
D.下列酸中:CF3COOH、CC13COOH、CHC12COOH,酸性最强的是CF3COOH

8.下述实验不能达到预期实验目的的是
|
序号 |
实验内容 |
实验目的 |
|
A |
将2.5g CuSO4·5H2O溶解在97.5g 水中 |
配制质量分数为1.6%的CuSO4溶液 |
|
B |
向盛有1mL硝酸银溶液的试管中滴加NaCl溶液,至不再有沉淀生成,再向其中滴加Na2S溶液 |
说明一种沉淀能转化为另一种溶解度更小的沉淀 |
|
C |
室温下,用pH试纸测定浓度为0.1mol·L-1NaClO溶液和0.1mol·L-1CH3COONa溶液的pH |
比较HClO和CH3COOH的酸性强弱 |
|
D |
室温下,分别向2支试管中加入相同体积、相同浓度的Na2S2O3溶液,再分别加入相同体积不同浓度的稀硫酸 |
研究浓度对反应速率的影响 |
不定项选择题 本题包括6小题,每小题4分,共计24分。每小题有一个或二个选项符合题意。若正确答案只包括一个选项,多选时,该题得0分;若正确答案包括两个选项,只选一个且正确的得2分,选两个且都正确的得满分,但只要选错一个,该小题就得0分。
7.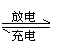 高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为

3Zn + 2K2FeO4 + 8H2O
3Zn(OH)2 + 2Fe(OH)3 + 4KOH 
下列叙述错误的是
A.放电时负极反应为:Zn ― 2e- + 2OH- = Zn(OH)2 
B.放电时每转移3 mol电子,正极有1mol K2FeO4被氧化 
C.充电时阳极反应为:Fe(OH)3
― 3e- + 5 OH- = FeO + 4H2O
+ 4H2O

D.充电时阴极附近溶液的碱性增强
6.下列各项内容中,排列顺序正确的是
① 固体的热稳定性:Na2CO3>CaCO3>NaHCO3
② 相同物质的量浓度的下列溶液中NH4+ 的浓度:(NH4)2SO4>(NH4)2CO3>NH4Cl

③ 微粒半径:K+>S2->F
④ 给出质子的能力:CH3COOH>C2H5OH>H2O
⑤ 氢化物的沸点:H2Se>H2S>H2O
A.①③ B.②④
C.①② D.③⑤ 
5.在指定环境中,下列各组离子一定可以大量共存的是 
A.使pH试纸呈红色的溶液:Fe2+、NO3-、SO42-、Na+

B.使无色酚酞试液显红色的溶液:S2-、K+、HCO3-、AlO2- 
C.在加入铝粉放出氢气的溶液:Na+、Cl-、NH4+、NO3- 
D.在c(H+)/c(OH-) = 1×1013的溶液:NH4+、Mg2+、C1-、K+ 
4.下列实验操作或对实验事实的叙述正确的是

A. 配制浓硫酸和浓硝酸的混合酸时,将浓硫酸沿器壁慢慢加入到浓硝酸中,并不断搅拌

B. 常温时,用pH试纸测得0.1 mol·L-1碳酸钠溶液的pH = 7 
C. 如果皮肤上不慎沾有苯酚,应立即用大量的NaOH稀溶液冲洗 
D. 向沸腾的NaOH稀溶液中滴加FeCl3饱和溶液,以制备Fe(OH)3胶体 
3.设NA为阿伏加德罗常数,下列叙述中错误的是
A. 在标准状况下,22.4L空气中约有NA个气体分子
B. 在含4molSi-O键的石英晶体中,氧原子的数目为2NA

C. 28g乙烯和28g丙烯中均含有6NA对共用电子对 
D. 含NA个氧原子的O2与含NA个氧原子的O3的质量之比为2︰3 
2.下列文字表述与反应方程式对应且正确的是

A. 氧化铁溶于氢碘酸:Fe2O3+6H+ = 2Fe3++3H2O 
B. 等物质的量的KHCO3和Ba(OH)2的溶液混合:HCO3-+ Ba2++OH-
= BaCO3↓ +
H2O 
C. NaHSO3溶液显酸性的原因是:HSO3- = SO32- + H+ 
D. 硫化钠水溶液呈碱性的原因是:S2- + 2H2O  H2S + 2OH-
H2S + 2OH- 
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com