
10、实践表明,我国的民主选举将在相当长的一段时间内采用直接选举和间接选举相结合的方式。选择不同选举方式的主要制约因素有
①社会经济制度 ② 物质生活条件
③ 选民的文化水平 ④选民和候选人的意愿
A ①②③ B、②③④ C、①③④ D、①②④
9.下列有关村民自治的观点,正确的是
①村民可以直接投票选举村干部 ②村委会主任由乡镇政府任命
③村民自治章程和村规民约只要对村民有利就行
④村务公开、民主评议村干部、村委会定期报告工作等形式,都是村民自治的重要方式
A.①② B.②③ C.①④ D.③④
8.在我国,实行村民自治和城市居民自治是
①发展社会主义民主的基础性工作
②社会主义民主最为广泛而深刻的实践
③基层民主中公民参与政治生活的重要形式
④村民和城市居民自我管理、自我教育的基层政权组织
A.①②③ B.②③④ C.①③④ D.①②④
7、据报载,广东等地已开始实行政府财政预算的细化和公开化,增加政府开支的透明度,有人称之为“阳光财政”和“玻璃钱柜”。实施“阳光财政”和“玻璃钱柜” ①有利于进一步树立政府的良好形象 ②便于政府自觉接受人民监督 ③体现了政府职能的转变 ④可以进一步推动政府廉政建设 ⑤有利于实行民主监督 A.①②③ B.③④ C.①②④⑤ D.①②
6.一个城管执法人员,发现几名小摊贩占道贩卖日用品,不仅影响附近商店的正常营业,还造成交通阻塞。但该城管执法人员由于同情小摊贩谋生艰难,采取了不予理睬的态度。该城管执法人员违反了依法行政
①程序正当要求 ②高效便民要求 ③合法行政要求 ④合理行政要求
A.①② B.②③ C.③④ D.③
5.海水开发,大势所趋。天津是国家确定的海水淡化示范城市,市政府将淡化海水纳入水资源进行统一配置,建立专项资金,采取一系列扶持措施,使海水淡化产业实现重大突破。市政府的决策主要是在履行
A.政治职能 B.经济职能 C.文化职能 D.环保职能
2月26日一份由196名选民联名递交的人大代表罢免函,摆在了天津市河东区人大常委会的工作案头。这是目前规模最大的一次由选民直接提请的人大代表罢免动议。据此回答1-2题。 1、196名选民提交罢免函,是符合我国《选举法》规定的,这是公民依法行使权利的表现。这表明( ) A.人民民主专政是新型的民主和新型的专政 B.我国的人民民主具有广泛性的特点 C.我国的人民民主具有真实性的特点 D.我中的人民民主专政是工人阶级领导的国家政权 2、选民要求罢免代表,在中国政坛吹来一股清新的民主之风。这表明( ) ①我国社会主义民主政治不断发展 ②建设我国的民主政治必须从我国国情出发 ③我国人民的民主意识不断增强 ④要把人民当家作主和坚持党的领导结合起来 A.①②③④ B.①④ C.②③ D.①③ 3、2010年是虎年,有的单位打出招聘广告说:今年招工不招属虎的。有的则在广告上说:不招某省的人。从政治生活角度看,这些单位的做法( ) A.是在履行自己的政治自由 B.违背了权利与义务相统一的原则 C.违背了公民在法律面前一律平等的原则 D.违背了个人利益与集体利益、国家利益相4、据报载,乌鲁木齐市三位青年因当地某酒店悬挂国旗不当而向法院对该酒店提起了诉讼。这三位公民( ) A.正确行使了公民的政治权利和自由 B.正确行使了民主监督的权利 C.自觉履行了维护国家利益的义务 D.坚持了个人利益和国家利益、集体利益相结合
17.(2010江苏卷)(8分)下表列出了3种燃煤烟气脱硫方法的原理。
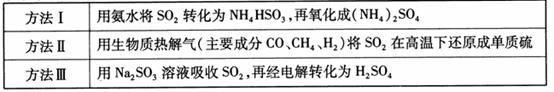
(1)
方法Ⅰ中氨水吸收燃煤烟气中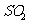 的化学反应为:
的化学反应为:
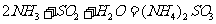
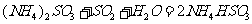
能提高燃煤烟气中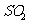 去除率的措施有 ▲ (填字母)。
去除率的措施有 ▲ (填字母)。
A.增大氨水浓度
B.升高反应温度
C.使燃煤烟气与氨水充分接触
D. 通入空气使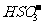 转化为
转化为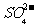
采用方法Ⅰ脱硫,并不需要预先除去燃煤烟气中大量的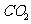 ,原因是▲(用离子方程式表示)。
,原因是▲(用离子方程式表示)。
(2) 方法Ⅱ重要发生了下列反应:
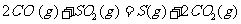
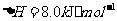
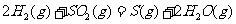
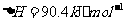
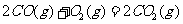
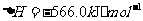
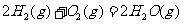
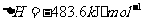
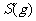 与
与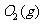 反应生成
反应生成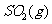 的热化学方程式为
。
的热化学方程式为
。
(3)
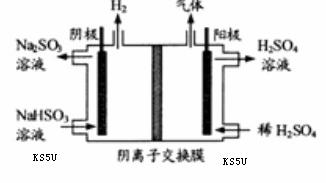
方法Ⅲ中用惰性电极电解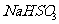 溶液的装置
溶液的装置
如右图所示。阳极区放出气体的成分为 。
(填化学式)
[答案]
(1)AC
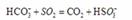
(2)S(g)+O2(g)= S O2(g) H=-574.0kJmol-1
(3) O2 SO2
[解析]本题考察的知识比较散,涉及到环境保护,一道题考察了几个知识点。覆盖面比较多。但盖斯定律、热化学方程式、离子方程式、点击方程式都是重点内容(1)提高SO2的转化率,可以增大氨水的浓度、与氨水充分接触;不需要通入CO2的原因是因为HCO3+SO2=CO2+HSO3而产生CO2 (2)主要考察盖斯定律的灵活运用。适当变形,注意反应热的计算。不要忽视热化学方程式的书写的注意事项。(3)阴极的电极产生的气体为O2和SO2.
25.(2010上海卷)接触法制硫酸工艺中,其主反应在450℃并有催化剂存在下进行:
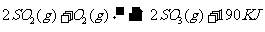
1)该反应所用的催化剂是 (填写化合物名称),该反应450℃时的平衡常数 500℃时的平衡常数(填“大于”、“小于”或“等于”)。
2)该热化学反应方程式的意义是 .
a.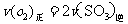 b.容器中气体的平均分子量不随时间而变化
b.容器中气体的平均分子量不随时间而变化
c.容器中气体的密度不随时间而变化 d.容器中气体的分子总数不随时间而变化
4)在一个固定容积为5L的密闭容器中充入0.20
mol SO2和0.10molSO2,半分钟后达到平衡,测得容器中含SO30.18mol,则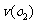 = mol.L-1.min-1:若继续通入0.20mol SO2和0.10mol O2,则平衡 移动(填“向正反应方向”、“向逆反应方向” 或“不”),再次达到平衡后, mol<n(SO3)< mol。
= mol.L-1.min-1:若继续通入0.20mol SO2和0.10mol O2,则平衡 移动(填“向正反应方向”、“向逆反应方向” 或“不”),再次达到平衡后, mol<n(SO3)< mol。
答案:1)五氧化二钒(V2O5);大于;2)在450℃时,2molSO2气体和1molO2气体完全反应生成2molSO3气体时放出的热量为190kJ;3)bd;4)0.036;向正反应方向;0.36;0.40。
解析:此题考查了工业制硫酸、化学平衡常数、热化学方程式、化学平衡状态、有关化学平衡的计算等知识。1)工业制硫酸时二氧化硫催化氧化使用的催化剂是五氧化二钒;该反应正向放热,故温度越高化学平衡常数越小;2)热化学方程式表示的是450℃时,2molSO2气体和1molO2气体完全反应生成2molSO3气体时放出的热量为190kJ;3)根据化学平衡状态的特征,容器中气体的平均相对分子质量不随时间变化、分子总数不随时间变化时,说明反应达到平衡状态;4)当达到平衡时,容器中SO3的物质的量为0.18mol,则v(SO3)=0.072mol.L-1.min-1,则v(O2)=0.036mol.L-1.min-1;再继续通入0.20molSO2和0.10molO2时,平衡向正反应方向移动,在此达到平衡时,SO3的物质的量介于0.36和0.40之间。
知识归纳:化学平衡常数只是和温度相关的函数,其随温度变化而变化。若正反应为吸热反应,温度升高K值增大;若正反应为放热反应,温度升高K值减小。
23.(2010福建卷)(15分)
J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如右表;J元素最低负化合价的绝对值与其原子最外层电子数相等;M是地壳中含量最多的金属元素。
(1)M的离子结构示意图为_____;元素T在周期表中位于第_____族。
(2)J和氢组成的化合物分子有6个原子,其结构简式为______。
(3)M和T形成的化合物在潮湿的空气中冒白色烟雾,反应的化学方程式为_____。
(4)L的最简单气态氢化物甲的水溶液显碱性。
①在微电子工业中,甲的水溶液可作刻蚀剂H2O2 的清除剂,所发生反应的产物不污染环境,其化学方程式为______。
②一定条件下,甲在固定体积的密闭容器中发生分解反应(△H>0)并达平衡后,仅改变下表中反应条件x,该平衡体系中随x递增y递减的是_______(选填序号)。
|
选项 |
a |
b |
c |
d |
|
x |
温度 |
温度 |
加入H2的物质的量 |
加入甲的物质的量 |
|
y |
甲的物质的量 |
平衡常数K |
甲的转化率 |
生成物物质的量总和 |
(5)由J、R形成的液态化合物JR2 0.2mol在O2中完全燃烧,生成两种气态氧化物,298K时放出热量215k J。
该反应的热化学方程式为________。
J。
该反应的热化学方程式为________。
解析:
(1) J元素最低负化合价的绝对值与其原子最外层电子数相等,可以判断J元素为碳元素;M是地壳中含量最多的金属元素为铝元素;根据J、R在周期表中的相对位置可以判断R为硫元素,则T为氯元素,处于第三周期第七主族
(2)J和氢组成含有6个原子的分子为乙烯,其结构简式为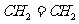
(3)M和T形成的化合物为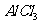 ,与水反应
,与水反应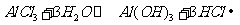 ,其中氯化氢气体呈雾状
,其中氯化氢气体呈雾状
(4)①氨水与双氧水发生氧化还原反应: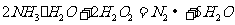
生成无污染的氮气;
②甲在固体体积的密闭容器中发生分解反应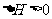 ,
,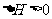 表明正反应为吸热反应,升高温度,平衡朝着正方向移动,甲物质的量减少;加入
表明正反应为吸热反应,升高温度,平衡朝着正方向移动,甲物质的量减少;加入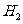 的物质的量即增加生成物的浓度,平衡朝逆方向移动,甲的转化率减小
的物质的量即增加生成物的浓度,平衡朝逆方向移动,甲的转化率减小
(5)JR2为CS2,燃烧生成二氧化碳和二氧化硫,依题意可以很快的写出反应的热化学方程式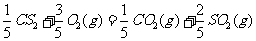
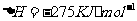
答案:(1) 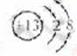 ;
ⅦA
;
ⅦA
(2)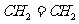
(3)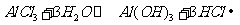 ,
,
(4)①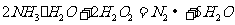
②a和c;a或c
(5)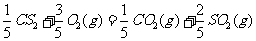
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com