
2、反应离子方程式:
(1)
(2)
1、实验现象: 3、图像
(1)
(2)
2、反应离子方程式:
(1)
(2)
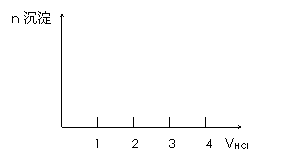 (三)向Na AlO2溶液中滴加HCl溶液至过量
(三)向Na AlO2溶液中滴加HCl溶液至过量
2、反应离子方程式:
(1)
(2)
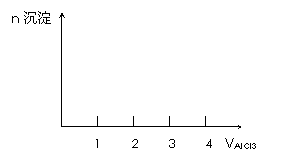 (二)向NaOH溶液中滴加AlCl3溶液至过量
(二)向NaOH溶液中滴加AlCl3溶液至过量
1、实验现象: 3、图像
(1)
(2)
2、化学性质
[实验1]从广口试剂瓶中取2片打磨好的镁条放入一支试管,加入少量水,滴入2-3滴酚酞,加热煮沸。观察现象。
[实验2]取一根4-5cm长的镁条,用砂纸将表面的氧化镁擦去,用坩埚钳夹持镁条,在酒精灯上点燃后,伸入充满二氧化碳的集气瓶中,观察现象。
[实验3]在一支试管中放入一小段擦去氧化膜的镁条,再向试管中加入一定量的稀硫酸,观察现象。
实验记录
|
序号 |
实验现象 |
实验结论(相关的化学方程式) |
|
实验1: |
|
|
|
实验2: |
|
|
|
实验3 |
|
|
[知识总结]镁的化学性质:
(1)与非金属的反应
与氧气反应 、
与氯气反应 、
与氮气反应
(2)与水反应:
(3)与二氧化碳反应:______________________________________
(4)与酸反应(盐酸、硫酸等)
_______________________________________、_____________________________
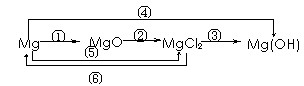 [归纳总结]根据本节课所学知识,结合下图转化关系完成方程式,并说明镁的重要用途。
[归纳总结]根据本节课所学知识,结合下图转化关系完成方程式,并说明镁的重要用途。
①
②
③
④
⑤
⑥
[练习]金属镁可用于火箭、飞机、轮船的制造。镁在现代材料工业中需求量逐渐增大。海水中含有约0.129%的镁元素,仅次于氯和钠,总储量约1800亿吨,开发潜力很大。
⑴在提取镁的生产过程中,需要浓缩海水,提高海水中MgCl2的质量分数,你认为既环保又经济的方法是 。
⑵浓缩海水中MgCl2的质量分数为9.150%,求要将150吨浓缩海水中MgCl2都转化为Mg(OH)2,理论上需要Ca(OH)2多少吨?(相对原子质量:Mg 24 Cl 35.5 Ca 40 O 16 H 1)
1、物理性质:镁是 色的金属固体,是热和电的良导体,质地 。硬度较 ,熔点较低,镁的密度较_____,镁能与铜、铝、锡、锰、钛等形成许多合金,但是硬度和强度都很____,因此镁合金被大量用于制造 、 和 的部件,氧化镁的熔点可以达到2800℃,是很好的______材料
海水提镁的步骤:
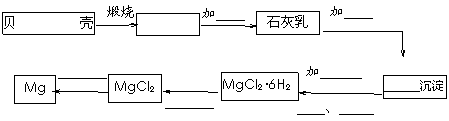
相关的化学反应方程式为: ①
② ③
④ ⑤
[思考]海水中提取镁的过程中,海水沉淀池中得到氢氧化镁沉淀时为什么加入的是石灰乳而不是NaOH溶液?
电解得到金属镁为什么不采用电解熔融的氧化镁?
电解产生的Cl2怎么处理?
2、写出下列反应的化学方程式: MgCl2+ NaOH ==
Mg(OH)2+ H2SO4=== Mg(OH)2
学习过程
3、认识化学在自然资源综合利用方面的重要价值
学习重点:镁的化学性质
知识牵引:1、自然界的镁主要以 的形式存在于 和海水中,海水中镁的总储量约为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com